Clear Sky Science · ja
分割ビオチンリガーゼ法により、凝集過程で多量体化したα-シヌクレインに関連するタンパク質を明らかにする
脳内のタンパク質の塊が重要な理由
パーキンソン病や関連疾患では、本来は役立つ脳タンパク質であるα-シヌクレインが粘着性のある塊、レビー小体として凝集することがあります。これらの沈着は症状が現れる何十年も前から出現し、剖検での特徴的所見ですが、α-シヌクレインを無害な状態から有害な凝集体へ押しやる他のどのタンパク質が関与しているかはまだ分かっていません。本研究では巧妙な分子「近接タグ」を用いて、α-シヌクレインが単量体から小さな塊へ移行する際にどのタンパク質がその近くにいるかをマップし、病気の始まり方や遅らせる・防ぐために標的にできそうな経路について新たな手がかりを示しています。
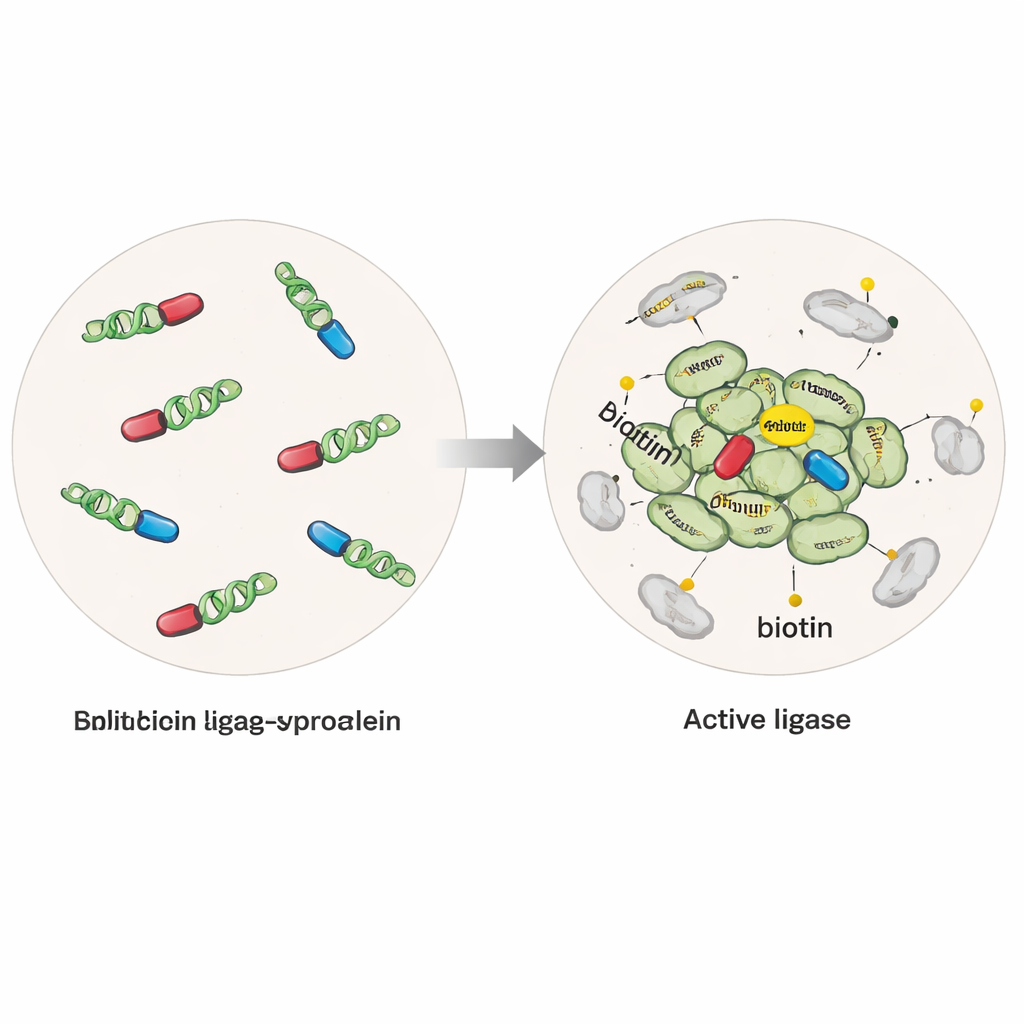
近くの分子を光らせる分子“タグ”
研究者らはヒト細胞に、改変酵素と融合したα-シヌクレインを発現させました。この酵素は数ナノメートルよりさらに小さい範囲内にある任意のタンパク質に小さなビオチンタグを付与できます。一つのバージョンでは酵素が完全な形で常に活性であり、単量体の近傍や凝集体の周辺にいるタンパク質を捕捉しました。もう一つの選択的な「分割」バージョンでは、酵素を2つの不活性な断片に分け、それぞれを別のα-シヌクレイン分子に結合させました。α-シヌクレイン同士が多量体やオリゴマーとして集合して初めて断片が再び結合して活性酵素となり、初期の凝集体の周辺だけでタグ付けが起こります。精製したα-シヌクレイン繊維(フィブリル)を細胞に加えることで、病的な凝集を誘導し、正常状態と病的状態を比較することも可能にしました。
近傍タンパク質の地図作り
タグ付けの時間を与えた後、チームはすべてのビオチン標識タンパク質を回収し、質量分析法で同定しました。この手法はタンパク質を高精度に質量と量で識別します。全条件で1277種類の異なるタンパク質が見つかり、慎重なフィルタリングを経てα-シヌクレインの近傍に実際に存在すると考えられる581種に絞られました。完全型と分割型の酵素系を比較することで、主に単量体に付随するタンパク質と多量体を好むタンパク質を区別できました。また、フィブリルを加えた細胞と加えていない細胞を比較して、凝集が誘発されたときにα-シヌクレインの局所的なタンパク質環境がどう変わるかを調べました。
凝集体に取り込まれる主要な細胞経路
得られた相互作用ネットワークの概要は、いくつかの主要な生物学的テーマを示しています。正常条件下では、多量体化したα-シヌクレインは多くの膜輸送関連タンパク質やタンパク質修飾酵素の近くにあり、シナプス小胞の管理やタンパク質品質管理に関与するという提案と一致します。PAK4、RIPK2、MAP4K4などのリン酸基を付加するキナーゼが健康な多量体の近くで濃縮していた一方、凝集体が形成されると接触を失うように見え、これらの関係の破綻が病的形態を促す可能性を示唆しています。チームはまたインスリン様成長因子(IGF)シグナルに関連するタンパク質を検出し、インスリン抵抗性とパーキンソン病の臨床的関連を支持する所見を示しました。さらに、14-3-3シャペロンファミリーや特定の細胞内分解経路の構成要素など、損傷タンパク質の処理に関わるタンパク質が凝集に伴って動員されることも明らかになりました。
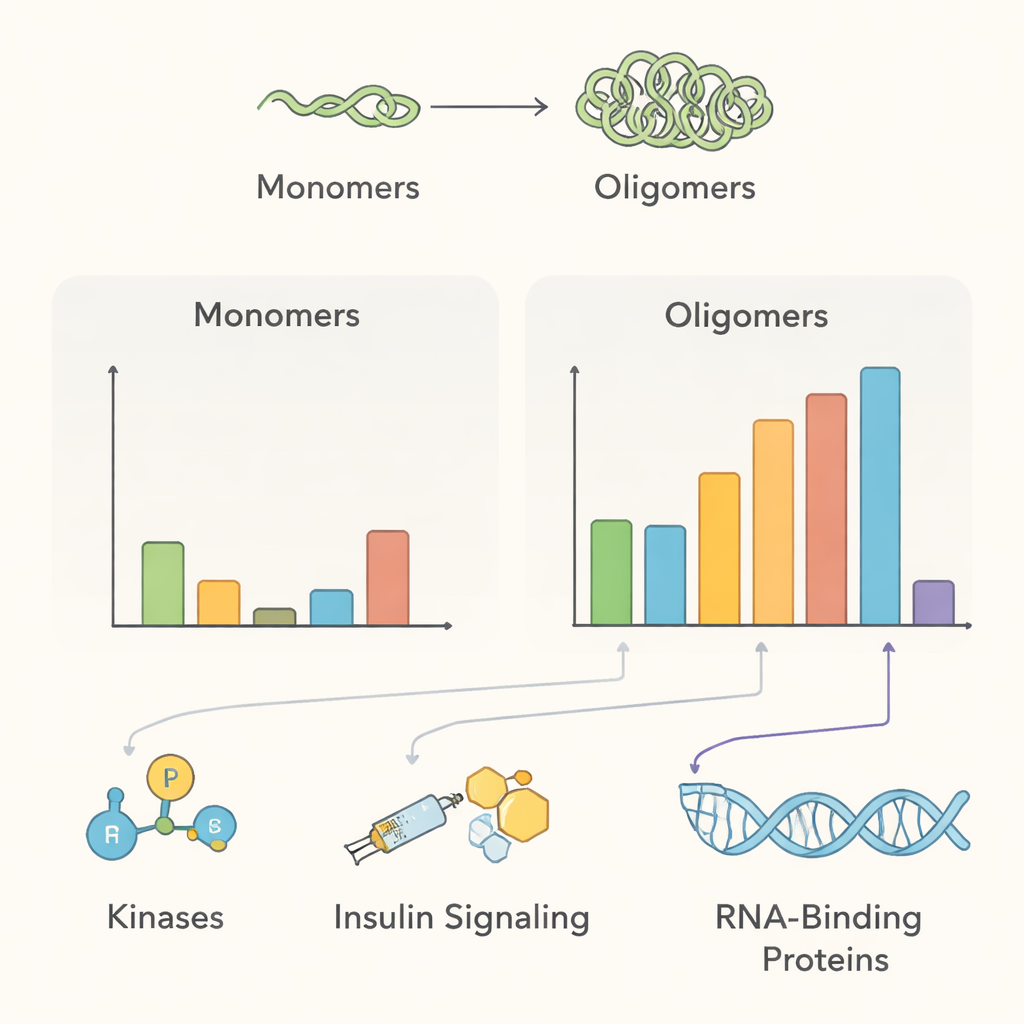
他の脳疾患への思いがけない橋渡し
パーキンソン病を越えて、データは筋萎縮性側索硬化症(ALS)や前頭側頭型認知症(FTD)との驚きの関連を浮かび上がらせます。FUSと呼ばれるRNA結合タンパク質は、これらの疾患で誤局在化して凝集することが知られており、正常条件でも凝集誘導条件でも多量体化したα-シヌクレインの近くに存在していました。他のRNA関連タンパク質も、α-シヌクレインの凝集に伴って近接性を変化させました。これらの発見は、小さなα-シヌクレイン集合体がRNA取り扱いタンパク質を細胞内の不適切な場所に閉じ込める可能性を示唆し、レビー小体疾患とALS/FTDの生物学を結びつける可能性がありますが、直接の物理的相互作用はまだ検証が必要です。
疾患理解における意義
非専門家向けの主な要点は、この研究がα-シヌクレインが正常な助け手から有害な塊へ移る過程で共に移動するタンパク質の初期段階の「接触リスト」を提供したことです。研究は、特定のキナーゼや品質管理酵素との保護的関係を失うことが、新しい有害なパートナーを獲得することと同じくらい重要かもしれないことを示唆します。実験は単純化された細胞モデルで行われており、因果関係を証明するものではありませんが、ニューロンや脳組織での今後の検証に向けた具体的な候補や経路を浮かび上がらせています。長期的には、これらの変化するタンパク質近隣関係を地図化することで、保護的相互作用の回復、インスリン関連シグナルの支援、あるいはRNA結合タンパク質の捕捉の防止といった戦略を導き、微妙な分子変化から完全なレビー小体疾患への進行を遅らせる可能性があります。
引用: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
キーワード: α-シヌクレイン, レビー小体病, タンパク質凝集, 近接プロテオミクス, パーキンソン病