Clear Sky Science · ja
Mg-プロトポルフィリンによるNaV1.5チャネルの高選択的電位センサー閉塞はがん細胞の遊走を阻害する
植物色素が示す新しいがん戦略
心臓と腫瘍が思いがけない共通の脆弱性を持つ可能性があります。それは細胞膜にある特殊な電気的ゲート、NaV1.5です。本研究は、植物のクロロフィルの構成要素に近縁の天然物質、マグネシウム‑プロトポルフィリンIX(MgPpIX)がこのゲートを極めて高精度に閉塞できることを示しています。これにより一部のがん細胞の移動が鋭く遅くなり、光合成化学に着想を得た分子が脳や筋肉を大きく乱すことなく転移を抑える手段になりうることを示唆します。
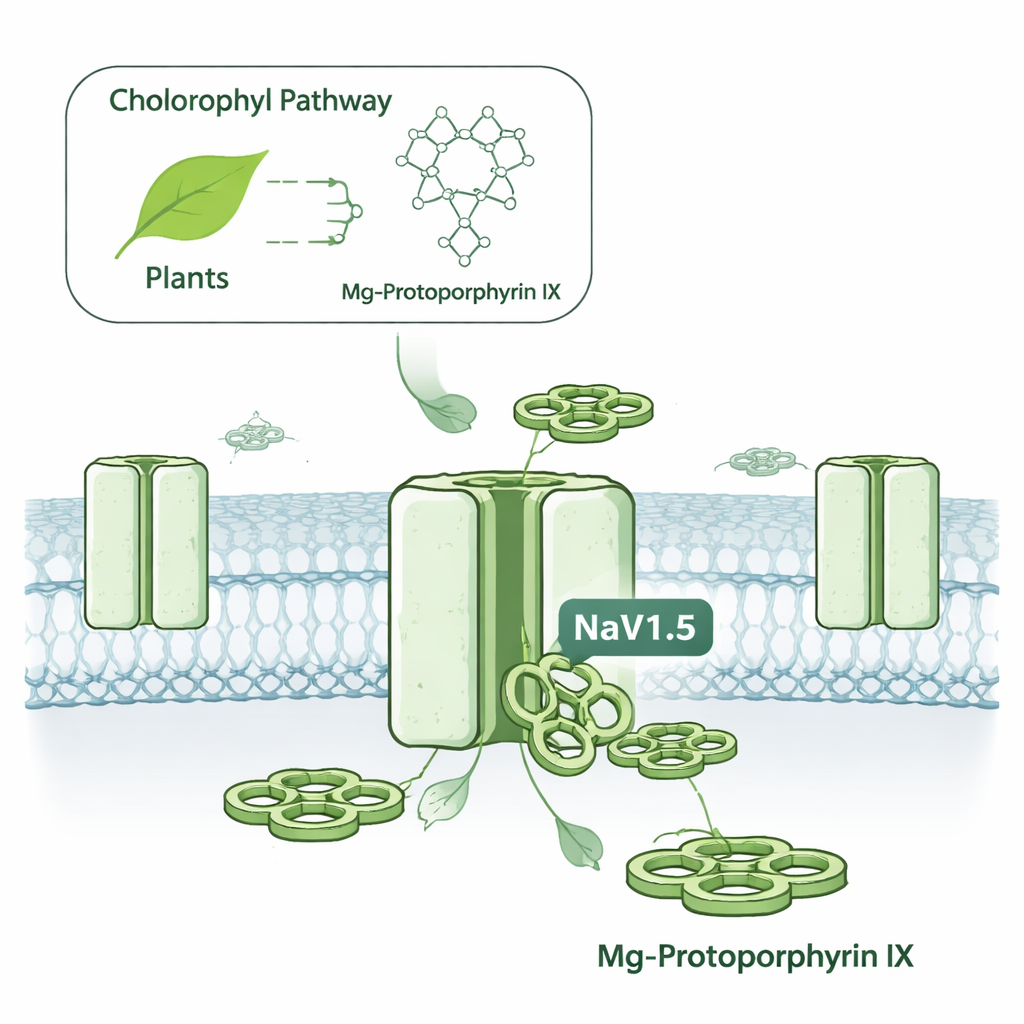
がん細胞に潜む電気的スイッチ
細胞は電位依存性ナトリウムチャネルを微小な扉として使い、イオンの出入りを通じて電気信号を生み出します。NaV1.5は心拍の発生に関与することでよく知られていますが、同じチャネルは乳がんや結腸がんなどいくつかのがんでも発現しており、その活動は細胞運動性や浸潤性の増大に結び付けられてきました。NaV1.5を標的にするのは困難でした。なぜなら従来の多くのナトリウムチャネル薬は神経や骨格筋の関連チャネルにも作用し、発作、しびれ、筋力低下などの副作用を招く危険があるからです。著者らは、いかなる小分子がNaV1.5をその近縁体から高い選択性で識別できるかを明らかにしようとしました。
記録的な精度を示す植物由来阻害剤
研究チームはヘムや植物のクロロフィルの芯に似た環状分子族、すなわち金属プロトポルフィリンを調べました。これらは中心金属が異なるだけの類縁化合物です。培養細胞で発現させたヒトNaV1.5チャネルに各種を適用したところ、ひとつの化合物が際立ちました:MgPpIXです。これはナノモーラー濃度でNaV1.5をほぼ99%抑制し、鉄を中心金属とする同族体(ヘミン)より約100倍強力でした。ニッケルや銅を含む他の金属体はほとんど不活性でした。注目すべきは、MgPpIXが同濃度で脳、末梢神経、骨格筋で用いられる他のいくつかのヒトナトリウムチャネル型にはまったく影響を与えなかったことで、このチャネル族に対する選択性はこれまで報告された中でも最も鋭い部類に入ります。
分子が小さな電位レバーを塞ぐ仕組み
この異常な精度を理解するために、研究者らは遺伝学的手法と計算機シミュレーションを組み合わせました。ナトリウムチャネルは4つの繰り返しドメインをもち、それぞれに膜電位変化で位置を変える「電位センサー」が含まれます。NaV1.5と感受性の低い近縁体の間で個々のアミノ酸を交換することで、MgPpIXの作用は第2ドメインの電位センサー、特に細胞外に露出した2つの残基に起因することが突き止められました。現実的な膜環境での分子動力学シミュレーションは、MgPpIXが電位センサーの休止状態(“ダウン”)にあるときにそのそばに収まることを示唆しました。MgPpIXの陽性に帯電した金属中心はチャネル上の負に帯電した側鎖に引き付けられ、平らな環は周囲の脂質と相互作用します。この結合は電位センサーを所定の位置に固定し、“アップ”の活性状態へ移行できなくすることでチャネルを閉じたままにするようです。興味深いことに、心拍のような強い脱分極はこの分子を一時的に払いのけることがあり、著者らはこれを「逆使用依存性」と表現しています。
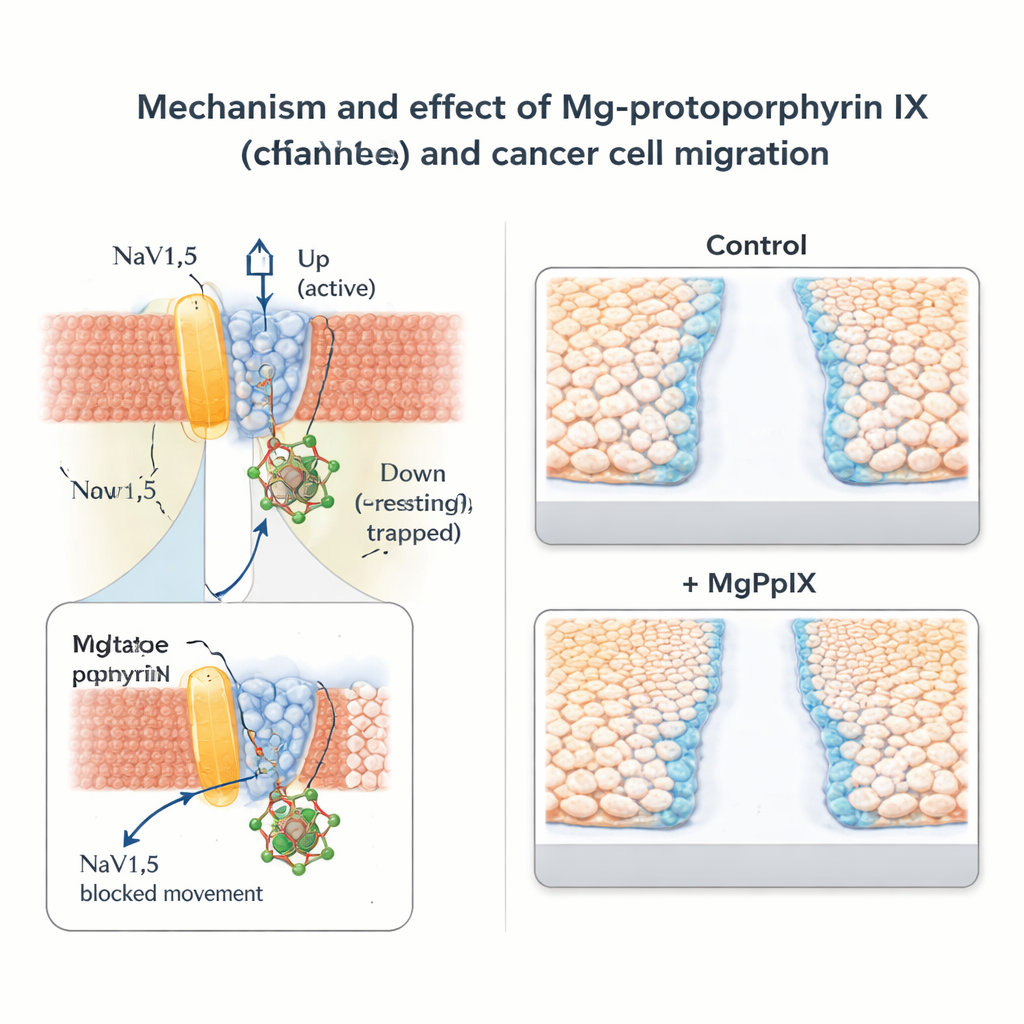
広範な神経遮断なしにがん細胞の移動を遅らせる
つづいて研究チームは、この分子的ブレーキががんの挙動に何をもたらすかを調べました。NaV1.5を自然発現する乳がん(MDA-MB-231)および結腸がん(SW-480)細胞株では、MgPpIXはナトリウム電流を劇的に低下させ、標準的なスクラッチアッセイやトランスウェルアッセイで細胞の遊走を遅延させました。ある金属プロトポルフィリンがNaV1.5を多く阻害するほど、細胞移動の阻害も強くなり、チャネル活動と運動性の関連が裏付けられました。対照的にNaV1.5を欠くがん細胞株では、電気的にも遊走試験でもMgPpIXに反応せず、作用は一般的な毒性ではなく高度に特異的であることを支持します。古典的なナトリウムチャネル毒素テトロドトキシンと比べても、MgPpIXははるかに低濃度でより強い移動抑制を達成しました。
抗転移薬としての期待と注意点
専門外の読者に向けた中心的なメッセージは、研究者らが心臓型の電気ゲートを精密に挟み込む植物関連分子を見つけたということです。ゲートの小さな電位レバーを休止位置に閉じ込めることで、MgPpIXは実験室内でがん細胞の運動性を強く抑えつつ、感覚や運動に不可欠な他のナトリウムチャネルを温存します。心臓の迅速な電気活動がこのブロックを部分的に解除し得るため、腫瘍細胞が心臓細胞よりも大きく抑制される安全域が存在する可能性すらあります。MgPpIX自体がそのまま薬になるかは別として、その独特な結合部位と作用機序は、NaV1.5を前例のない選択性で標的とする将来の薬剤設計にとって強力な設計図を提供します。
引用: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
キーワード: ナトリウムチャネル, Nav1.5, がん細胞の遊走, クロロフィル由来分子, 標的化イオンチャネル薬