Clear Sky Science · ja
マウスとサルの中脳ドーパミン作動性ニューロンを標的とするMiniPromoters Ple384(TH)とPle388(PITX3)
なぜこの研究が脳の健康に重要なのか
脳のドーパミン産生細胞は、私たちの運動、報酬からの学習、そしてモチベーションの維持に関わります。これらはまた、パーキンソン病で失われる細胞でもあります。研究者や医師は、ラボ動物だけでなく将来的には人体でも、これら脆弱なニューロンに特異的に有用な遺伝子や分子ツールを届けたいと考えています。しかし、遺伝子治療を正しい細胞だけで作動させ、脳全体に広がらないようにすることは大きな障害でした。本研究は、マウスとサルの中脳ドーパミンニューロンでほぼ選択的に遺伝子を駆動できる、コンパクトなDNAの“スイッチ”を二つ報告し、より精密で安全性の高い治療への道を開きます。
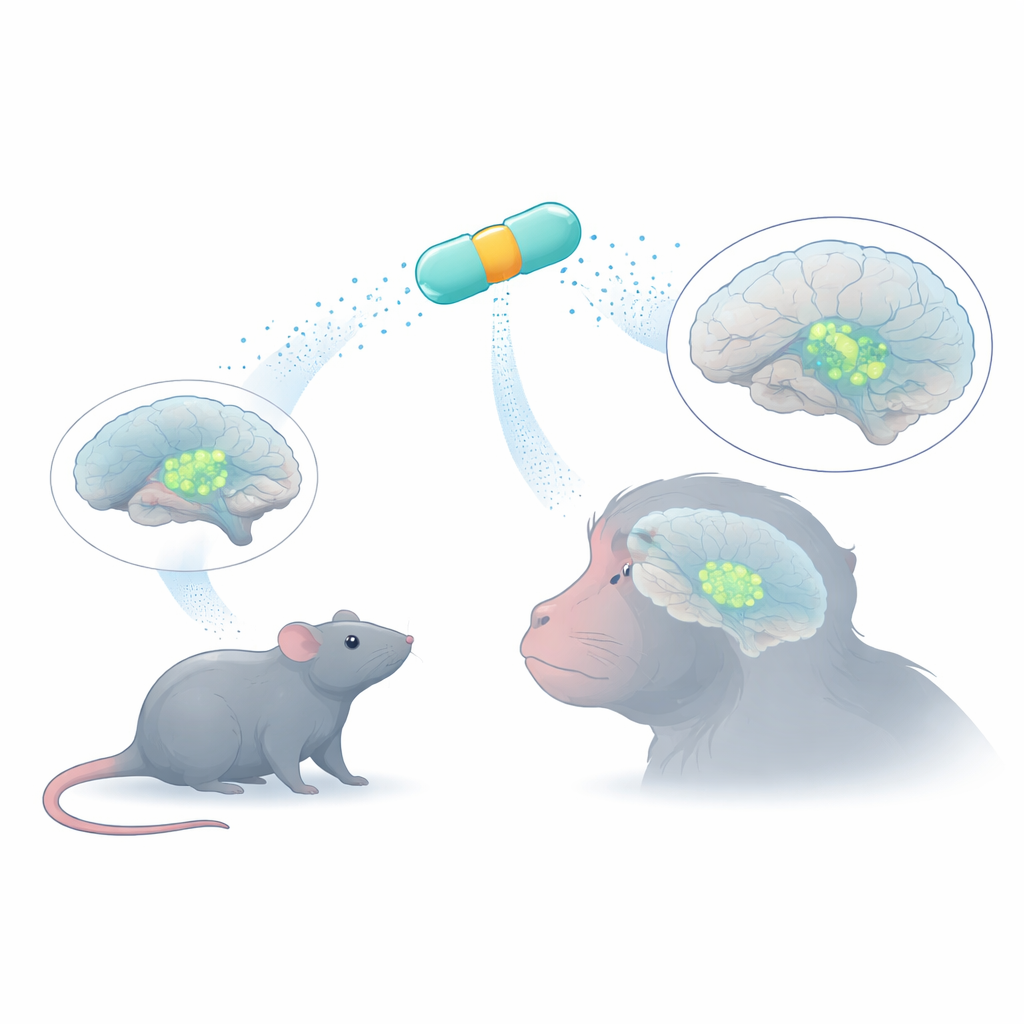
小さな遺伝的スイッチに託された大きな役割
治療用遺伝子を脳細胞に届けるため、研究者はしばしばアデノ随伴ウイルス(AAV)という、無害で限られた量のDNAしか搭載できない輸送体を使います。各ウイルス内では短いプロモーター配列がオン・オフのスイッチの役割を果たし、その遺伝子がどこで活性化されるかを決めます。多くの天然プロモーターは大きすぎるか粗く、遺伝子を多くの細胞型で作動させてしまいます。研究チームはバイオインフォマティクスを用いて、人間のDNAから8つの非常にコンパクトな“MiniPromoter”を設計しました—ドーパミン合成ニューロンを示すことで知られる遺伝子から取った制御要素を短く組み合わせたものです。彼らの目標は、AAVに収まる十分な小ささを保ちつつ、強くかつ細胞型に特異的な発現を駆動するスイッチのセットを作ることでした。
マウス脳で適切な標的を探す
8つの候補MiniPromoterはまずマウスで試験されました。各プロモーターは緑色蛍光タンパク質を運ぶAAVに組み込まれ、どこでスイッチが作動するかを可視化しました。ウイルスは血流内に注入するか、脳の液体貯留空間に直接投与しました。多くのMiniPromoterは選択性に欠け、あるものは多数の非ドーパミン細胞を点灯させ、別のものはほとんど働きませんでした。その中で二つが際立ちました。ひとつはPle384で、これはすべてのカテコールアミン産生ニューロンで使われる主要酵素であるチロシンヒドロキシラーゼ(TH)の制御領域から構成されています。もうひとつはPle388で、中脳ドーパミンニューロンのサブセットに重要な遺伝子PITX3に由来します。Ple384とPle388はともに、黒質緻密部と腹側被蓋野—ドーパミンニューロンの中脳ハブ—で明るく強く限定されたシグナルを示し、標識された細胞の90%以上がドーパミンの特徴的分子を持っていました。
深く掘らずにマウスからサルへ
ヒト疾患を目指した遺伝子治療は最終的に脳が大きく複雑な霊長類でも機能しなければなりません。黒質へ直接注入することは技術的に困難で、この小さく深い構造を損傷する可能性があります。そこで研究者らは、同じMiniPromoterを横脳室への単回注射を介してニホンザルの脳脊髄液中に送達できるかを試しました。液体空間から広く拡散することが知られたAAVカプシド変異体を用い、Ple384とPle388はいずれも黒質および腹側被蓋野の中脳ドーパミンニューロンで堅牢な発現を駆動し、視床下部や青斑核のような他のドーパミン豊富領域は大部分回避されました。標的領域で標識された細胞の大多数がドーパミンニューロンであり、スイッチが種を超えて選択性を保つことが確認されました。
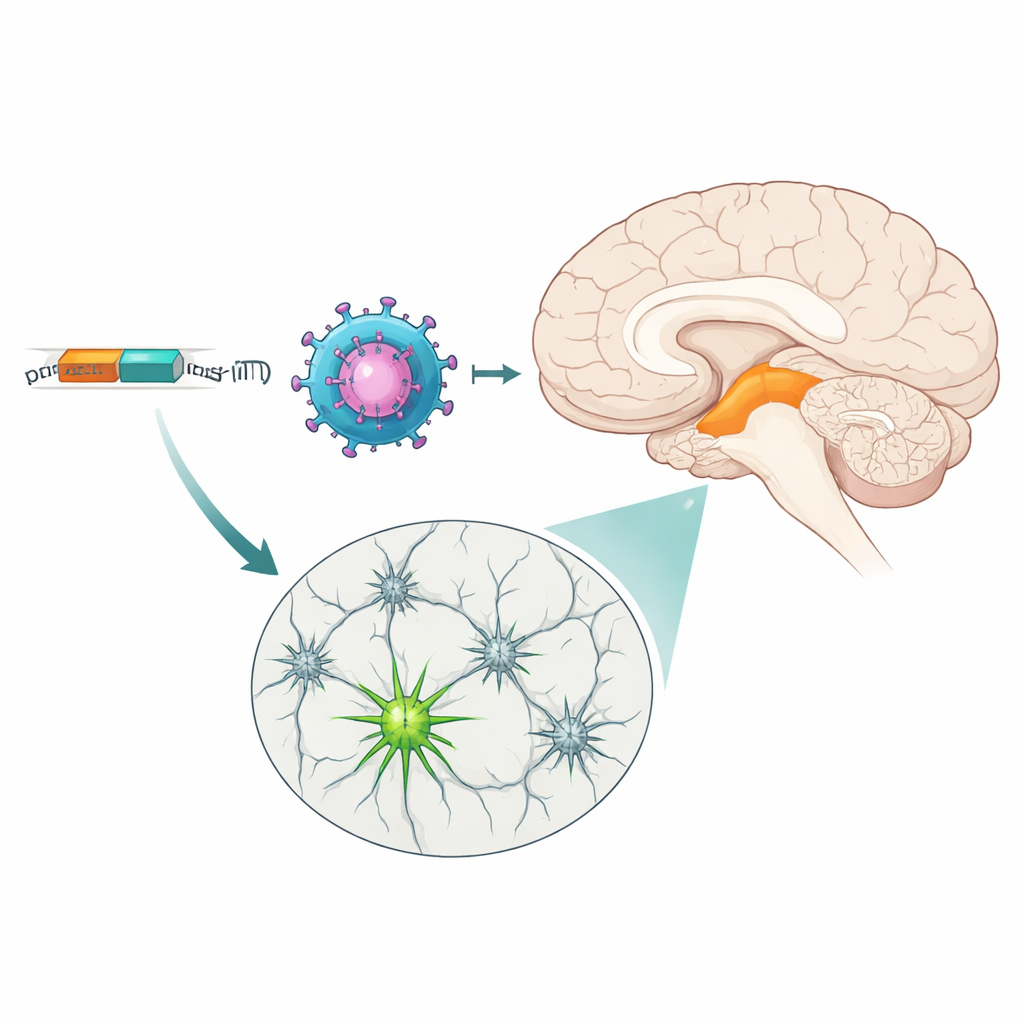
異なる強みを持つ二つのツール
両方のMiniPromoterは標的を捉えましたが、表現パターンは異なりました。より広範なチロシンヒドロキシラーゼ遺伝子に基づくPle384は、より多くのニューロンを点灯させ、黒質の腹側・背側層ともに覆い、腹側被蓋野のより大きな領域にも及びました。より制限されたPITX3に由来するPle388は、主に腹側層のニューロンのサブセットを標識し、蛍光は弱めでした。オフターゲットの発現は主に注入部位近傍や血流投与後の一部の末梢器官で見られましたが、対照実験はウイルスベクターが多くの脳領域に到達できることを示しており、発現を中脳ドーパミンニューロンにほぼ限定しているのはMiniPromoter自身であることが示唆されます。この強度の調整可能性—一つはより強力で広範、もう一つはより選択的で中程度—により、穏やかな調節から広範な介入まで、目的に応じて適したスイッチを研究者が選べます。
将来の治療にとっての意味
専門外の方に向けた要点は、著者らがマウスとサルのドーパミンニューロンに対して精密でプログラム可能な照明スイッチのように働く二つのコンパクトな遺伝的スイッチを作成したことです。Ple384はこれらの細胞へ強力で広範なアクセスを提供し、Ple388はより狭く、特に脆弱なサブセットに焦点を当てます。これらのスイッチは一般に用いられるウイルスベクター内に十分収まる小ささであるため、治療遺伝子の搭載余地を残し、望ましくない脳領域を避けることで副作用を減らすのに役立つ可能性があります。パーキンソン病や関連疾患の遺伝子治療が進むにつれて、こうした標的化された制御要素は、強力でありながら精密な治療を構成する重要な要素となるでしょう。
引用: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
キーワード: ドーパミンニューロン, 遺伝子治療, パーキンソン病, AAVベクター, 細胞特異的プロモーター