Clear Sky Science · ja
バルクおよび単一細胞シーケンシング解析で明らかになったCOPDに関連する酸化ストレス遺伝子TPPP3とVEGFA
なぜこの肺の研究があなたに関係あるのか
慢性閉塞性肺疾患(COPD)は、年々呼吸が徐々に困難になる病気であり、現在では世界で第3位の死因となっています。喫煙や大気汚染が主要な原因として知られていますが、医師は病気を早期に捉えたり、肺内部で進行する損傷を止めたりするための正確なツールをまだ十分に持っていません。本研究は、大規模な遺伝子データセット、単一細胞解析、実験室での検証を組み合わせて、「酸化ストレス」——有害な酸素由来の副産物が体の防御を圧倒して引き起こす損傷——に関連する特定の遺伝子を明らかにし、それらがCOPDにおける肺線維化や気道のリモデリングをどう促すかを示しています。
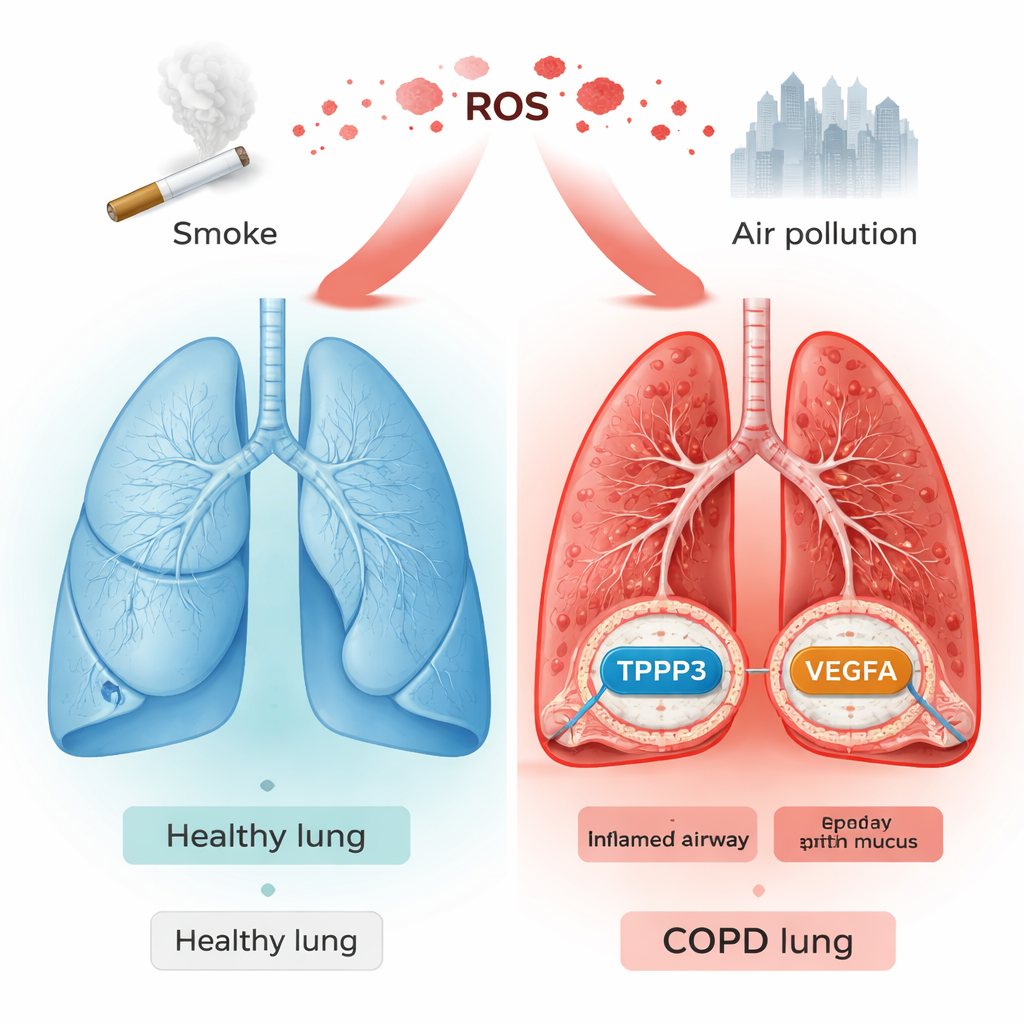
肺の内部で起きる有害な火花
呼吸ごとに取り込まれるのは酸素だけではなく、特にタバコの煙に含まれる粒子や化学物質も入ってきます。これらは活性酸素種(ROS)を発生させることがあり、ROSは不安定な分子で小さな火花のように細胞を傷つけ、慢性炎症を引き起こします。COPDではこうした火花が何年も燃え続け、徐々に気道を狭め、肺胞を破壊していくと考えられます。著者らは、COPDにおける酸化ストレスと最も強く結び付くヒト遺伝子を特定し、病気を早期に示すマーカーや将来的に安全に調節できる標的を見つけることを目指しました。
ビッグデータを掘って危険な遺伝子を探す
まず研究チームは、喫煙者の肺サンプル(COPDあり・なし)の公的に利用可能な遺伝子発現データを収集しました。酸化ストレスに既に関連付けられている遺伝子に注目し、それらがCOPD肺で上方または下方に変動しているかを検討しました。画像認識で用いられるような高度な統計解析や機械学習ツールを用いて、何千もの候補からCOPD患者と対照で差のある76の酸化ストレス関連遺伝子に絞り込みました。さらにその中から、別々のアルゴリズムが合流して疾患肺を健康な肺とよく区別する12の“ハブ”遺伝子のコアセットを特定し、これらの遺伝子がCOPD生物学の重要な分岐点に位置していることを示唆しました。
気道を細胞単位で観察する
従来の組織サンプルは多くの細胞種を混ぜ合わせたものですが、肺は専門化した細胞のモザイクです。ハブ遺伝子がどこで働いているかを見るため、研究者らは単一細胞RNAシークエンシングデータを用いました。これにより、気道を覆う上皮細胞、免疫細胞、血管細胞など主要な肺の細胞型を同定しました。中でもTPPP3とVEGFAの2遺伝子が際立っており、いずれも気道上皮細胞で強く発現し、ROSに関連する経路と密接に結び付いていました。これらの表面細胞は煙や汚染物質に対する最初の防壁を形成するため、発現変化は長期の刺激が持続的な構造変化につながる仕組みを示唆しています。
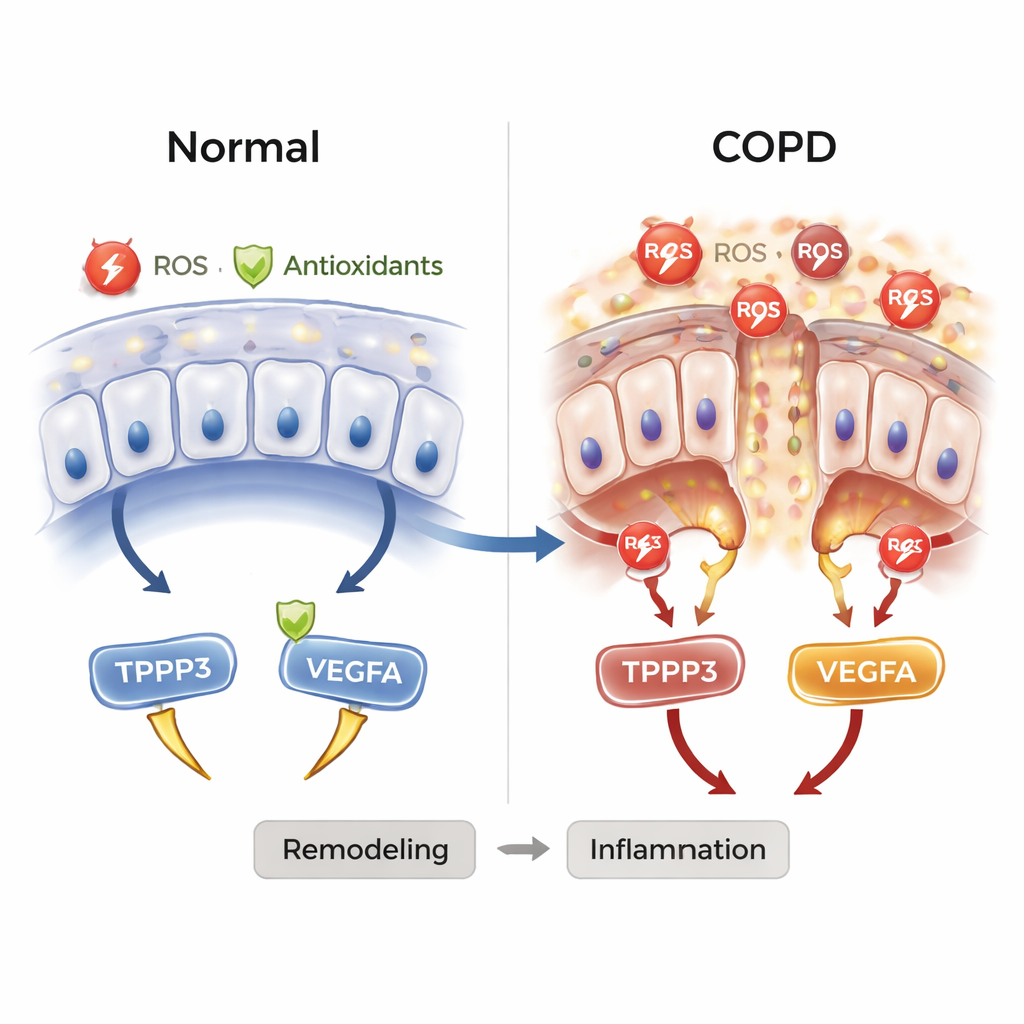
実験室で煙による損傷を再現する
計算予測を検証するため、研究チームはヒト気管支上皮細胞を培養し、タバコ煙抽出物に曝露して喫煙者の気道を模倣しました。顕微鏡下で観察すると、煙処理された細胞ははるかに多くのROSを示し、自然な抗酸化防御が低下していました。COPDに典型的な炎症性分子も増加しました。重要なことに、これらのストレスを受けた細胞ではTPPP3とVEGFAの発現が著しく上昇し、煙による酸化ストレスがこれらの遺伝子を活性化し得ることを裏付けました。この実験モデルは、TPPP3とVEGFAが酸化的損傷と炎症、気道の構造的リモデリングをつなぐ役割を果たしているという考えを支持します。
今後のケアにとっての意味
専門外の方への要点は、本研究が何年にもわたる喫煙や汚染曝露を永続的な呼吸障害に変える分子配線の一端を解き明かしたということです。12の主要な酸化ストレス関連遺伝子、特に気道上皮細胞でのTPPP3とVEGFAに注目することで、将来的にCOPDをより早期に診断したり、患者をより精密なサブタイプに分類したりする血液や組織のバイオマーカーの可能性が示されます。また、これらは将来の薬が気道の肥厚や線維化を遅らせたり防いだりすることを目指す際の新たな分子スイッチの候補でもあります。
引用: Choi, W., Wu, Y., Chen, W. et al. Oxidative stress-associated genes TPPP3 and VEGFA in COPD revealed by bulk and single-cell sequencing analysis. Sci Rep 16, 6801 (2026). https://doi.org/10.1038/s41598-026-37375-4
キーワード: COPD, 酸化ストレス, TPPP3, VEGFA, 気道リモデリング