Clear Sky Science · ja
高強度広帯域テラヘルツ波の非熱効果によって誘導されるヒト上皮細胞におけるDNA二本鎖切断を介した効率的なアポトーシス
がん細胞を殺す新たな光
がん治療はしばしば綱渡りのようで、腫瘍細胞を破壊しつつ健康組織や免疫系を大きく損なわないことが求められます。本研究はそのための一風変わった手段、すなわちマイクロ波と赤外線の間に位置する不可視の光である強力なテラヘルツ(THz)波に注目します。研究者らは、慎重に調整した高強度のTHzパルスが、組織を加熱したり炎症を引き起こすような粗暴な細胞死を伴わずに、がん細胞に制御された「自殺」を促すことを示します。
穏やかな細胞死が重要な理由
多くの一般的ながん治療は細胞を死に導きますが、しばしば副作用を伴います。薬剤や生物学的製剤は腫瘍が耐性を獲得すると効果を失い、免疫系を弱らせることがあります。X線や放射性物質、熱を用いる物理的除去法は周辺の健常組織を傷つけ、壊死—炎症や疼痛を引き起こす激しい細胞死—を生じることが多いです。それに対し、細胞が静かに自己分解する秩序立った過程であるアポトーシスを誘導できれば、特に皮膚近傍の腫瘍を縮小する際に、はるかに低侵襲で苦痛の少ない手段を提供できる可能性があります。
テラヘルツ波と乳がん細胞
研究チームは、実験室でよく用いられる上皮型ヒト乳がん細胞(MCF‑7)を対象にしました。これらの細胞を、体温に保ちながら最大4時間にわたって非常に強い広帯域パルスTHz波に曝しました。電場強度は数百万ボルト毎センチメートルに達し、日常機器より遥かに高い値です。この条件下で、アポトーシスを起こす細胞の割合は曝露時間とともに着実に増加しました。試験した中で最も高いTHz強度では、ほぼ99%のがん細胞がアポトーシスに入り、壊死で死んだ細胞は1%未満でした。この大規模でクリーンなプログラム細胞死の波は、THzパルスが単に細胞を加熱しているだけではないことを示唆します。
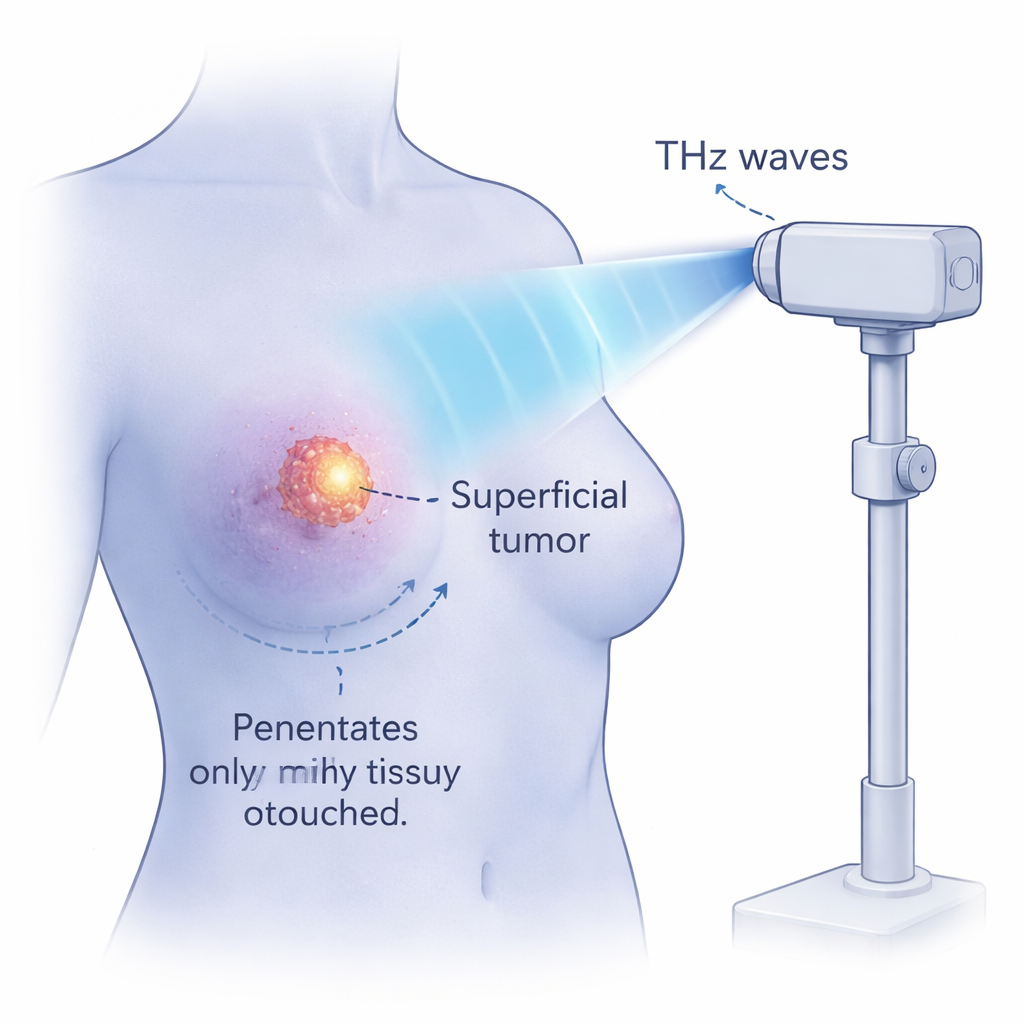
非加熱効果と安全な温度限界
水はTHz放射を強く吸収するため、偶発的な加熱が懸念されます。研究者らは熱画像計測で照射中の温度変化を追跡しました。中程度の強度で4時間照射しても、がん細胞の温度上昇は約3°Cにとどまり、壊死は4%未満でした。細胞を単に数時間加熱する対照実験では、41°C未満ではほとんど死なず、43°Cを超えると壊死が急増しました。最も強いTHz設定でも、研究者らは細胞温度をこの43°Cの閾値以下に保ちながら、ほぼ完全なアポトーシスと最小限の壊死を観察しました。パルスの反復率を下げることで、温度を抑えつつ強い抗腫瘍効果を維持できることを示し、非熱的なメカニズムが働いていることを裏付けています。
DNAを揺らして壊し、死の遺伝子をオンにする
そのメカニズムを探るため、研究チームは細胞内部を調べました。電子顕微鏡では、THz処理された細胞にアポトーシス初期の典型的な兆候が見られました:凝縮した遺伝物質、変形した核、そして外膜は保たれていました。蛍光マーカーγ‑H2AXを用いると、DNAの広範な二本鎖切断が検出され、照射された細胞での損傷は未処理や軽度加熱の対照よりもはるかに多く見られました。損傷のパターンはTHzビームの強度プロファイルに従い、中心部に向かって強くなっていました。遺伝子およびタンパク質解析では、GADD45Bやc‑Junなどのストレス・損傷応答分子群が強く活性化される一方で、p53や多くのカスパーゼなど従来の細胞死経路に関わる既知の因子はほとんど変化しませんでした。著者らは、高強度のTHz場がDNAに激しい振動的“共鳴”を引き起こし、二重らせんを物理的に引き伸ばして切断し、その後p53およびカスパーゼに依存しない独特のアポトーシス経路を誘導している可能性を提案しています。
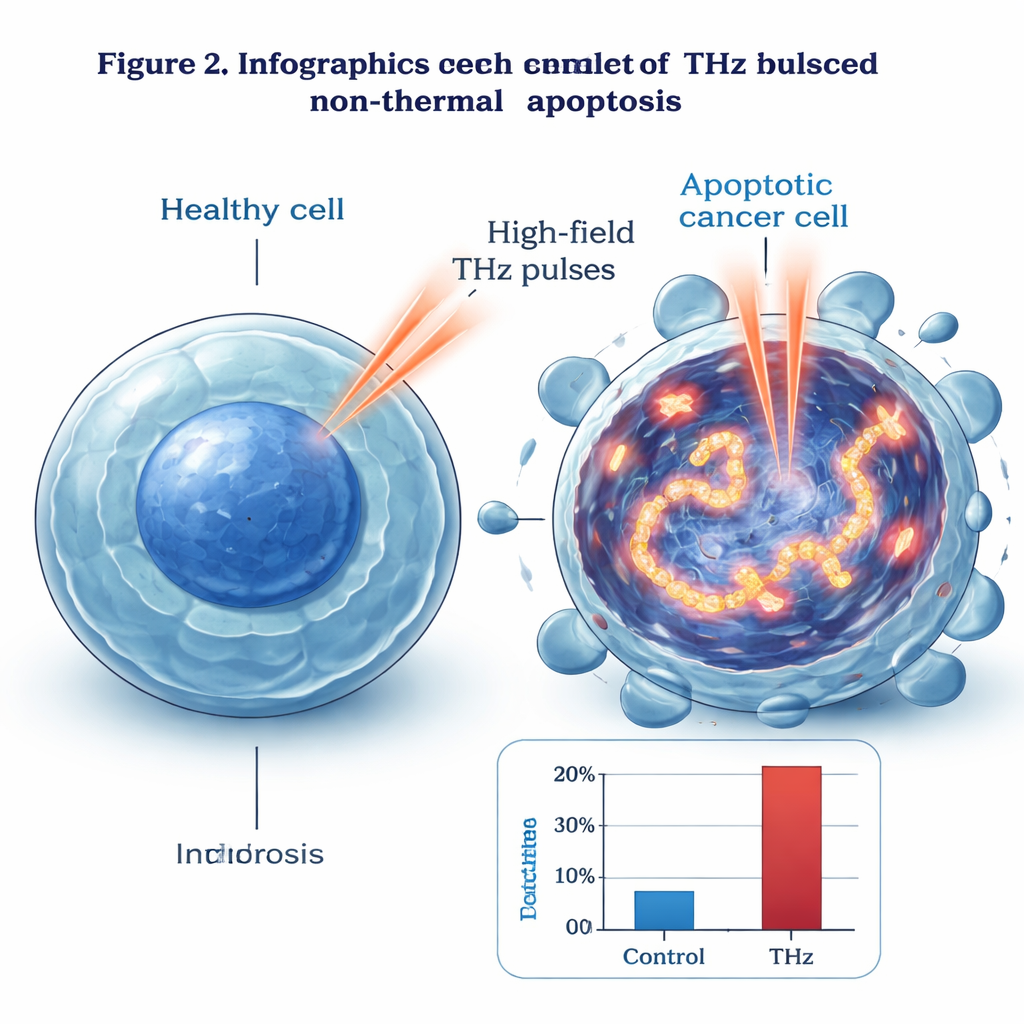
培養皿から将来の治療へ
これらの実験は細胞培養で行われましたが、新しいタイプの物理的がん治療の可能性を示唆しています。高強度のTHz波は湿った組織に数ミリメートル浸透することができ、表在性の腫瘍に届く一方で急速に減衰するため、深部臓器を温存する可能性があります。効果が主に非熱的であるため、周辺組織を焼くことなく層状にがん細胞を除去し、強い炎症を誘発しないことが理論的には期待できます。なお多くの課題が残ります:提案されたDNA“共鳴”機構の検証、正常細胞に対する安全性の徹底的な評価、動物実験や臨床試験の実施が必要です。それでも、この研究は、生体分子の自然な運動に同調するよう精密に調整された光パルスが、将来的に特定のがんを精密かつ比較的穏やかに消失させる手段を提供する可能性があることを示すものです。
引用: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
キーワード: テラヘルツがん治療, 非熱性アポトーシス, DNA二本鎖切断, 乳がん細胞, 物理的腫瘍消失