Clear Sky Science · ja
Akt–EphA2 軸と細胞–細胞接着を標的にすることでがん細胞のアノイキス感受性を高める
なぜ浮遊するがん細胞が重要なのか
がん細胞が腫瘍から離れて血流を介して移動するとき、本来は周囲組織への接着を失うために死ぬべきです。この組み込まれた安全装置は「接着喪失誘導細胞死」と呼ばれ、健康な組織が不適切な場所に増殖するのを防ぎます。しかし転移性がん細胞はしばしばこの信号を無視して浮遊したまま生き残り、新しい腫瘍の種をまきやすくなります。本研究は一見単純な疑問を投げかけます。侵攻的な乳がん細胞に重要な機械的『触覚』を復活させれば、これらの遊走する細胞を死に追いやれるのか、もしできないなら生き残るためにどんな代替手段を用いるのか、ということです。
失われた触覚の再活性化
細胞は周囲の硬さを常に試し、足場となる構造を引っ張っています。健康な組織では、接触を失ったり非常に柔らかい表面に着地したりすると自己破壊が誘導されることが多いです。トロポミオシン2.1(Tpm2.1)というタンパク質はこの内部張力機構の重要な構成要素であり、がん細胞では欠損または低下していることが多いです。研究者らは広く研究されている転移性乳がん細胞株を用い、この細胞にTpm2.1の発現を高めるように改変して剛性感知機能の多くを回復させました。これらの改変細胞を接着できない特殊な非付着皿で増殖させると、修飾されていないがん細胞に比べて細胞死が増え、増殖が遅くなり、運動性も低下しました。それでも、数日間浮遊させてもTpm2.1発現細胞の約70%はまだ生存しており、触覚を復元するだけでは問題が完全に解決しないことを示唆しています。
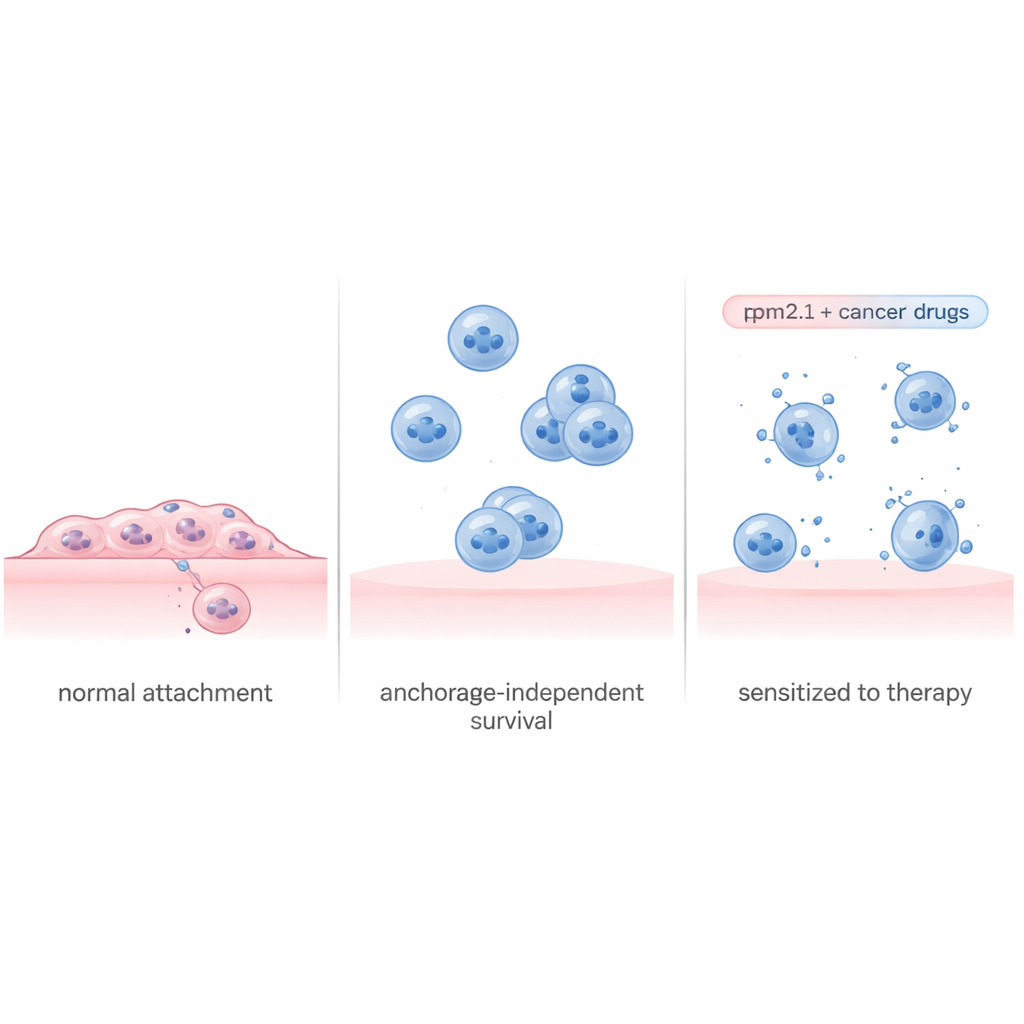
がん細胞の生存プレイブックを読む
なぜ一部の細胞は死に、一部は生き残るのかを理解するために、研究チームは浮遊するTpm2.1発現細胞を初期に死の兆候を示す群と健康に見える群に分けました。そして4日間にわたり各群でどの遺伝子がオン/オフになっているかを測定しました。死に向かう細胞では、細胞分裂、DNA修復、接着に関与するプログラムが広くシャットダウンされ、自己破壊へと向かう一方通行のように見えるストレスシグナルが現れました。対照的に生き残った細胞は協調的な生存プランを活性化していました。接着喪失直後には炎症および免疫関連経路をオンにし、後には成長と生存の主要回路、特にタンパク質Aktを中心としたよく知られた経路を増強しました。同時に、細胞同士が互いにくっつくのを助ける遺伝子を強力に増やし、基質に接着していなくても保護的なクラスターを形成できるようにしていました。
数の力:細胞クラスターが死を抵抗する仕組み
遺伝子データが細胞–細胞接着の増加を示していたため、研究者らは単純な密集が浮遊中の細胞生存を助けるかどうかを検証しました。Tpm2.1発現細胞を高密度で培養してクラスター形成が容易な状態にすると、希薄状態に比べてはるかに少ない細胞が死にました。生き残る細胞で特に高発現していた接着分子ICAM1が際立ち、これは循環腫瘍細胞のクラスター形成と遠隔組織への定着を助けることが既に知られています。ICAM1を小分子阻害剤でブロックすると、Tpm2.1発現細胞の浮遊中の死が増え、標準的な付着培養にはほとんど影響がありませんでした。これらの発見は、内部の力学が部分的に回復した後でも、がん細胞が周囲に掴まる代わりに互いにしがみつくことで死を回避できる、という考えを支持します。
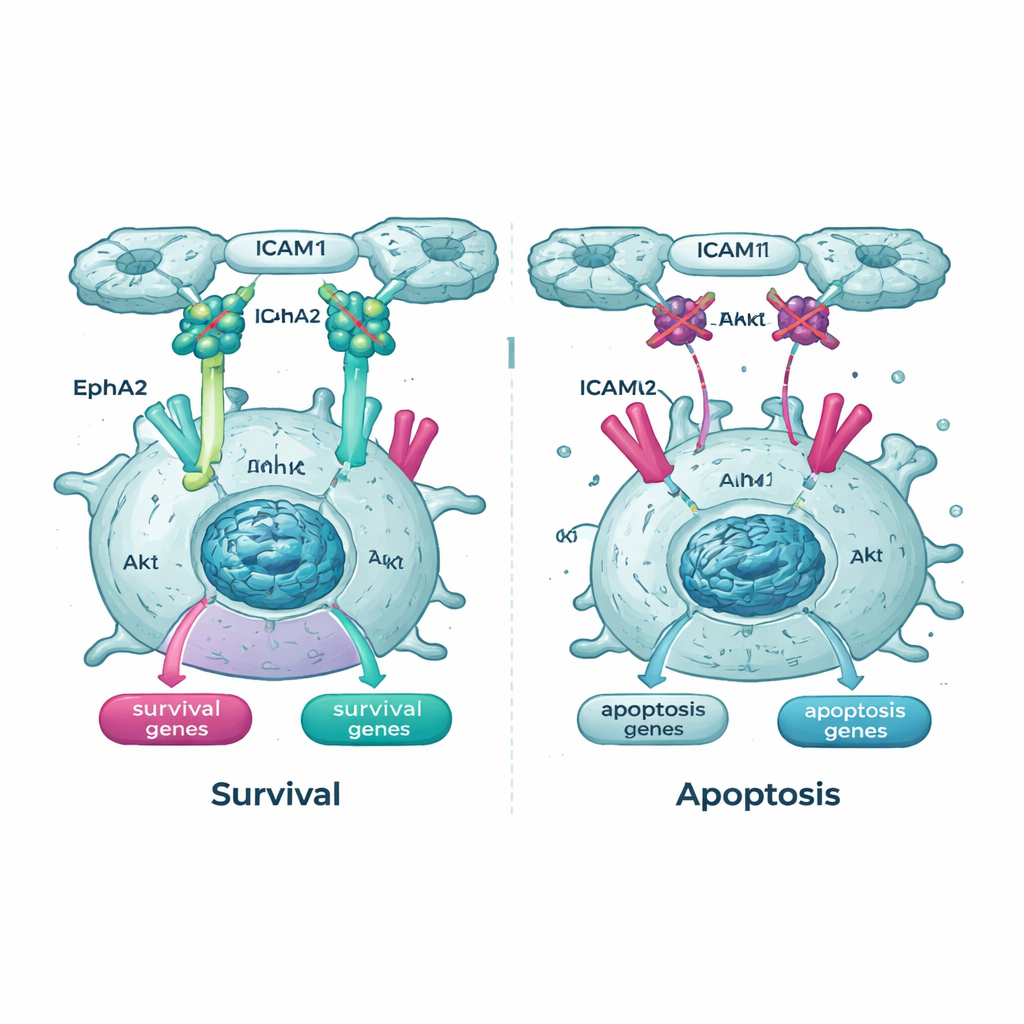
細胞内部の重要な生命線を断つ
遺伝子解析はまた、Akt 経路とそのパートナーの一つである受容体EphA2を浮遊するがん細胞の重要な生命線として浮かび上がらせました。Tpm2.1発現細胞では、浮遊状態での活性化されたリン酸化型Aktが対照細胞より低く、EphA2の量と活性も低下していました。研究チームがAktまたはEphA2を阻害する薬剤で処理すると、通常のがん細胞もTpm2.1発現がん細胞も、浮遊中に死にやすくなりました。特に剛性感知が回復した細胞は時間経過でこれらの薬剤に対して感受性が高く、機械的な安全装置が部分的に再稼働すると残された生存シグナルへの依存度が高まることを示唆しています。
準備状態を致命的な弱点に変える
専門外の方への要点は、がん細胞の壊れた安全スイッチの一つ――接触を失ったことを感知して応答する能力――を修復することは必要だがそれだけでは自己破壊を完全に引き起こすには不十分だということです。生き残る細胞は、互いに固まって代替の成長・生存経路へ内部配線を切り替えることで生き延びます。本研究は、Tpm2.1 によって剛性感知を回復させると転移性乳がん細胞が『準備された(プライム)状態』になり、死に近づくがまだ不可逆的ではない状態になることを示しています。その状態でAkt–EphA2経路を遮断し、ICAM1を介した細胞–細胞接着を妨げることで、これらの準備された細胞を死へと押し込み、接着喪失誘導細胞死を大幅に増強できます。実用的には、この研究は遊走する腫瘍細胞が新たな転移を播く前に根絶することを目指した将来の併用療法戦略の道筋を示しています。
引用: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
キーワード: 乳がんの転移, 細胞接着, アノイキス, Akt シグナル伝達, 剛性感知