Clear Sky Science · ja
ゲノム規模のスクリーニングにより細胞表面プリオンタンパク質発現の中核調節因子を同定
脳の健康にとってなぜ重要か
クレutzフェルト=ヤコブ病(人)や牛海綿状脳症(いわゆる「狂牛病」)のようなプリオン病は稀ですが常に致命的な脳疾患です。中心的な原因はプリオンタンパク質と呼ばれる通常の脳内タンパク質の誤った折りたたみであり、これが細胞間に広がって損傷をもたらします。神経細胞の表面にこのタンパク質が多く存在するほど、病気が成立しやすくなります。本研究は、ニューロン様細胞の外側に現れるプリオンタンパク質の量を制御する遺伝子をゲノム全体でマッピングすることを目的としました。そのマップは研究者がこのタンパク質を減らす新しい方法を設計し、複数の神経変性疾患の進行を遅らせる手がかりになる可能性があります。
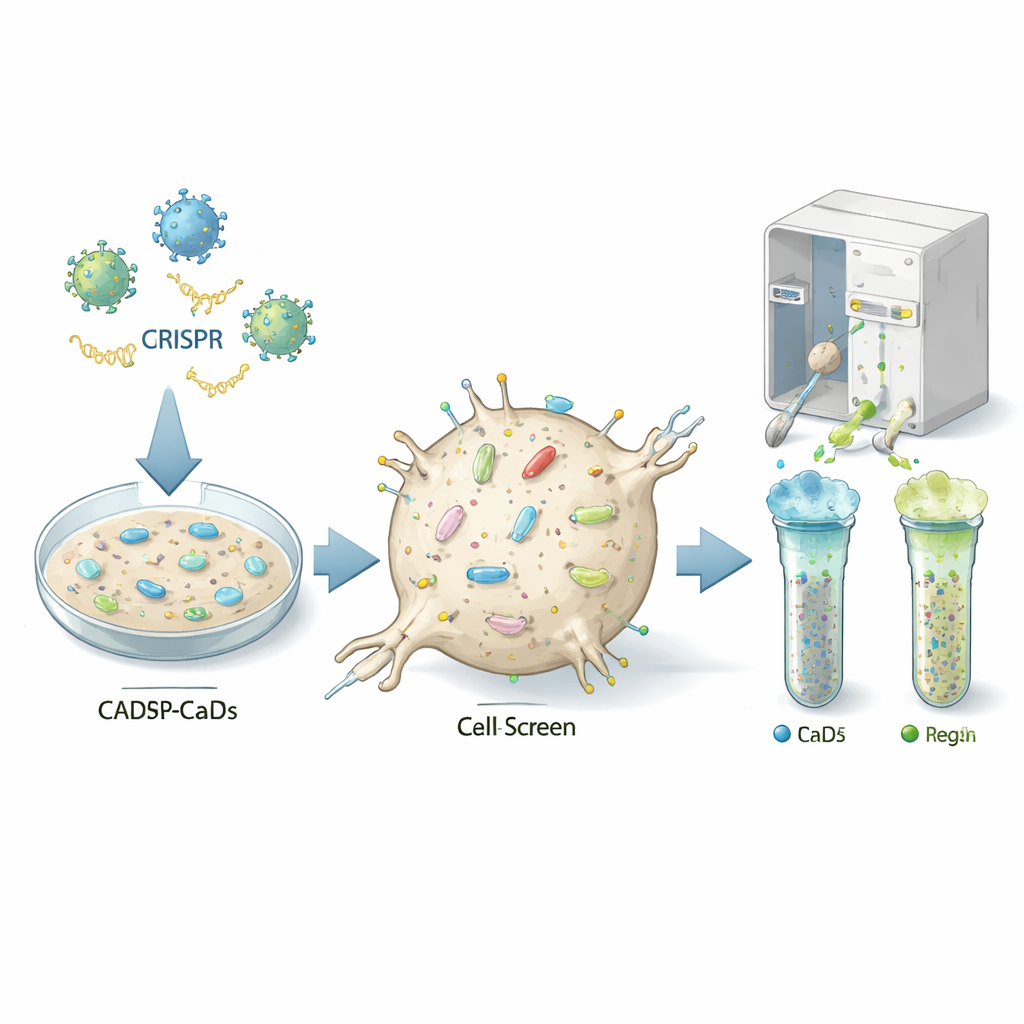
細胞の調節ノブを見つける
著者らはCRISPRと呼ばれる強力な遺伝子編集手法を用いて、プリオンに感染可能なマウス由来のニューロン様細胞株(CAD5細胞)でほぼすべての遺伝子を個別にノックアウトしました。各細胞は異なる遺伝的“打撃”を受け、結果として特定の遺伝子を欠く何百万もの変異体が含まれる集団が得られました。チームは細胞表面の正常なプリオンタンパク質を認識する蛍光標識抗体で細胞を染色し、セルソーターでこのタンパク質が異常に低い群と高い群の細胞を分離しました。低群または高群で濃縮されたガイドRNAをシーケンスすることで、どのノックアウト遺伝子が通常、細胞表面のプリオンタンパク質のオン/オフスイッチとして働くかを推測できました。
二つの細胞状態、重なる解答
ニューロンは一生の間に見た目や振る舞いが一様ではないため、同じ遺伝子が異なる細胞状態でプリオンタンパク質を制御するかどうかを研究者らは検討しました。CAD5細胞は増殖の速い未分化の状態に維持できる一方で、培地から血清を除くとより成熟したニューロン様の形をとります。チームは両方の条件で同じゲノム全体のCRISPRスクリーニングを実施しました。未分化(やや未成熟)細胞では、表面プリオンタンパク質を増やす遺伝子46個と減らす遺伝子21個を検証しました。分化(よりニューロン様)細胞では、正の調節因子41個と負の調節因子13個を確認しました。そのうち23個の遺伝子は両方の細胞状態で共通しており、主にタンパク質に脂質の“アンカー”を付ける働きをする遺伝子群で、成熟度に関わらず動作する中核的な調節機構を浮き彫りにしました。
最も重要な組み立てライン
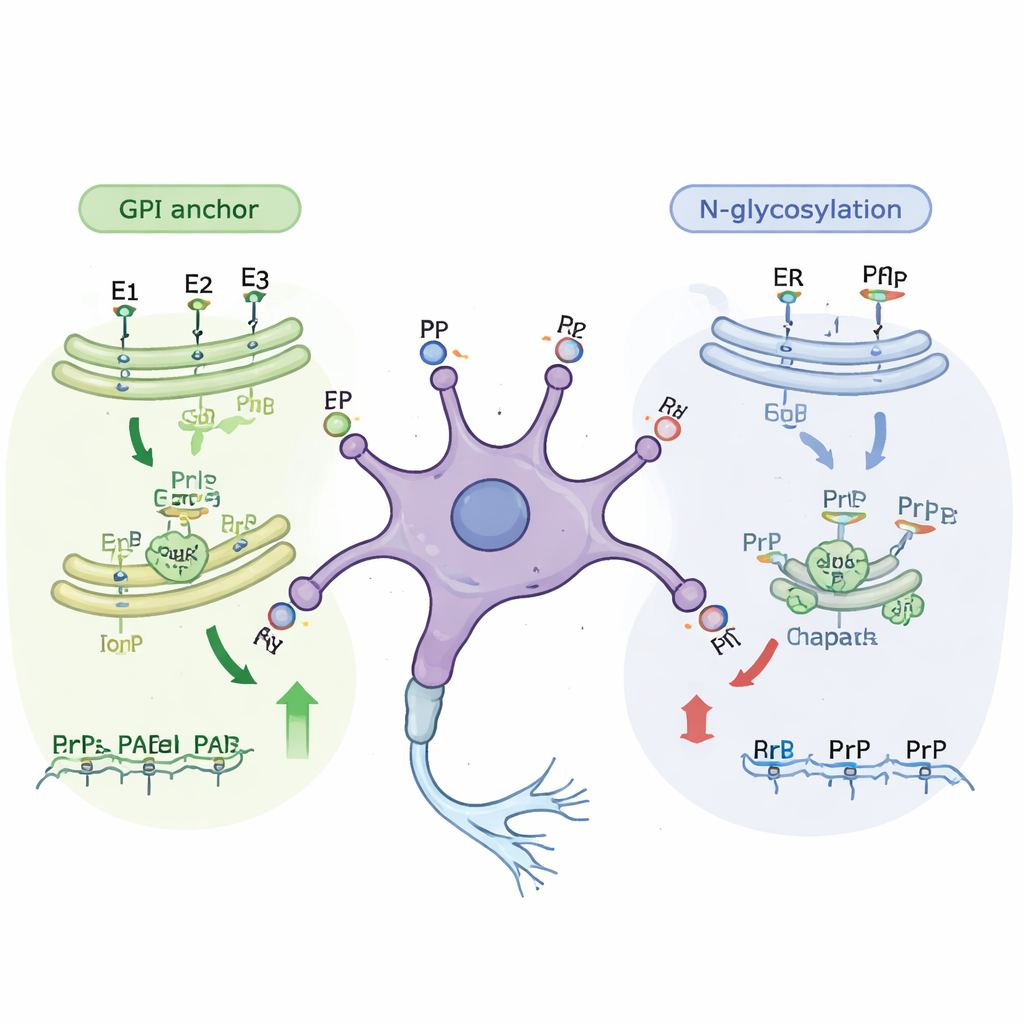
さらに解析すると、新たに同定された多くの遺伝子が、タンパク質が細胞表面へ運ばれる際に修飾を行う既知の“組み立てライン”に属することがわかりました。主要な経路の一つはGPIアンカーを構築するもので、これは脂質に富む小さな構造でプリオンタンパク質を細胞膜の外側に固定します。この経路のほぼ任意の段階を妨げると、未成熟および成熟細胞の双方でプリオンタンパク質が表面に達する量が減少しました。第二の経路はN結合型糖鎖付加(N-グリコシル化)で、タンパク質が細胞内膜を通過する際に複雑な糖鎖が付加されます。この糖鎖付加経路の遺伝子は主に未成熟細胞で重要として浮上しました。研究者らが特定の糖鎖付加ステップを阻害する小分子を細胞に処理すると、細胞死を引き起こすことなく表面プリオンタンパク質が約3分の1減少し、遺伝学的発見を裏付けました。
補助タンパク質とストレス応答
スクリーニングはまた、他のタンパク質の正しい折りたたみを助ける分子シャペロンが重要なプリオン調節因子であることを示しました。特にHspa5(BiPとも呼ばれる)は細胞のタンパク質折りたたみ区画で中心的なシャペロンとして、よりニューロン様の細胞で正の調節因子として浮上しました。研究者らがHspa5を阻害する薬剤を用いると、細胞状態にかかわらず表面プリオンタンパク質のレベルが低下し、明らかな細胞障害は見られませんでした。他のヒットには、タンパク質輸送に関与する遺伝子、遺伝子発現のオン/オフを制御する因子、シナプス機能やアルツハイマー病・ALSなど他の脳疾患と関連する複数のタンパク質が含まれていました。これらの結果は、細胞表面のプリオンタンパク質レベルが、タンパク質の産生、修飾、輸送、品質管理にまたがる複雑な経路網によって形づくられていることを示しています。
今後の治療にとっての意味
本研究は、プリオン感染に感受性のあるニューロン様細胞の表面に現れるプリオンタンパク質の量を制御する遺伝子の最初の包括的なカタログを提供します。特にGPIアンカー経路、N-グリコシル化経路、Hspa5シャペロン系に属する遺伝子は薬剤探索の有望な出発点として浮かび上がります。これらの活性を低下させれば、誤折りたたみの起点となるプリオンタンパク質の量を減らせるはずで、過去の研究では部分的な減少でも動物における疾患の進行を有意に遅らせることが示されています。一方で、未成熟細胞と成熟細胞の間に明確な差があることは、標的選定の際に脳細胞の状態が重要であることを強調します。これらの遺伝子を操作して実際の脳内でのプリオン感染や他の神経変性疾患にどう影響するかを検証するにはさらに研究が必要ですが、本研究は研究者がこれらの破滅的な疾患を遅らせたり予防したりするために探ることができる細胞レバーのロードマップを提供します。
引用: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
キーワード: プリオンタンパク質, CRISPRスクリーニング, 神経変性, タンパク質の糖鎖付加, GPIアンカー