Clear Sky Science · ja
機械学習による腫瘍浸潤リンパ球の自動定量化が明らかにした肺がんにおける予後および免疫ゲノム学的特徴
なぜ肺腫瘍内の小さな免疫細胞を数えることが重要なのか
肺がんは依然として致死率の高いがんの一つですが、すべての腫瘍が同じ振る舞いをするわけではありません。ある腫瘍はリンパ球などの免疫細胞が内部に多く入り込んで監視されている一方で、ほとんど手つかずのものもあります。これらの腫瘍浸潤リンパ球(TIL)は、患者の予後や現代の免疫療法が有効かどうかの手がかりを与えることがあります。問題は、現在TILは通常顕微鏡で目視カウントされており、時間がかかり主観が入りやすい点です。本研究は時宜を得た問いを投げかけます:日常的な病理スライド上で機械学習を用いてこれらの細胞を自動的に測定できるか、そしてそれが肺がんの生物学や患者生存に関して何を示すか?
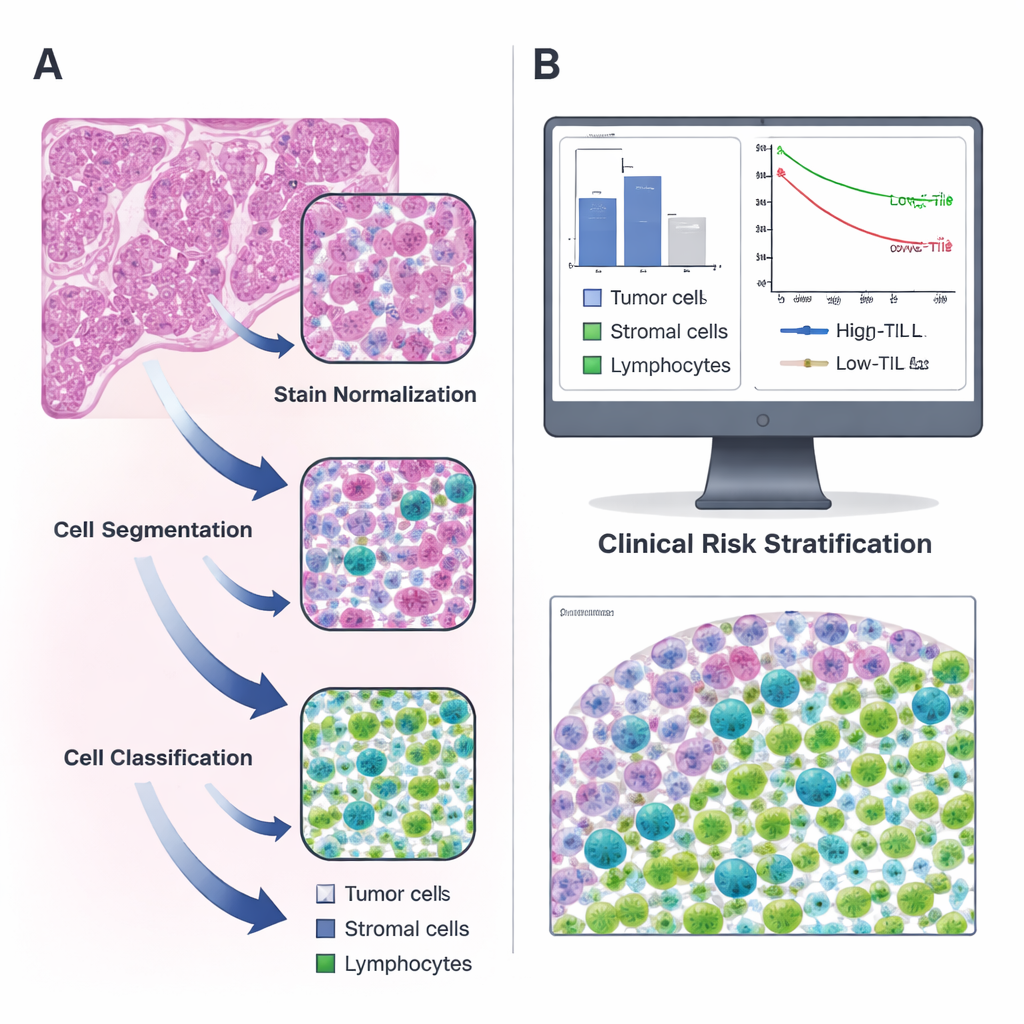
通常のスライドをデジタル地図に変える
研究者らは一般的な肺がんの一型である肺腺がんに着目し、The Cancer Genome Atlas の公開データと自施設の独立コホートを用いました。各患者について、病理医がよく目にするピンクと紫のH&E(ヘマトキシリン・エオシン)染色スライドを解析しました。オープンソースのQuPathソフトウェアを使い、段階的なパイプラインを構築しました:まずスライド間の色差を補正し、次にウォーターシェッドアルゴリズムで重なった核を分離し、最後に学習済みの分類器が検出した各細胞を腫瘍細胞、支持組織(ストローマ)、またはリンパ球としてラベル付けしました。2名の専門病理医が機械の出力を繰り返し確認・修正し、機械が自律的に各細胞型を信頼して認識できるようにしました。
免疫細胞数と患者アウトカムの結びつき
システムが細胞を確実に識別できるようになると、チームは300例以上の患者について腫瘍組織1平方ミリメートルあたりに存在するリンパ球数を算出しました。TILのレベルは大きくばらついており、平均的には全細胞のごく一部にすぎませんでした。情報量の多いカットオフを統計的に探索した結果、1平方ミリメートルあたり135個のTILを「高TIL」と「低TIL」を分ける境界として選びました。この閾値を超える腫瘍を持つ患者の生存は、免疫細胞浸潤が乏しい患者より長く、こうした傾向は元のコホートと検証コホートの両方で一貫していました。言い換えれば、自動化ツールで得られた単純な数値が生存の有意な違いを捉えており、従来の手作業によるより手間のかかる研究と整合していました。
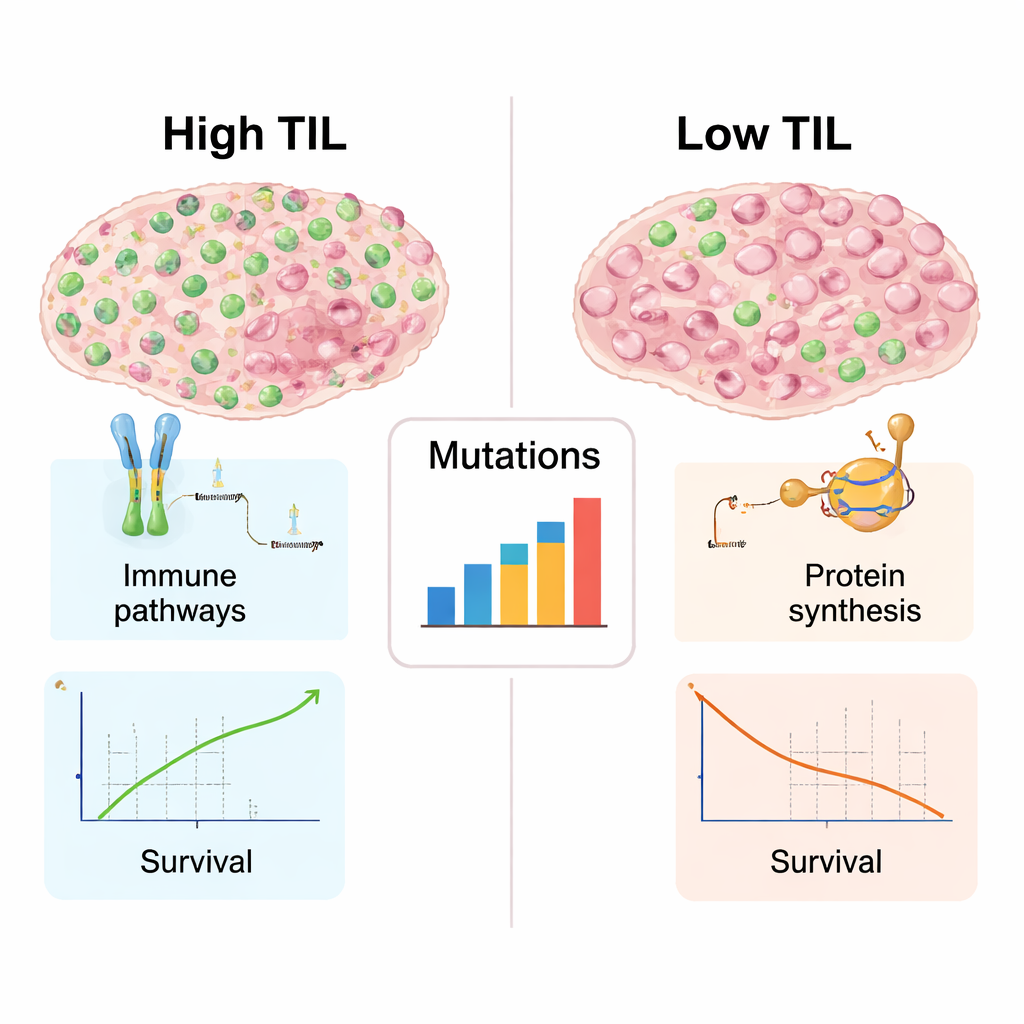
免疫豊富な腫瘍の内部像
多くの腫瘍で遺伝学的・分子データが利用可能だったため、著者らは単なる細胞数以外に高TIL腫瘍と低TIL腫瘍を区別する特徴を調べることができました。リンパ球であふれる腫瘍は免疫活性のシグネチャーが強く、異常なタンパク質の認識やそれらをT細胞へ提示する機構、免疫攻撃の調整に関与する遺伝子群の発現が高まっていました。これらの腫瘍はまた、より多様なDNA変異を伴い、免疫系にとって新たな標的を生む可能性がありました。一方、低TIL腫瘍はリボソーム構成やタンパク質合成に関連する遺伝子の優位を示し、増殖のための機械は活発でも免疫関与は比較的静かな様相を呈していました。この差は、免疫細胞に富み免疫療法に反応しやすい「ホット」腫瘍と、免疫系にほとんど無視される「コールド」腫瘍という対比と一致します。
免疫状態を予測するようコンピュータを教育する
チームはさらに一歩進み、細かいイメージ特徴のコンパクトなセットで、すべてのリンパ球を個別に数えなくても腫瘍が高TILに属するか低TILに属するかを予測できるかを検討しました。スライド中の微妙なテクスチャーパターン——小領域でのピクセル強度の変化——をHaralick特徴量として要約し、腫瘍の臨床ステージと組み合わせてランダムフォレストモデルに投入しました。交差検証では、この分類器は高TILと低TILの腫瘍を高い精度で区別し、独立した病院コホートでも妥当な性能を維持しました。重要なのは、この手法全体が標準的なコンピュータと無償のソフトウェアで動作するため、多くの病理検査室が特殊なハードウェアなしに導入可能であることを示唆している点です。
今後の肺がん医療への示唆
専門外の読者にとっての要点は、コンピュータが日常的な肺がんスライドを読み取り、免疫系が腫瘍にどれほど関与しているかを捉えられるようになるということです。高い浸潤リンパ球レベルはより活発な免疫反応、変異の多様性の豊かな状況、そして総じて良好な生存と結びつきます。さらなる研究、特に免疫療法を実際に受けた患者での検証が必要ですが、この自動化手法は将来的に腫瘍を迅速かつ一貫して免疫の「ホット/コールド」に分類するのに役立つ可能性があります。それは誰が免疫療法で最も恩恵を受けるかの判断を導き、コールド腫瘍をホットに変える新しい戦略の開発を促すかもしれません。
引用: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
キーワード: 肺腺がん, 腫瘍浸潤リンパ球, 機械学習, デジタル病理学, がん免疫療法