Clear Sky Science · ja
CKAAKN ペプチド結合長循環ナノリポソームによる膵臓がんへのオリドニン標的送達
この研究が重要な理由
膵臓がんは発見が遅れがちで標準的な化学療法に抵抗しやすいため、最も致命的ながんの一つです。本研究は、植物由来の抗がん化合物オリドニンを、ナノサイズの脂質バブルであるナノリポソームを使って膵臓腫瘍に直接届ける、より賢い手法を探ります。より多くの薬剤を腫瘍に集め、健康な組織への影響を抑えることで、この研究は穏やかでより効果的な治療法への道を示しています。
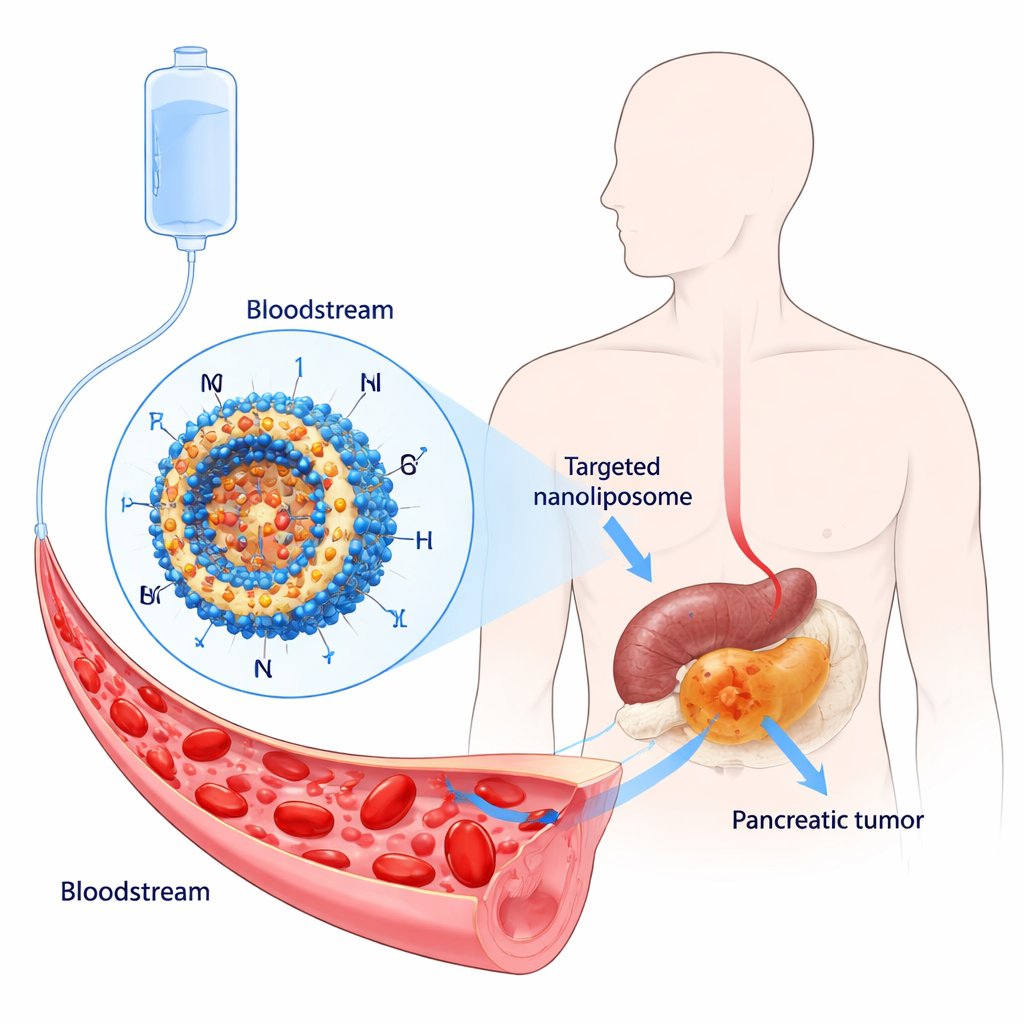
治療が難しい致命的ながん
膵臓がんは生存率がほとんど一桁台にとどまるため、「がんの王」といった不穏なあだ名が付いています。手術適応となる患者はごく一部で、手術後に再発するケースも少なくありません。パクリタキセルやシスプラチンのような化学療法薬は病勢を抑えることがありますが、副作用が強く、腫瘍はしばしば薬剤耐性を獲得します。したがって、より精密で毒性の低い薬剤と、全身に薬を行き渡らせるのではなく腫瘍内に薬を濃縮できる送達システムの探索が続いています。
植物由来分子を現代医薬へ変える
オリドニンは漢方薬用植物Rabdosia rubescens(学名)から抽出される天然化合物です。実験室での研究は、オリドニンが細胞分裂を阻害しアポトーシスを誘導することで、膵臓を含むさまざまながん細胞の増殖を抑えることを示しています。しかし、オリドニン単体は薬として扱いにくく、水に溶けにくく吸収性が低く、用量が高くなると毒性を示すことがあります。その潜在力を活かすため、著者らはオリドニンをナノリポソームに封入し、細胞膜に似た脂質でできた小球体に入れて血流を安全に移動し、腫瘍部位でゆっくり放出するよう設計しました。
薬のための“ステルス”ホーミングパッケージの設計
研究チームは二層構造の送達システムを構築しました。まず、ポリエチレングリコール(PEG)で表面をコーティングした長時間循環型リポソームを作製しました。PEGは親水性の高分子で、免疫細胞の回避を助け血中滞留時間を延ばします。次に短いペプチドCKAAKNを付加し、膵臓がんに対するホーミングタグとしました。このペプチドは多くの膵臓腫瘍で異常に活性化しているWntシグナル経路の一部を模倣し、改変したリポソーム(ORI@CPD-Lipoと呼ばれる)が対応する受容体を示すがん細胞に付着できるようにします。最終的な粒子は直径約100ナノメートルで、オリドニンを高含有量で搭載し、薬剤を数時間にわたってゆっくりと放出しました。
標的化粒子の細胞内および動物での振る舞い
細胞培養試験では、CKAAKNタグ付きリポソームは正常膵臓細胞よりもヒト膵臓がん細胞に対してはるかに効率よく取り込まれ、とくに接触後最初の数時間で顕著でした。遊離のCKAAKNペプチドを過剰に加えるとがん細胞の取り込みが減少し、特異的結合が関与することを示唆しました。空のリポソームは毒性が低く、赤血球を損なわなかったため安全性の観点でも良好でした。オリドニンを搭載した標的リポソームは、遊離オリドニンや非標的リポソームよりもがん細胞をより効果的に死滅させ、培養皿上の傷創を横切るがん細胞の移動をより強く抑制しました。膵臓腫瘍を持つマウスでは、蛍光標識した標的リポソームが腫瘍に最大48時間蓄積し、非標的リポソームよりも腫瘍への集積が高い一方で、肝臓や脾臓を介して排除される経路は予想通り残っていました。
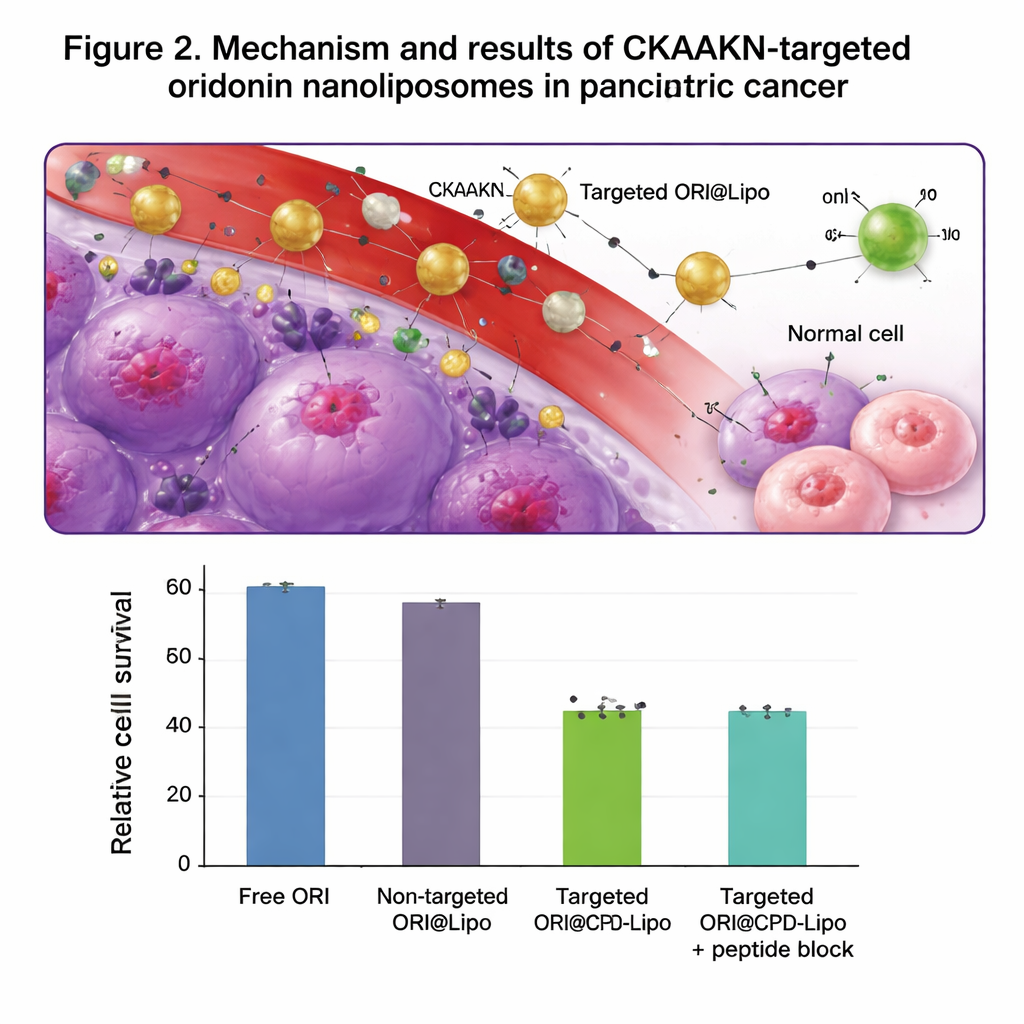
将来の治療への示唆
総じて、伝統的な植物由来化合物を現代の精密な送達手段と組み合わせることで、実験モデルにおける抗腫瘍効果を大幅に高められることが示されました。CKAAKNで修飾した長循環ナノリポソームは、正常組織への暴露を限定しつつ膵臓がん細胞へより多くのオリドニンを運び、がん細胞死を促進し転移につながり得る細胞移動を抑えます。これらの結果はまだ前臨床段階であり、著者らも十分な動物治療試験や臨床試験が必要であると注記していますが、本研究は膵臓がんに対する標的ナノ医薬の基盤をしっかりと築き、他の有望な天然分子を腫瘍指向性の薬に転換する一般的な戦略を示唆しています。
引用: Zhang, F., Luo, K., Xuan, S. et al. CKAAKN peptide-conjugated long-circulating nanoliposomes for the targeted delivery of oridonin to pancreatic cancers. Sci Rep 16, 6065 (2026). https://doi.org/10.1038/s41598-026-36920-5
キーワード: 膵臓がん, ナノリポソーム, 標的薬物送達, オリドニン, 腫瘍ホーミングペプチド