Clear Sky Science · ja
YTHDC1はSQSTM1を介したオートファジーを通じて網膜芽細胞腫の悪性形質を調節する
小児の眼のがんにとってなぜ重要か
網膜芽細胞腫は幼児に最も多く見られる眼のがんです。早期に発見されれば治癒できることが多い一方で、腫瘍が眼の周囲組織へ浸潤したり脳に向かって広がり始めると、命と視力の両方を守ることが格段に難しくなります。本研究は、腫瘍細胞内部に存在する分子的な“ブレーキ”――YTHDC1とSQSTM1という二つの分子――に注目しています。これらは網膜芽細胞腫の攻撃性を抑える働きをしているように見えます。どのようにこのブレーキが機能するかを理解することで、より穏やかで標的を絞った治療法につながる可能性があります。
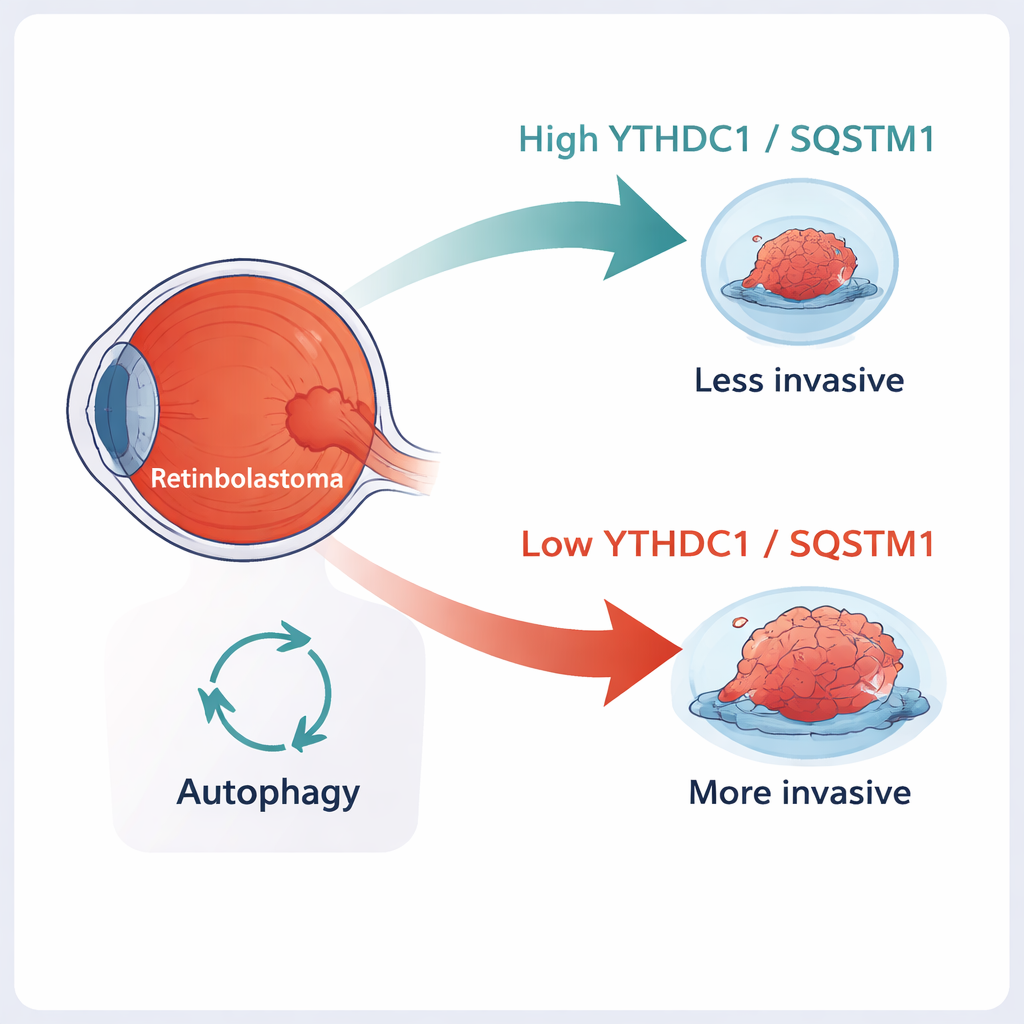
小児の眼腫瘍を詳しく見る
網膜芽細胞腫は、通常5歳未満の子どもの光を感知する網膜層から発生します。古典的には、保護役の遺伝子であるRB1の両方のコピーが失われることで発症します。しかし、RB1の喪失だけでは、なぜ一部の腫瘍は眼内にとどまり、他は周辺組織に侵入したり視神経に沿って広がるのかを完全には説明できません。近年、RNAに付けられる化学的な目印(タグ)が、これらのメッセージの安定性や持続時間を変え、がんの振る舞いに強い影響を与えることが明らかになってきました。最も一般的なタグの一つであるm6Aは、こうしたRNAメッセージの安定性を変化させます。
欠けていた分子的ブレーキの発見
著者らはまず、眼内にとどまった腫瘍と既に浸潤性を示す腫瘍の遺伝子発現を比較しました。公開されている網膜芽細胞腫のRNAシーケンスデータセットを用いて、両群で発現が異なる数千の遺伝子を同定し、そこからm6Aの「調節因子」に注目しました。これにはm6Aを付加・除去する酵素や、そのタグを読み取る「リーダー」タンパク質が含まれます。主要な10種類の調節因子の中で、リーダーの一つであるYTHDC1が浸潤性腫瘍で一貫して低くなっていることが分かりました。50人の小児の検体と実験室での組織解析でも、YTHDC1のRNAとタンパク質の両方のレベルがより攻撃的ながんで低下していることが確認されました。
YTHDC1の機能を検証する
YTHDC1が実際に何をしているかを確かめるため、研究チームは二つのヒト網膜芽細胞腫細胞株でその量を操作しました。遺伝学的手法でYTHDC1を減らすと、細胞の増殖が速まり、組織の障壁を模した人工膜をよりよく通過するようになり、浸潤性の指標が増加しました。マウスモデルでも、YTHDC1を欠く細胞はより大きく重い腫瘍を形成しました。逆に、YTHDC1を過剰に発現させると増殖が遅くなり、移動や浸潤能が低下しました。これらの実験は、YTHDC1が腫瘍抑制因子として機能し、網膜芽細胞腫の危険な振る舞いを抑えていることを示唆します。
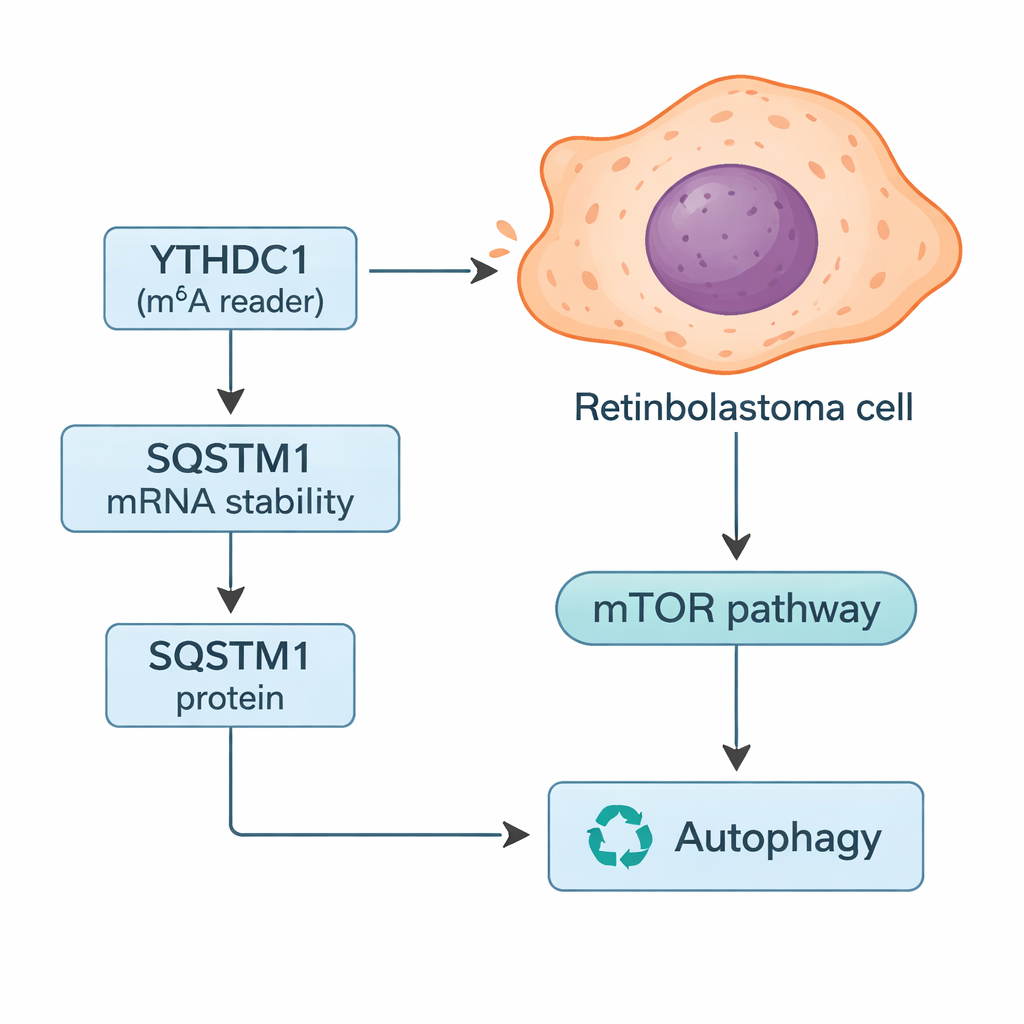
YTHDC1は細胞のリサイクル機構をどう制御するか
さらに詳しく調べるため、研究者らはYTHDC1によって制御されうる特定の遺伝子のメッセージを探索しました。データベース検索と腫瘍データの組み合わせから、p62として知られるSQSTM1に注目しました。SQSTM1は、損傷した構成要素を分解し、資源が乏しいときに燃料を供給するなど、オートファジー(細胞のリサイクル)を管理する役割を持ちます。本研究は、YTHDC1がSQSTM1のRNAに物理的に結合してそれを安定化させ、より多くのSQSTM1タンパク質が作られるようにしていることを示しました。YTHDC1が減少するとSQSTM1のレベルは下がり、そのRNAはより速く分解されました。SQSTM1を単独でサイレンシングすると網膜芽細胞腫細胞の増殖と浸潤が増し、YTHDC1過剰発現による保護効果の一部が消失したため、SQSTM1がこの経路の重要な仲介役であることが示されました。
オートファジー、エネルギー、そして腫瘍の攻撃性
SQSTM1がオートファジーの中心にあることから、研究チームはYTHDC1とSQSTM1の変化がこのリサイクル過程にどう影響するかを検討しました。蛍光マーカーとタンパク質測定を組み合わせた実験で、YTHDC1またはSQSTM1を減らすとオートファジーの「フラックス」が亢進し、より多くの細胞材料がリサイクル系に運ばれて処理されることが分かりました。また、オートファジーを通常抑制している主要な栄養感知スイッチであるmTOR経路の変化も観察されました。SQSTM1が少ないとmTORの活性が低下し、これはオートファジーが亢進する状況と一致します。著者らは、浸潤性の網膜芽細胞腫ではYTHDC1の低下がSQSTM1信号を弱め、mTOR活性を減少させ、オートファジーを高めることで腫瘍細胞がストレスに耐え広がるのを助けていると提案しています。
将来の治療にとっての意味
専門外の読者に向けた要点は、本研究が網膜芽細胞腫細胞内の連鎖反応――YTHDC1がSQSTM1を制御し、それが細胞のリサイクル機構を形づくる――を示し、この連鎖が腫瘍の攻撃性に影響を与えることを明らかにした点です。この連鎖が弱まると腫瘍はより速く成長し浸潤しやすくなります。臨床応用にはまだ多くの作業が必要ですが、この経路は治療の新たな着想を提供します:YTHDC1機能の回復、SQSTM1の安定化、あるいはオートファジーやmTOR活性の微調整は、いずれ既存の化学療法を補完する可能性があります。こうした標的治療は、子どもたちの腫瘍の広がりを抑えつつ視力をより多く温存し、治療の副作用を減らす助けになるかもしれません。
引用: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
キーワード: 網膜芽細胞腫, YTHDC1, SQSTM1, オートファジー, mTOR経路