Clear Sky Science · ja
最適化された放出プロファイルを持つデキサメタゾン含有人工蝸牛インプラント電極キャリアの長期in vivo薬物動態
高機能な聴覚インプラントをより耳にやさしくする
人工内耳は重度の難聴者に聴力を取り戻すことができますが、繊細な内耳に微細な電極を挿入する行為は依然として損傷と炎症を引き起こします。その初期の損傷が残存する自然聴力を失わせ、時間とともにインプラントの性能を低下させる可能性があります。本研究は、薬剤を放出するダミー電極(実際のインプラント配列の代用)をより賢く設計し、ステロイド薬を内耳にゆっくり放出して炎症を局所で抑えつつ、薬剤の総量をできるだけ少なくする方法を検討します。
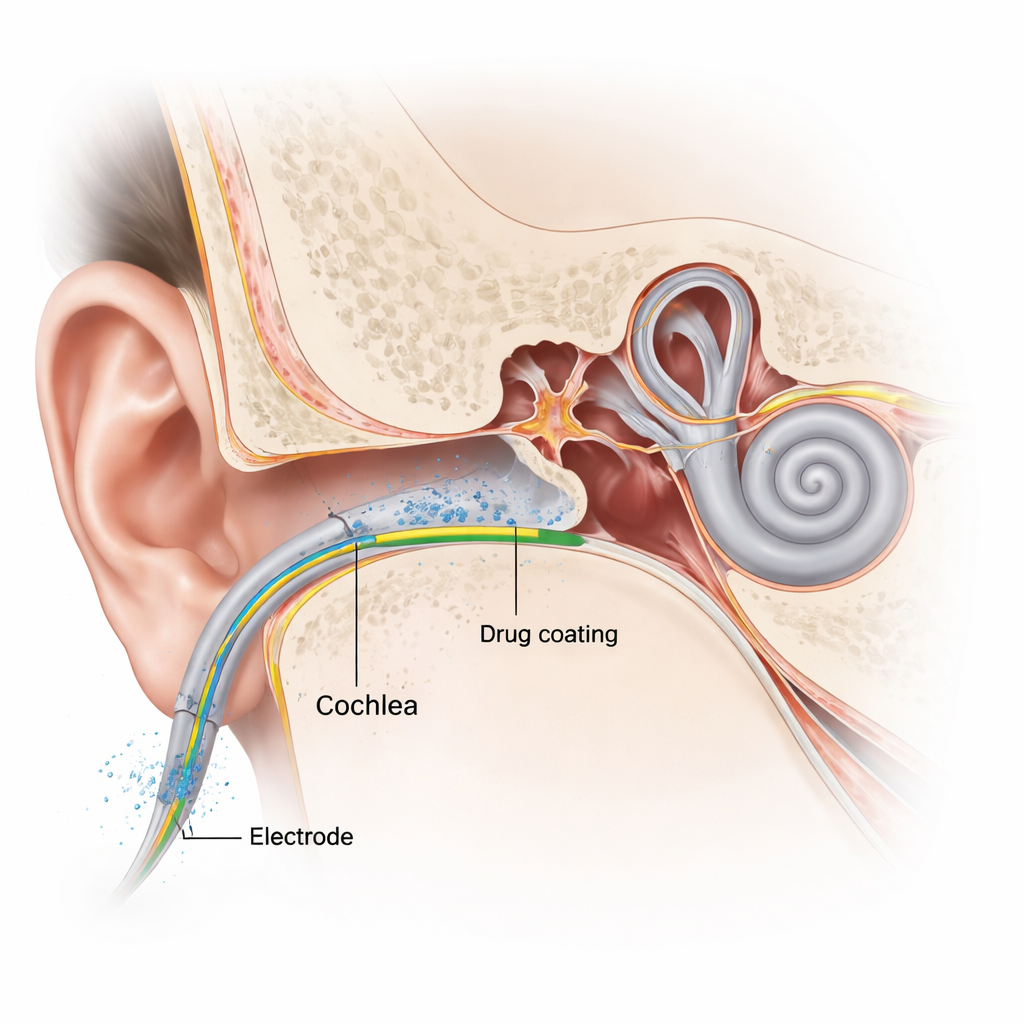
なぜ人工内耳が依然として聴力に害を与えるのか
人工内耳は改良が進んでいるものの、らせん状の蝸牛に電極を挿入する手技は侵襲的です。電極の機械的な押し込みにより、音を感知する有毛細胞や神経構造が損傷を受け、炎症反応が引き起こされます。術後数日から数週間で、体はインプラントを異物として認識し、その周囲に線維性組織を形成します。この瘢痕様組織は電極の電気抵抗を上げ、より強い電流を必要とし、音高(ピッチ)情報の精度を低下させます。長期的には、この過程が残存する自然聴力を侵食し、インプラントの恩恵を制限する可能性があります。
よく知られた薬をより賢く使う
内耳を保護する有望な方法の一つは、損傷部位に直接抗炎症薬を届けることです。ステロイドのデキサメタゾンは脆弱な細胞を保護し腫れを軽減するために内耳疾患の治療で既に用いられています。しかし、全身投与や中耳投与では薬剤が内耳液から速やかに洗い流され、有効濃度を長く維持するのが難しいです。以前の研究では、シリコーンロッド全体にデキサメタゾンを均一に混ぜることで数週間にわたる安定したトリクル放出が得られることが示されましたが、この方法は比較的大量のステロイドを必要とし、術直後の強い炎症期に理想的とは言えない、最初の短い“バースト”放出しか得られないことがありました。
電極に沿った薬剤ストリップ
新しい研究では異なるアイデアを試しました:シリコーンロッド全体に薬を充填する代わりに、最初の数ミリメートルに浅い溝を彫り、その溝にデキサメタゾン混合シリコーンを充填しました。これらの細長い“ストリップ”は、主な損傷領域に最も近い部分に薬剤のエッジを集中させます。1.3、2.6、5.2マイクログラムの3つのバージョンが作製され、これらをモルモットの内耳に埋め込み、12週間にわたって内耳液を繰り返し採取して薬剤濃度と蝸牛内での分布を追跡しました。濃度は高感度な化学分析で測定されました。
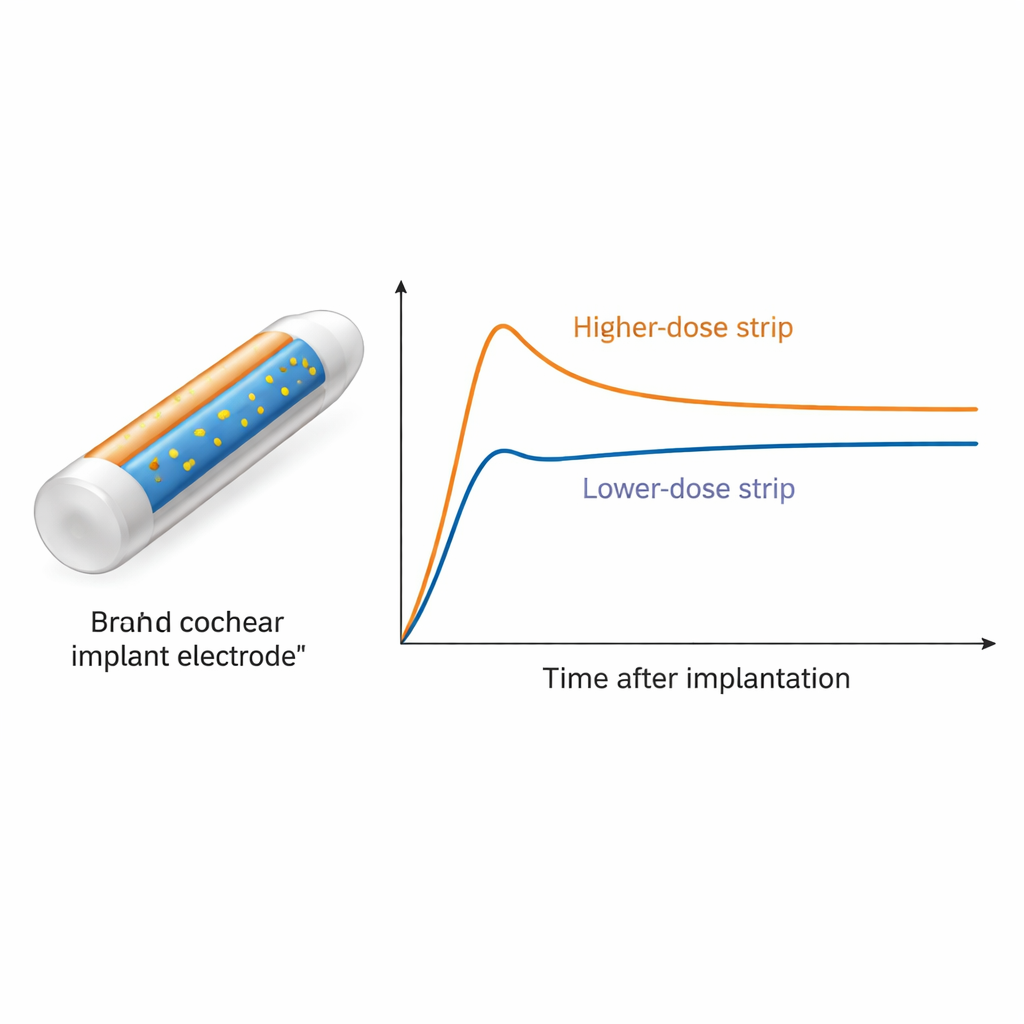
より少ない薬でより長い保護
ストリップコーティングされたロッドは期待された二相性パターンを示しました:初期の急上昇の後、長く穏やかなプラトーが続きます。最高用量のロッド(5.2マイクログラム)は術後1日で約450ナノグラム毎ミリリットルのピーク濃度に達し、その後約1か月かけて徐々に低下し、約50〜60ナノグラム毎ミリリットルの安定領域に入り、少なくとも84日間持続しました。中用量(2.6マイクログラム)は同じ形状を示したものの濃度は低く、12週目には約10ナノグラム毎ミリリットル近辺に落ち着きました。最小用量(1.3マイクログラム)は強い保護を与えると考えられる約50ナノグラム域に達しなかったため、後のサンプリングからは除外されました。42日目に蝸牛の長さに沿って一連の微小サンプルを採取したところ、内耳液の至る所にデキサメタゾンが存在し、埋め込んだロッド付近で最も高く、蝸牛の遠位端に向かっては低いが依然として検出可能な量が得られました。
将来の患者のために、より少ない薬でより多くを
新しいストリップコーティングロッドを以前の全充填ロッドと比較すると、被覆デザインの方が効率的でした。5.2マイクログラムの被覆ロッドは、約10倍の薬を含むロッドと同等のバーストピークを達成し、有用な濃度を同等かそれ以上の期間維持しました。薬剤を表面近くに集中させ、小さな薬剤粒子を使うことで初期放出を促進し、安定した低濃度相への移行を滑らかにしました。これは、実際の人工内耳が術後初期の炎症に対して局所的に強力な保護を提供しつつ、内耳が曝露するステロイドの総量を制限できる可能性があり、安全性に関する懸念を和らげることを意味します。
インプラントを持つ人々にとっての意義
患者にとって究極の目標は、よりやさしい手術と長期的な聴力の向上です。強力な初期バーストの抗炎症薬を放出し、その後数か月にわたって低く安定した濃度を維持する薬剤放出電極は、耳の残存する自然聴力を保護し、瘢痕組織がインプラントの性能を低下させるのを防ぐ助けとなり得ます。本研究は動物実験とダミーロッドを用いたものであるものの、薬剤を電極にどのように、どこに組み込むかを精密に制御することで、内耳に到達する薬物のタイミングと量を微調整できることを示しています。この種の工学的改良は、聴覚を刺激するだけでなく、それが依存する脆弱な構造を積極的に保護する人工内耳への道を開くかもしれません。
引用: Liebau, A., Kammerer, B., Kather, M. et al. Long-term in vivo pharmacokinetics of dexamethasone-loaded cochlear implant electrode carrier dummies with optimized release profiles. Sci Rep 16, 5424 (2026). https://doi.org/10.1038/s41598-026-36620-0
キーワード: 人工内耳, 内耳薬物送達, デキサメタゾン, 聴力保存, 制御放出