Clear Sky Science · ja
早期糖尿病性角膜症における角膜神経構造異常のAI支援検出:深層学習フレームワークの開発と検証
なぜ糖尿病で小さな眼の神経が重要なのか
糖尿病は足や脚の大型神経を侵し、痛みやしびれ、場合によっては切断につながることがよく知られています。しかし、こうした明白な障害が現れるずっと前から、体内で最も小さな神経が機能不全を起こし始めることがあります。眼の前面にある透明な窓である角膜にはこれらの微細な線維が密に存在します。本研究は、高度な画像化と人工知能(AI)を組み合わせることで角膜の早期神経損傷を捉えられることを示しており、糖尿病の人々における神経障害を重症化する前に、痛みを伴わずに検出する新しい方法を提供する可能性があります。
目を通して見る早期神経損傷
現在の糖尿病性神経損傷の検査は決して完璧ではありません。簡便なベッドサイド検査は医師の技量や患者の反応に依存し、微妙な初期変化を見落とすことが多いです。神経伝導検査や皮膚生検のようなより精密な検査は侵襲的で高価なため、日常的なスクリーニングには実用的ではありません。しかし角膜は、生体内共焦点顕微鏡という特殊なカメラで非侵襲的に観察でき、角膜神経の高倍率画像を取得できます。研究者たちはすでに、これらの神経の全体的な減少が糖尿病性神経障害の重症度と一致することを示しています。しかし、最も早い警告サインは必ずしも神経の数の減少ではなく、むしろ一見保たれた繊維上に現れる微細な構造的欠陥であることがあります。
マイクロニューローマと呼ばれる小さなホットスポットに着目する
近年、高性能の顕微鏡を用いる臨床家は、糖尿病患者の角膜神経に沿って小さく明るく腫れた点状の所見を観察してきました。これらの「マイクロニューローマ」は、ストレスを受けた末端や再生中の神経終末を反映していると考えられ、大規模な神経喪失が生じる前に現れることがあります。本研究チームは、コンピュータにこれらの微妙な特徴を自動的に識別させることを目指しました。彼らは中国の2つの眼科センターから糖尿病患者と健康なボランティアを合わせて5,000枚以上の角膜画像を収集しました。経験豊富な角膜専門医が画質の悪い画像を慎重に除外し、マイクロニューローマの存在する領域をラベル付けし、局所的な膨隆、大きな球状の肥大、より拡散した明るい斑点という三つの視覚パターンに分類しました。
神経画像を読むAIアシスタントの学習
専門家がラベル付けしたこれらの画像を用いて、研究者たちは多段階の深層学習システムを構築しました。まず一つ目のAIモデルがぼやけた画像や対象外の画像をふるいにかけ、主要な神経層が明瞭に写っている画像のみを保持しました。二つ目のモデルは与えられた画像にマイクロニューローマが存在するかどうかを判定しました。三つ目のモデルはこれらの病変が現れる正確な領域を輪郭化し、さらに三つの追加モデルがそれらを三つの視覚型に分類しました。このシステムは一つの病院のデータで訓練され、その後同一施設の未見の画像と、別の病院からの完全に独立した集団でそれぞれテストされ、異なる患者群や撮像条件でも信頼して機能するかを検証しました。
実際の性能はどれほどか
AIは基本的な画質管理で非常に高い精度を示し、使用可能な画像を97%以上の確率で正しく判定しました。マイクロニューローマの有無を判定する際には、内部および外部のテストセットのいずれでも約81〜84%の正答率を示しました。病変のセグメンテーションとサブタイプ分類の能力も良好で、二次センターのデータに対しても比較的高い性能を維持しました。臨床での実用性を評価するために、研究チームはこの画像手法の正式な訓練をあまり受けていない若手眼科医に別の150枚の画像セットをまず自力で読影させ、次にAIの支援を受けて読ませました。AIの支援により、彼らの診断精度は約69%から88%に上昇し、画像1枚あたりの平均読影時間は半分以上短縮されました。これは、この種のツールが診療の効率を高め、臨床医の視覚的負担を減らす可能性を示唆しています。
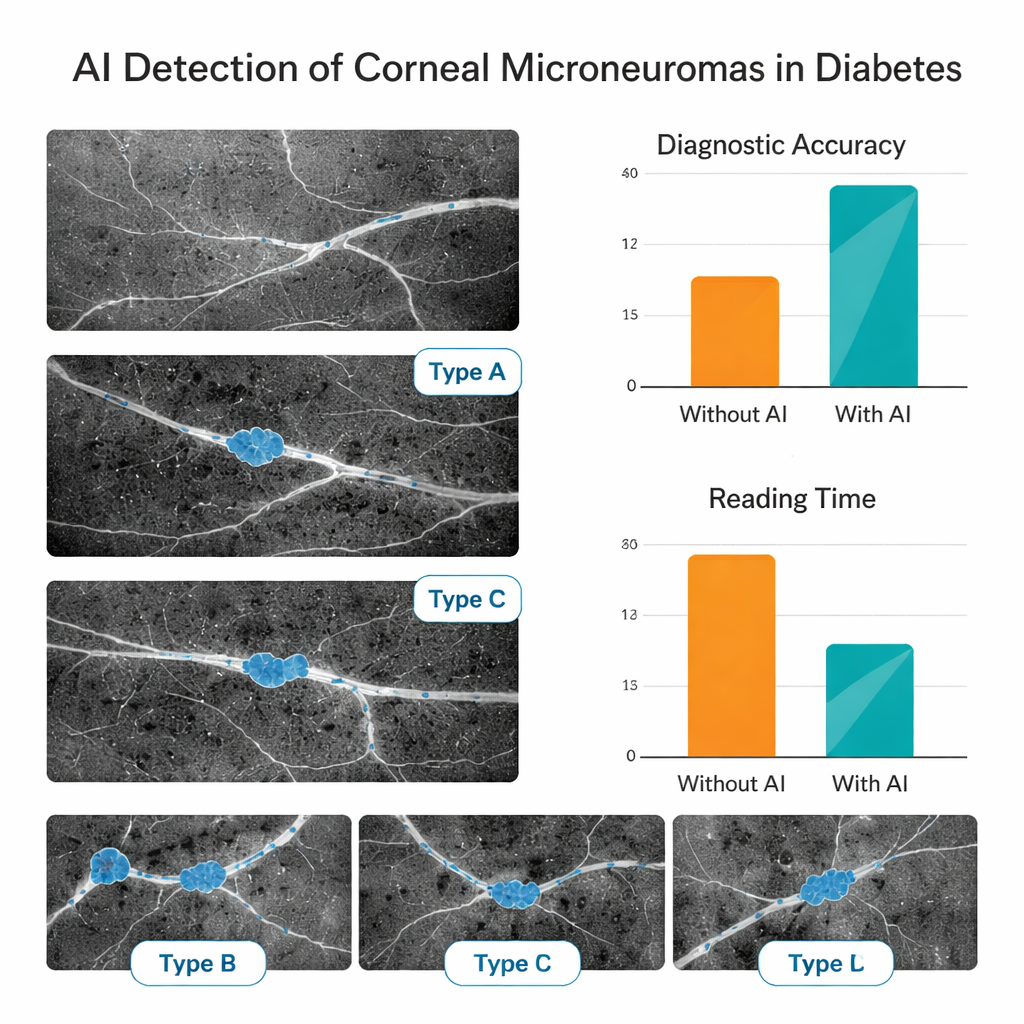
糖尿病患者にとっての意義
この研究は、慎重に訓練されたAIシステムが角膜の微小な神経異常を自動で検出・記述できること、そしてそれが経験の浅い医師による複雑な眼科画像の解釈を大幅に助けることを示しています。研究はまだ初期段階であり、二つのセンターからの後ろ向きデータに基づいているとはいえ、眼表面が体内の小さな神経の健康状態を映す「窓」として機能するという考えを強化します。将来、多施設にわたる長期研究で角膜マイクロニューローマが早期の糖尿病性神経障害を確実に示すことが確認されれば、この種のAI支援画像診断は、糖尿病患者のスクリーニング、進行の追跡、そして神経損傷が不可逆的になる前の介入の迅速で非侵襲的な手段となる可能性があります。
引用: Pan, J., Shi, X., Wan, L. et al. AI-Assisted detection of corneal nerve structural abnormalities in early diabetic keratopathy: development and validation of a deep learning framework. Sci Rep 16, 5846 (2026). https://doi.org/10.1038/s41598-026-36576-1
キーワード: 糖尿病性ニューロパシー, 角膜神経, マイクロニューローマ, 深層学習, 生体内共焦点顕微鏡