Clear Sky Science · ja
宿主のm6A修飾が細胞特異的フェロプトーシスを引き起こす微生物群を形作り、慢性呼吸器疾患への因果経路となる
なぜあなたの微生物が肺に関係するのか
喘息や慢性閉塞性肺疾患(COPD)などの慢性的な呼吸障害は、たいてい喫煙、汚染、アレルギーのせいにされます。本研究は、もう一つあまり明白でない関係者、すなわち腸や皮膚に生きる数兆の微生物を示唆します。大規模な遺伝データを用いて、著者らは特定の微生物が単に肺疾患に伴うだけでなく、細胞内の微妙な化学変化と鉄依存の細胞損傷という経路を通じて疾患を引き起こす助けとなり得ることを示しました。この隠れたネットワークを理解することで、微生物やその分子経路をより健康的な方向に導く新しい予防・治療法が将来生まれる可能性があります。
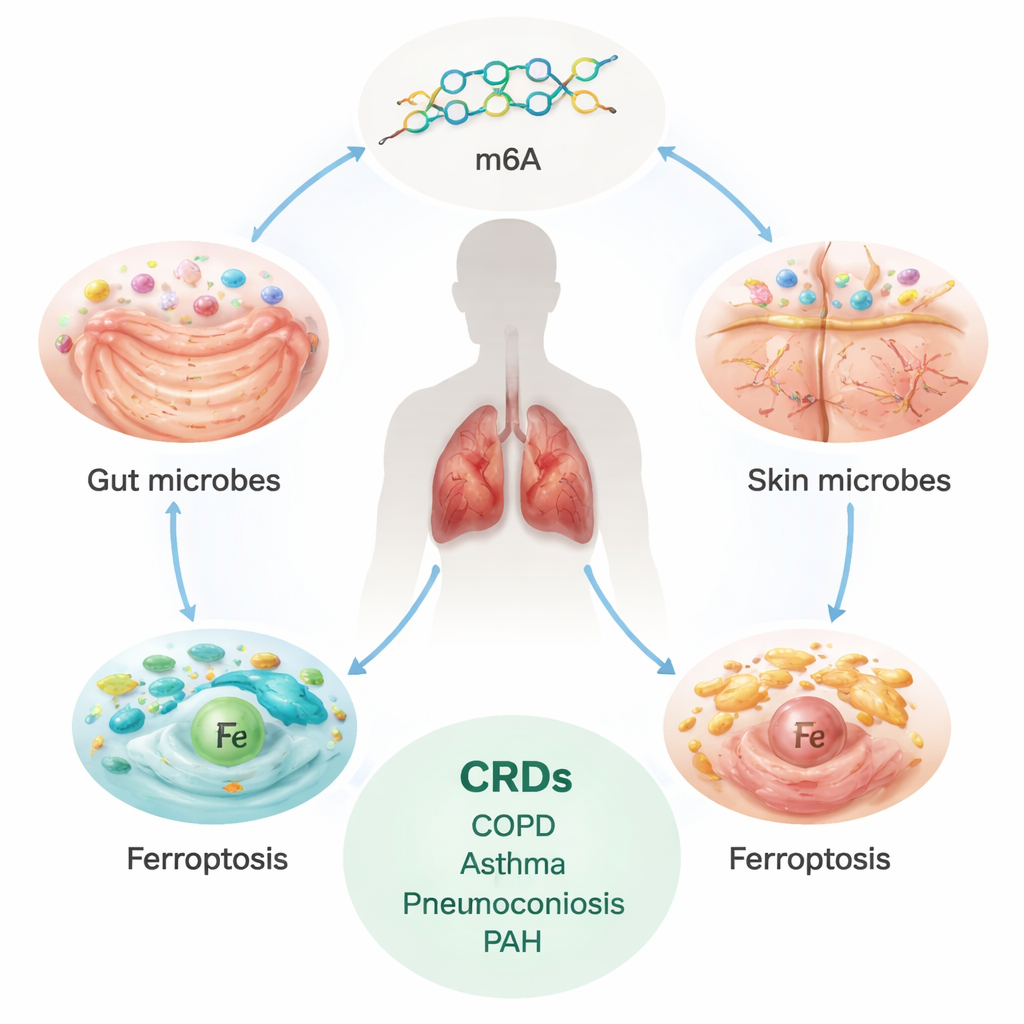
慢性肺疾患の隠れた負荷
COPD、喘息、間質性肺疾患(ILD)、粉じん症、肺動脈性肺高血圧症(PAH)を含む慢性呼吸器疾患は、世界中で数億人に影響を与え、毎年数百万人の死因となっています。これらの病状は多くの場合ゆっくりとしかし着実に進行し、肺や血管に瘢痕や再構築を残して息切れを招きます。現在の治療は主に症状の管理にとどまり、根本的な損傷を完全に止めたり逆転させたりするものではありません。こうしたことから、研究者たちは重篤な病気になる前に修正可能なより深い根本原因を探すようになりました。
腸と皮膚にいる微生物の仲間たち
現在では、腸や皮膚が免疫系の教育、代謝の形成、バリア防御の維持に寄与する複雑な微生物コミュニティの住処であることが分かっています。では、これらの微生物は実際に肺疾患を駆動しているのか、それとも人が病気になるにつれて単に変化しているだけなのでしょうか。因果を見分けるために、研究者たちはメンデルランダム化法を用いました。これは人々の生涯にわたる「自然な実験」として遺伝的差異を利用する手法です。彼らは数百の腸内および皮膚微生物型に関する遺伝データを、欧州の大規模研究による5つの主要な慢性肺疾患データと組み合わせ、特定の微生物の高低傾向が各疾患のリスクと関連するかを検証しました。
肺を助ける微生物、害する微生物
解析により、各呼吸器疾患のリスクを増減させる多数の腸内微生物が同定され、しばしば疾患ごとに特異的なパターンが見られました。例えば、特定の腸内細菌はCOPD、喘息、PAHに対して保護的に働くように見え、他の菌はILDやCOPDのリスクを高めていました。皮膚微生物は効果はより控えめながらも検出可能な関連を示し、種によってはある条件でリスクを高め、別の条件で低下させるものがありました。研究チームは解析の方向を反転させることも行い、COPDや喘息などの遺伝的リスクが腸内および皮膚の微生物叢の変化を予測することも見出しました。この双方向のやり取りはフィードバック・ループを示唆しており、微生物が肺疾患の形成に関与し、肺疾患がまた我々の微生物生態系を再形成し得ることを示しています。
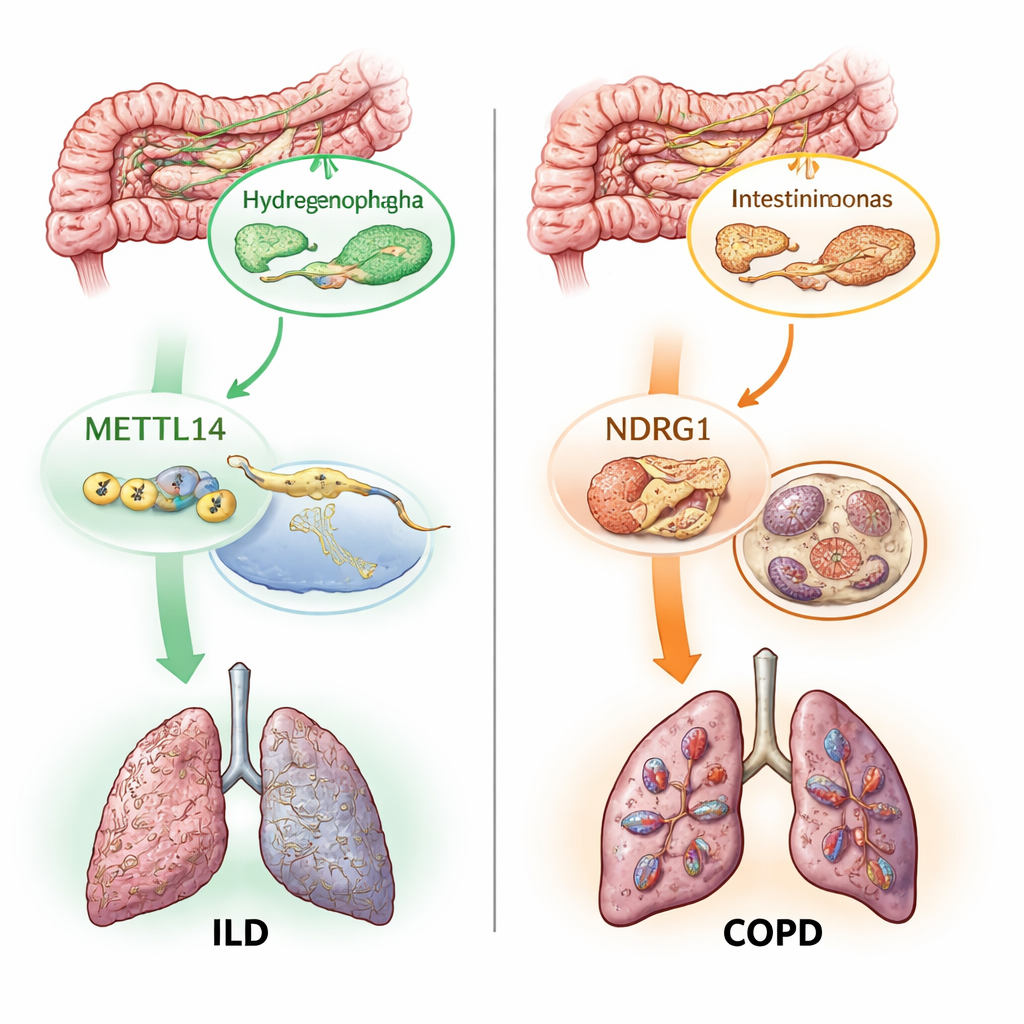
二つの分子スイッチ:RNA標識と鉄依存の細胞死
どの微生物が重要かを地図化するだけでなく、著者らはこれらの微小な仲間がどのように肺組織に影響するかを問いました。注目したのは既に肺障害に関与すると疑われている二つの分子過程です。第一はm6A修飾と呼ばれる、RNAに付加される小さな化学タグで遺伝子のオン・オフを調節するものです。第二はフェロプトーシスで、脂質の過酸化による暴走的な酸化が引き金となる鉄依存の細胞死の一形態です。19のm6A関連遺伝子と数百のフェロプトーシス関連遺伝子に対する遺伝的代理を用いて、これらの経路の変化が肺疾患と因果関係にあるかを検証しました。その結果、m6Aのライター遺伝子の一つMETTL14はILDのリスク低下と関連し、NDRG1を含む複数のフェロプトーシス関連遺伝子はCOPD、ILD、喘息のリスク増加と関連していることが分かりました。
点を結ぶ:微生物から細胞へ、そして疾患へ
この研究で最も斬新だったのは、これらの要素が因果の連鎖としてどのように組み合わさるかをたどった点です。統計的媒介解析は、METTL14のILDに対する保護効果の一部が特定の腸内細菌であるHydrogenophagaに及ぼす変化を通して働くことを示唆しました。別の経路では、腸内細菌Intestinimonas massiliensisがNDRG1とフェロプトーシスの活性化を部分的に介してCOPDリスクに影響しているように見えました。研究チームはさらにヒトの肺組織データを確認し、METTL14とNDRG1の両方が疾患組織と健康組織で発現が異なることを確認しました。最後に、単一細胞の遺伝地図を用いて免疫細胞を詳しく調べたところ、NDRG1のCOPDに対する有害な影響が単球の一サブセットという特定の免疫細胞型に結びついていることが示され、将来この遺伝子を標的にする薬は細胞特異的に作用させる必要がある可能性を示しました。
将来の治療にとっての意義
専門外の読者への要点は、肺の健康は呼吸するものだけで決まるのではなく、私たちの体内外に住む微生物とそれらが細胞内で切り替える分子スイッチにも左右されるということです。本研究はすべてのステップを実験的に証明するものではなく、主に欧州系の人々に限定されるという限界がありますが、遺伝学的な強い手がかりを提供し、腸内微生物、m6AのようなRNA標識、そして鉄依存の細胞死が慢性肺損傷へとつながる連結経路を形成していることを示しています。長期的には、この研究はマイクロバイオームを基盤とする治療とMETTL14、NDRG1、あるいはフェロプトーシスを標的とする薬を組み合わせ、症状緩和にとどまらず慢性呼吸器疾患の進行を断ち切ることを目指す新しい戦略に着想を与える可能性があります。
引用: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
キーワード: 腸内マイクロバイオーム, 慢性肺疾患, 喘息とCOPD, RNAエピジェネティクス, 細胞死経路