Clear Sky Science · ja
ATF4はミトコンドリア機能不全とミトファジーを調節し、角膜内皮細胞のアポトーシスに寄与する
なぜ眼の窓は曇るのか
角膜――目の前面にある透明な窓――は、その内面にある薄くて働き者の細胞層によって透明性を保たれています。フックス内皮角膜ジストロフィー(FECD)では、この細胞が徐々に失われ、角膜のむくみや視界の濁りを招き、しばしば角膜移植が必要になります。本研究は基本的かつ重要な疑問を投げかけます:これらの細胞が死を選ぶ原因は何か、そしてある分子の“スイッチ”を切ることで細胞を救えるのか、ということです。
視界を保つもろい細胞層
角膜内皮は六角形の細胞が一枚に並んだシートで、角膜から過剰な液体を絶えず排出して透明性を保っています。FECDではこれらの細胞がストレスを受けて徐々に消失し、基底膜上にグッタ(異常な物質の隆起)が蓄積します。FECDに対する承認された薬剤はなく、主要な治療は角膜移植であるため、研究者たちは細胞内のどのストレス応答がどのようにして細胞死へと駆り立てるのかを詳細に理解しようとしています。以前の研究は、タンパク質折りたたみを担う小胞体(ER)と細胞のエネルギー源であるミトコンドリアという二つの重要な細胞区画のいずれにもストレスが生じることを示していましたが、これら二つのストレス応答が互いにどのように連絡し合うかは明らかではありませんでした。
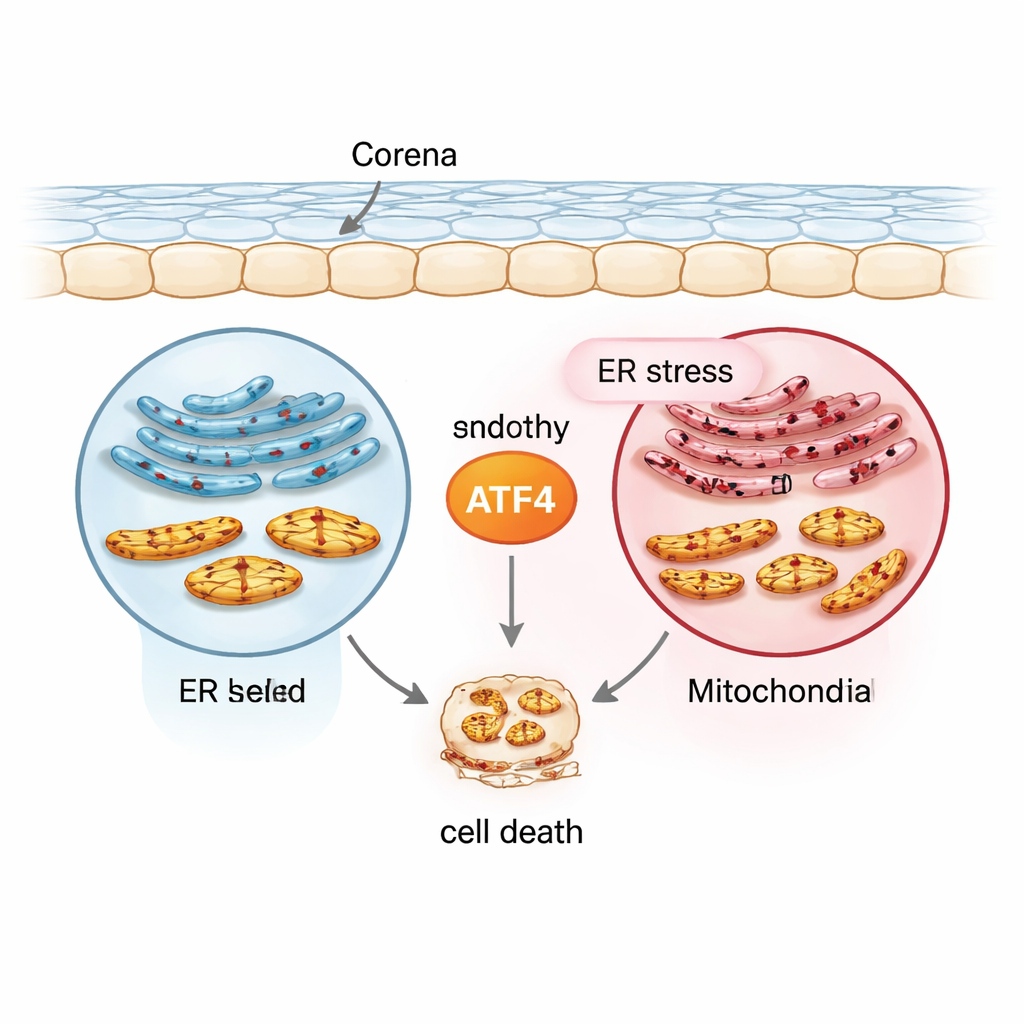
中心にいるストレス伝達係:ATF4
研究チームは転写因子であるATF4に注目しました。ATF4は多くのストレス応答遺伝子のオン/オフを切り替えます。彼らは正常なヒト角膜内皮細胞株(21T)、疾患関連のTCF4リピート拡張を保持するFECD様細胞株(F35T)、一次ヒト角膜内皮細胞、UVAに曝露したマウスモデルを用いて慢性的なストレスを模した一連の条件を作り出しました。小胞体ストレスはチュニカマイシンという薬剤で誘導し、ATF4や他のマーカーを測定しました。正常細胞と比較して、FECD様細胞はそもそもATF4や関連するストレスタンパク質のレベルが高く、慢性的ストレス下では培養細胞やヒト角膜組織の両方でATF4がさらに上昇しました。このパターンは、ATF4が初期の保護的反応と後期の自己破壊的シグナルの分岐点に立っていることを示しています。
エネルギー喪失からプログラムされた死へ
次に研究者らはこのストレスがミトコンドリアにどのような影響を与えるかを調べました。FECD様細胞ではミトコンドリアのATP産生が低下し、膜電位が失われ、長く網目状だった形が多数の小さな断片に分裂しました。これらの変化は小胞体ストレスが持続すると悪化しました。同時に、活性化されたカスパーゼや切断された形のPARPといった古典的な細胞死関連タンパク質が増加し、Bcl‑2のような保護的タンパク質は減少しました。これらの変化は総じて、FECDでストレスを受けた角膜内皮細胞がミトコンドリア主導のアポトーシスへ押し流されていることを示しています。アポトーシスは整然としているものの不可逆的なプログラム細胞死です。
慢性ストレス下で停滞する掃除システム
通常、重度に損傷したミトコンドリアはミトファジーと呼ばれるリサイクル過程で除去され、タグ付けされて小胞に包まれて処理されます。チームは、初期のミトファジー開始分子(ParkinやLC3)が、特にストレス後に正常細胞とFECD様細胞の両方で活性化されることを見出しました。しかし、重要な補助タンパク質は減少しており、電子顕微鏡観察では小胞内に部分的に分解されたミトコンドリアが蓄積しているのが確認されました。これは、掃除プロセスは始まるものの完了せず、細胞内に故障した“発電所”が残ってさらなるストレスと細胞死を助長していることを示唆します。
ATF4をオフにして細胞を救う
ATF4がこの悪循環を主導しているかを確かめるため、研究者らは培養角膜内皮細胞で小干渉RNAを用いてATF4を部分的にサイレンシングしました。同じ慢性ストレス条件下で、ATF4を減らした細胞は死を促進するタンパク質のレベルが低く、ミトコンドリア膜電位は保たれ、断片化は少なく、細胞生存性試験でもより良い生存を示しました。重要なことに、停滞したミトファジー構造の数は減少し、ATF4を低下させることで損傷と掃除のバランスがより効果的に回復したことが示唆されました。ATF4遺伝子を一コピーだけ持つように遺伝子改変されたマウスでは、UVA曝露で死を促進するパートナータンパク質CHOPの活性化が抑えられ、ATF4が十分に存在するマウスと比べてより正常に近い形の内皮細胞が保持されました。
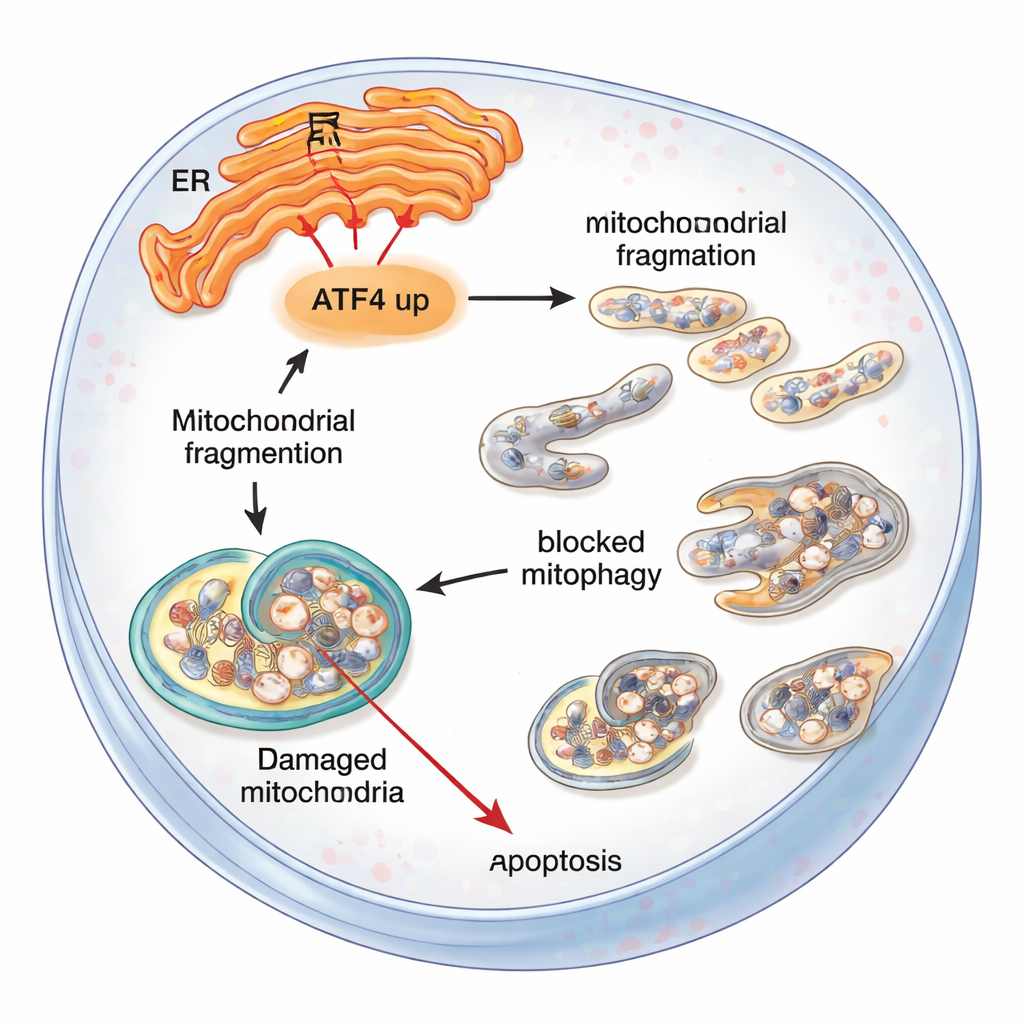
FECDの患者にとっての意味
専門外の読者に向けた要点は、ひとつのストレス伝達因子であるATF4が角膜内皮細胞を対処から崩壊へと傾けうるということです。小胞体ストレスが長引くと、ATF4はミトコンドリアを乱し、細胞の掃除機構を停滞させ、最終的にこれらの重要な細胞の自己破壊を促します。ATF4を遺伝的に(マウスで)あるいは細胞内で標的分子を用いて抑えることで、ミトコンドリアが保護され、廃棄物除去が改善され、より多くの細胞が生存します。本研究はまだ実験室および動物段階にありますが、ATF4と関連するストレス経路が将来的にフックスジストロフィーの進行を遅らせたり防いだりし、角膜移植の必要性を減らす可能性のある有望な薬剤標的であることを示しています。
引用: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
キーワード: フックス内皮角膜ジストロフィー, 角膜内皮, ミトコンドリアストレス, ミトファジー, ATF4