Clear Sky Science · ja
QAL333の抗腫瘍活性と予測モデリング:統合トランスクリプトミクス・バイオインフォマティクス解析が示す選択的細胞毒性と感受性決定因子
なぜこの新規化合物が重要か
がん薬は患者によって効果の出方が大きく異なることが多く、その主因は腫瘍内部の配線(分子機構)の違いにあります。本研究は新たに設計された化合物QAL333を紹介しており、いくつかの大腸がんに対しては強い効果を示す一方で、多くの正常細胞には比較的影響を与えないことを示します。同様に重要なのは、腫瘍細胞の遺伝子活動パターンから、誰が利益を得やすいかを予測できる可能性を示している点で、より精密で個別化された治療戦略の可能性を示唆します。
特定の腫瘍タイプへの局所的な攻撃
研究チームは、すでにがん細胞を傷害することが知られている化合物群に関連する合成分子QAL333を、15種類のヒトがん細胞株と3種類の非がん細胞株の広いパネルで評価しました。その結果、大腸がん細胞、特にSW620と呼ばれる系統が高い感受性を示し、比較的低用量で細胞死を引き起こしました。対照的に、トリプルネガティブ乳がん細胞ははるかに耐性が高く、臨床的に安全に到達するのが難しい、十倍以上の用量を必要としました。興味深いことに、非がん細胞でも反応は一様ではなく、感受性を示すものもあれば、広く用いられる腎臓由来の細胞株のように驚くほど耐性の高いものもありました。こうしたパターンは、QAL333の効果が「がん」か「正常」かというラベルよりも、細胞内部の生物学的性質に強く依存することを示しています。
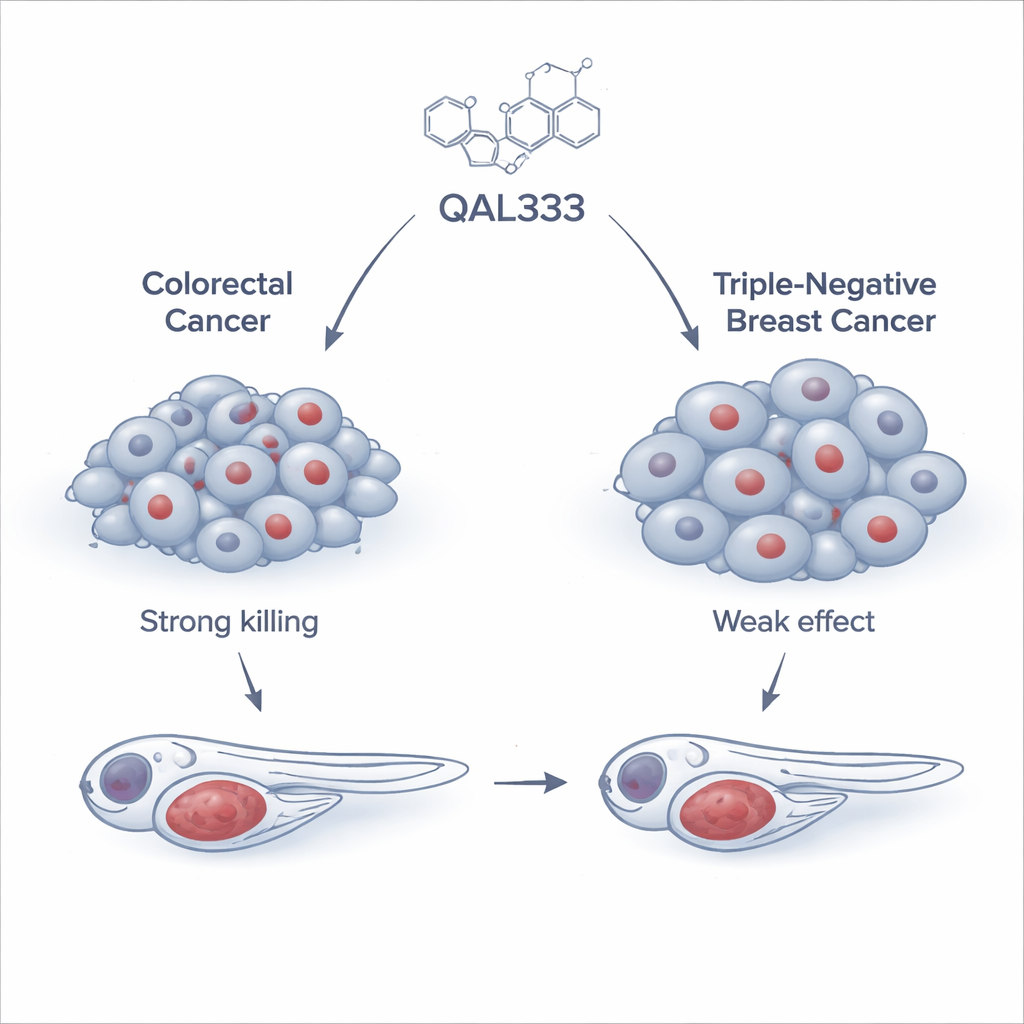
生体内での薬効評価
培養細胞での有望な結果が生体内でも再現されるかを確かめるため、研究者たちはゼブラフィッシュを用いました。ゼブラフィッシュは透明な胚を持ち、ヒト疾患モデルに広く利用されています。蛍光標識したヒトがん細胞をゼブラフィッシュ胚に移植し、QAL333で処理したところ、大腸がん細胞を移植した魚では腫瘍増殖が明らかに抑制され、臨床で使われる標準的な化学療法併用療法の効果に近づく結果が得られました。対照的に、トリプルネガティブ乳がん由来の腫瘍はほとんど反応せず、同じモデルで一般的な乳がん薬であるパクリタキセルはよく効いたことから、これらのin vivo検査はQAL333の効果がすべてのがんに共通するものではなく、一部の腫瘍に限られることを補強しました。
QAL333が細胞内でどのように作用するかを探る
なぜ一部の細胞は死に、一部は抵抗するのかを理解するため、研究者たちはQAL333処理後の何千もの遺伝子の活動変化を測定しました。感受性の高い大腸がん細胞では、細胞分裂や増殖を駆動する主要遺伝子が抑制され、主要な生存経路も弱まっていました。酸化ストレスや古典的なプログラム細胞死とは異なる形の細胞死に関連するシグナルも変動しており、QAL333がこれらの細胞内の損傷管理システムを過負荷にしていることを示唆します。これに対して耐性のある乳がん細胞は、NF-κBのような因子により制御されるストレス応答や炎症プログラムを立ち上げ、有害な状況に対処する能力を高めていました。こうした対比は、QAL333が弱い防御機構を持つ細胞を圧倒する一方で、別の細胞は効果的な反撃を行うという図を描きます。
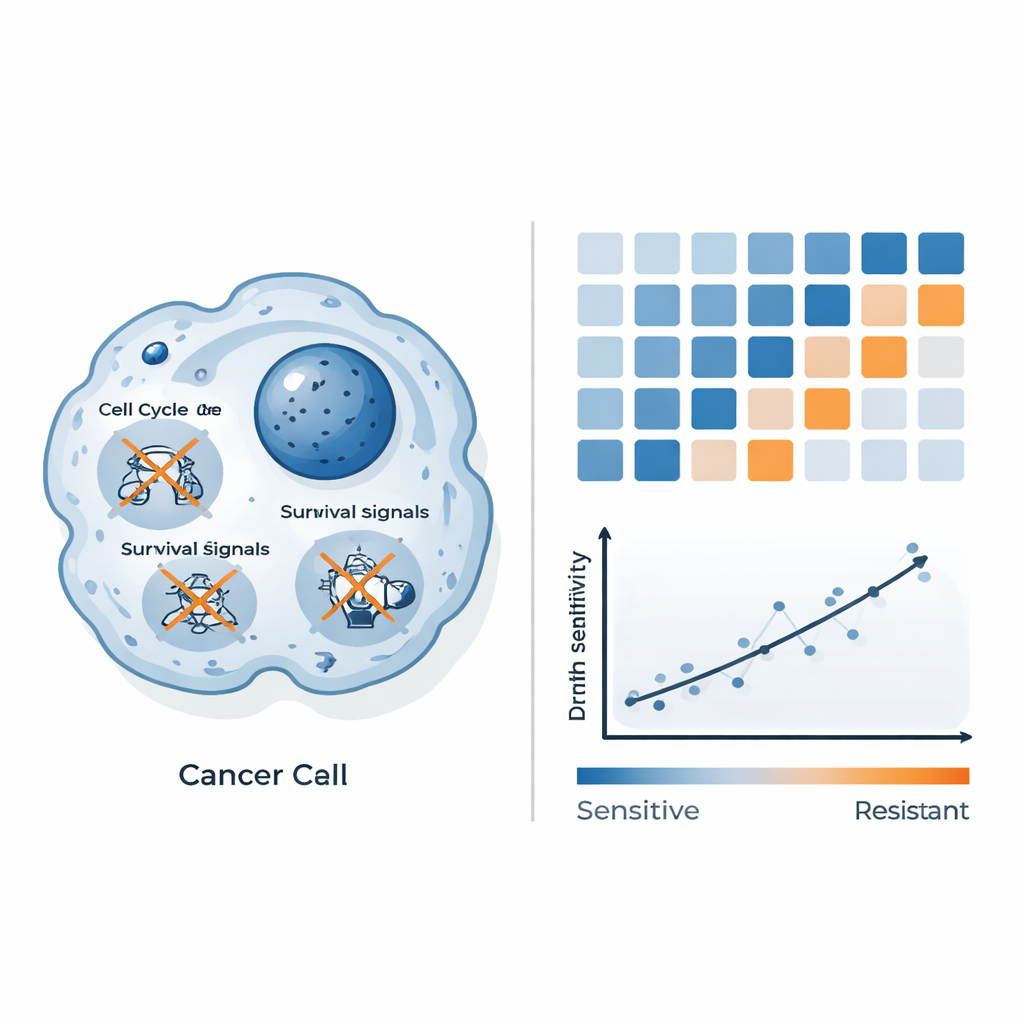
遺伝子パターンを用いた応答予測
遺伝子変化のカタログ化にとどまらず、研究者たちはこれらのパターンを実用的な予測ツールに変換できるかを検討しました。彼らは細胞株パネルのベースライン遺伝子活動データと実測の薬剤感受性を組み合わせ、機械学習を用いて最も情報量の多いシグナルを探索しました。単一遺伝子に頼るのではなく、遺伝子を生物学的経路にまとめ、三つのシステムから構成される「経路スコア」を作成しました:エネルギーや化学物質の処理(代謝経路)、周囲環境の組織化(プロテオグリカンや関連構造を含むがんに関わる経路)、および細胞内部の骨格の配列です。この総合スコアはQAL333で各細胞株を殺すのに必要な濃度と強く相関しました。スコアが低いほど感受性が高く、スコアが高いほど耐性が強い、つまりこれらのネットワークの調整状態が、QAL333の有効性を予測する可能性があることを示しています。
意外な幅広い生物学的影響の示唆
主な焦点はがんでしたが、QAL333は「クオラムセンシング」と呼ばれる細菌のコミュニケーションシステムを撹乱する能力も示しました。非常に低用量で、この化合物は歯周病菌のバイオフィルム形成を抑え、免疫細胞における特定の炎症シグナルを弱めました。著者らはこれらを初期の探索的所見として扱っていますが、QAL333または関連分子が将来的に、細菌コミュニティの除去が難しい感染症など、がん治療以外の用途を持つ可能性を示唆しています。
将来の患者にとっての意味
総じて、本研究はQAL333を、脆弱な大腸腫瘍を選択的に標的にする候補薬として位置づけるとともに、どの腫瘍が反応しやすいかを予測するための青写真を提示しています。さらなる高度な動物モデルや最終的には患者で確認されれば、単純な遺伝子発現テストが医師にQAL333が適合するかどうかの判断を助け、各腫瘍の配線に合わせたがん治療という大きな目標に整合します。一方で、本研究は有望な薬剤にも限界があることを強調しており、乳がんなどの耐性腫瘍には賢い併用療法や全く異なる戦略が必要になる可能性があります。
引用: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
キーワード: 大腸がん, 標的療法, 遺伝子発現, 薬剤感受性モデリング, ゼブラフィッシュ異種移植モデル