Clear Sky Science · ja
インシリコQSARモデリングからインビトロMTTアッセイへ:三陰性乳がん(TNBC)および皮膚がんに対する新規uPARリードの実験的検証
この研究が重要な理由
三陰性乳がんや特定の皮膚がんのようながんは、転移が早く標準治療に耐性を示すことが多いため、治療が非常に困難です。本研究は、がん細胞表面に存在する有望な新しい標的であるuPARに着目し、コンピュータベースの薬物設計と実験室での検証を組み合わせることで、これらの攻撃的な腫瘍の進展を遅らせたり止めたりする可能性のある新しい薬物候補を見出せることを示しています。
がんの拡がりを助ける出入口
腫瘍が致命的になるためには、細胞が元の部位から離れて周囲組織を突破し、血流に入り、遠隔臓器に植民する必要があります。uPARはこの過程で重要な役割を果たします。uPARはがん細胞表面に存在し、パートナータンパク質と協調して基質を分解する酵素を活性化し、細胞が移動・浸潤しやすくします。uPARは特に三陰性乳がん細胞や一部の皮膚がん細胞で高く発現しており、その豊富さは増殖の速さ、浸潤性の高さ、患者予後の悪化と関連しています。このため、uPARは魅力的でありながらこれまで十分に活用されてこなかった抗がん薬の標的です。
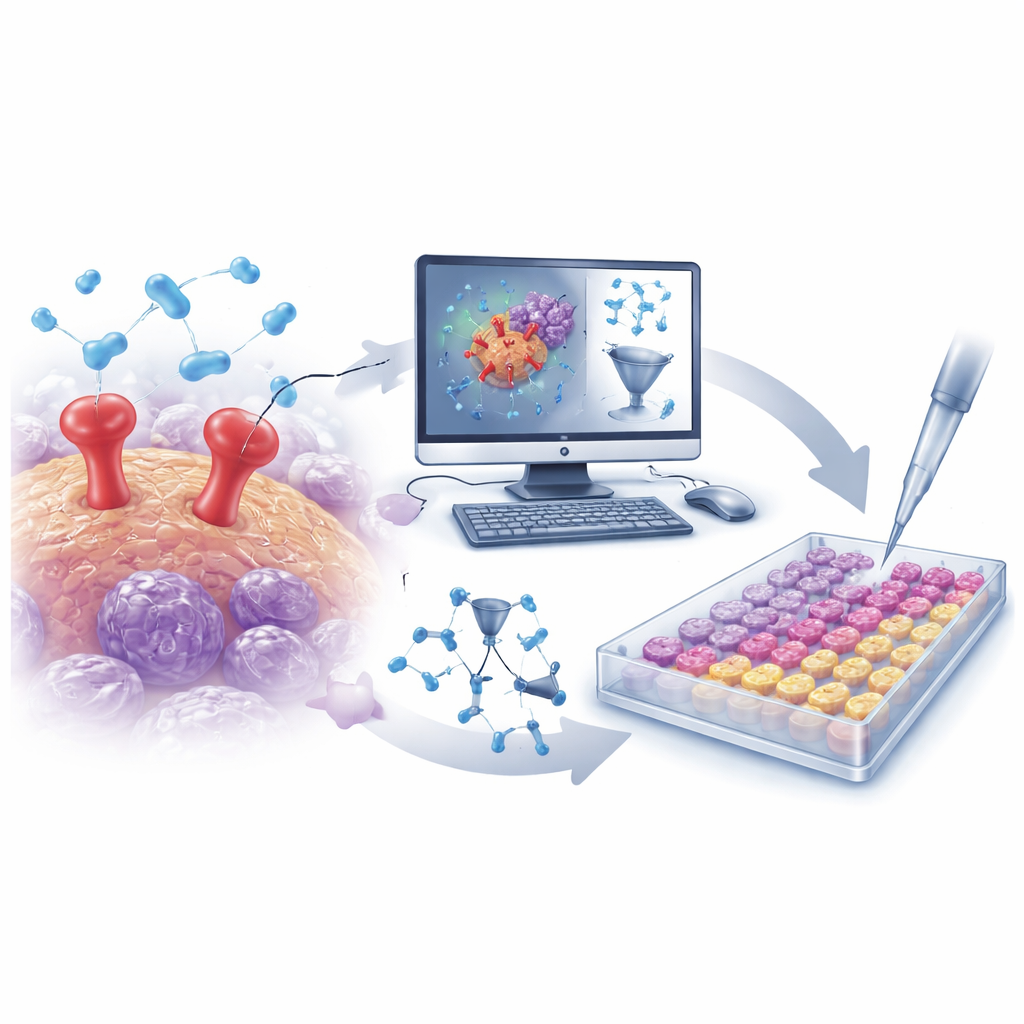
賢いアルゴリズムで大規模化学データを掘る
研究者らはまず、公開データベースから500を超える既知のuPAR阻害分子を集め、大規模な化合物集合を構築しました。各分子の構造は、サイズ、形状、電荷分布、柔軟性などの特徴を捉える何千もの数値記述子に変換されました。これらのデータを用いて、研究チームは定量構造活性相関(QSAR)モデルを構築しました。QSARは、どの構造的特徴が分子を強力なuPAR阻害剤にするかを学習する数学的ツールです。過学習を避けるための慎重な検証の後、このモデルは未知の化合物に対しても高い予測力を示し、uPAR阻害を強めるあるいは弱めるいくつかの重要な特徴を明らかにしました。これらの知見が新たな、より良く設計された分子の探索を導きました。
仮想スクリーニングから試験管へ
訓練済みのQSARモデルを手に、チームは約3万件のプロテアーゼ標的化化合物からなるフォーカスライブラリを仮想スクリーニングしました。モデルはこの膨大なプールを素早く絞り込み、有望なuPAR阻害候補の小さなセットを抽出しました。同時に、コンピュータドッキングシミュレーションで各候補がuPAR結合部位にどの程度適合するかを評価し、分子動力学シミュレーションでこれらのドッキング複合体が時間経過で安定に保たれるかを検証しました。このインシリコの統合キャンペーンから、二つの注目分子が浮上しました。QSARモデルで高い活性が示唆されたD685‑0061と、ドッキングおよびシミュレーションでuPARと特に安定した相互作用を形成すると判断されたC878‑1660です。
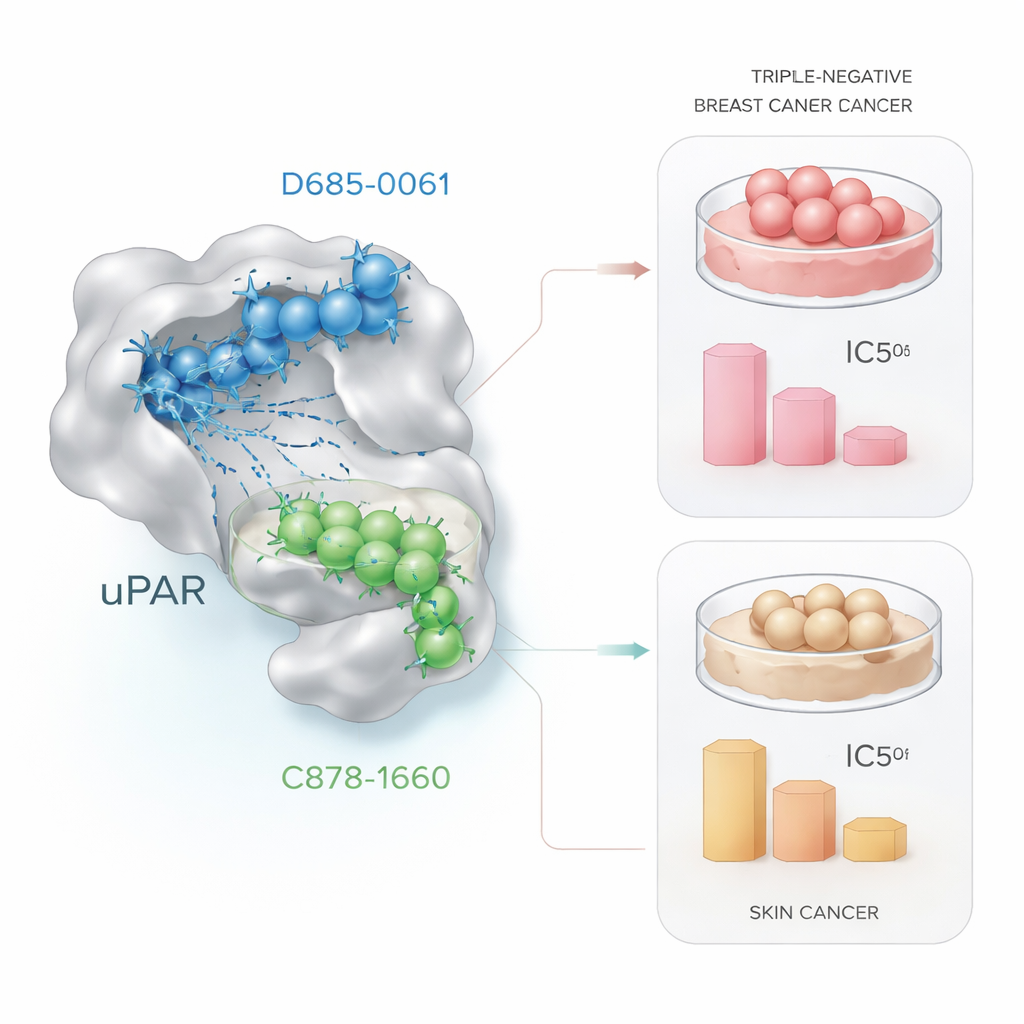
がん細胞で候補を実際に試す
計算上の有望性は、実際の生物学的効果に結びついて初めて意味を持ちます。これを検証するために、研究者らは生細胞に二つのリード化合物を段階的に投与し、標準的な実験法であるMTTアッセイを用いて細胞生存率を測定しました。三陰性乳がん細胞(MDA‑MB‑231)では、D685‑0061がより効率的に細胞を死滅させ、約21マイクロモルで生存率を半減させました。一方C878‑1660はおよそ4倍の濃度を必要としました。顕微鏡観察では、D685‑0061処理細胞に丸まり、基板から剥がれ、断片化するなどのプログラムされた細胞死の明瞭な兆候が見られました。対照的に、皮膚がん細胞(A431)ではC878‑1660のほうが強い殺傷活性を示し、約19マイクロモルで50%の細胞死を達成したのに対し、D685‑0061は約28マイクロモルを要し、いずれも用量依存的な損傷が観察されました。
今後のがん治療にとっての意義
本研究は即座に新薬をもたらすわけではありませんが、有望な二つの出発点と、それと同等に重要なより多くの候補を見つけるための強力な設計図を提供します。ビッグデータモデリング、3次元シミュレーション、そして慎重な細胞ベースの実験を結びつけることで、uPARを選択的に標的化する小分子が攻撃的な乳がんおよび皮膚がん細胞を損傷し得ることを示しました。D685‑0061とC878‑1660は現在、化学者が効力を高め、安全性を改善し、体内動態を最適化するために精製できるリード化合物として機能します。長期的には、このアプローチに基づく薬剤がuPAR駆動型がんの転移を阻止し、今日最も危険ながんのいくつかをより管理可能な病態へと変える助けとなる可能性があります。
引用: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
キーワード: uPAR阻害剤, 三陰性乳がん, 皮膚がん, コンピュータ支援薬物設計, MTT細胞生存性アッセイ