Clear Sky Science · ja
MNX1を介したヒストン修飾とPBX遺伝子ファミリーの役割:MNX1誘導性白血病形成における検討
なぜ小さな遺伝的異常が病む子どもたちに重大なのか
小児白血病の多くは現在治療可能になっていますが、乳児に起こるまれな型、乳児急性骨髄性白血病(AML)は依然として特に致死的です。こうした乳児の多くには同じ遺伝的事故が見られます:二本の染色体が断片を交換し、発生期に静かな働きをしている遺伝子MNX1が過剰に活性化するのです。本研究は単純だが重要な問いを投げかけます:MNX1が過剰発現した後、若い血液細胞内で実際に何を行い、どのようにがん化へと押し進めるのか――そしてその過程は阻止できるのか?
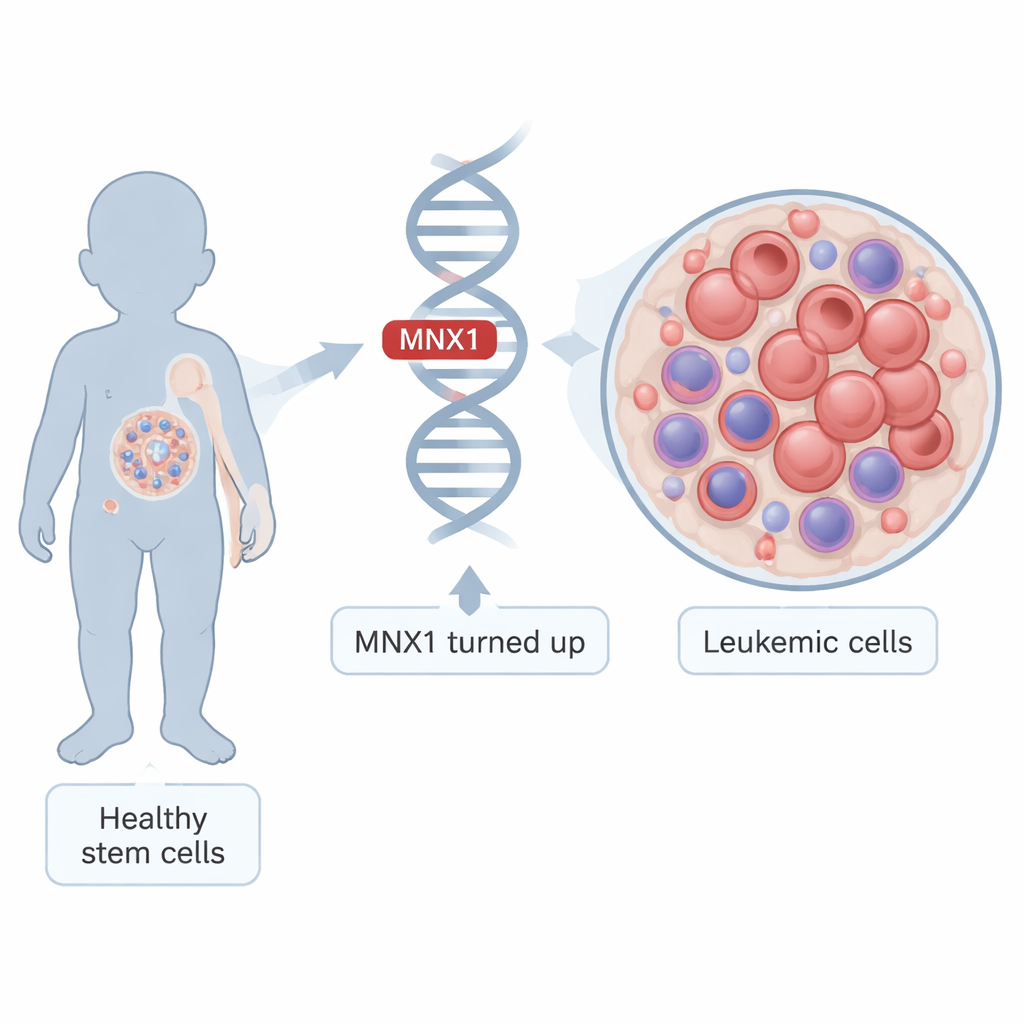
正常な乳児の血液細胞から暴走する増殖へ
白血病は未熟な血液細胞が成熟を止め、制御されずに増殖し始めると発生します。t(7;12)という染色体交換を持つ乳児では、MNX1が胎児肝や骨髄に存在する非常に早期の造血細胞で異常に活性化します。研究者らはこの状況を模倣するマウスモデルを作成しました:胎児の造血幹細胞でヒトMNX1をオンにし、それらをマウスに移植して、動物が前白血病状態から完全な白血病へと進行するのを観察しました。こうして得た異なる段階の細胞を健常対照と比較することで、MNX1が時間をかけて細胞内の制御システムをどのように書き換えるかをたどることができました。
MNX1は細胞の“指令書”を書き換える
MNX1は転写因子であり、DNA上に結合してどの遺伝子がオンまたはオフになるかを制御するタンパク質です。研究チームは質量分析、RNAシーケンス、クロマチンプロファイリングなど複数の強力な手法を組み合わせ、MNX1がどのようなパートナーと働き、どの遺伝子を変えるかを調べました。MNX1は、DNAが巻き付くスプール状のタンパク質であるヒストンに化学的な印(修飾)を付ける酵素と協働することが明らかになりました。特にMNX1は“ON”の印であるH3K4me3を増やし、“OFF”の印であるH3K27me3を特定箇所で減らします。これらの変化は局所的なDNA構造を緩め、増殖に関わる重要な遺伝子が発現しやすくなります。
重要な制御遺伝子への“ヒット&ラン”の押し付け
影響を受ける多数の遺伝子の中で際立っていたのはPbx1でした。Pbx1は長く白血病と関連づけられてきたPBXファミリーのDNA結合タンパク質の一員です。本研究はMNX1がPbx1遺伝子の制御領域に直接結合し、そこにONの印を付け、OFFの印をはぎ取ることを示しました。これによりPbx1の発現が非常に早い段階、すなわち細胞がまだ前白血病状態にある段階で立ち上がります。驚くべきことに、後期――白血病が確立した段階では――MNX1自身はその部位に強く結合していないことが多いものの、Pbx1遺伝子は依然として発現し続け、ヒストン修飾も促進された状態のまま残ります。これはいわば“ヒット&ラン”機構を示唆します:MNX1はクロマチンの重要領域に短時間関与して持続的なエピジェネティックな印を残し、その後離れても変化した状態が病気を駆動し続けるのです。
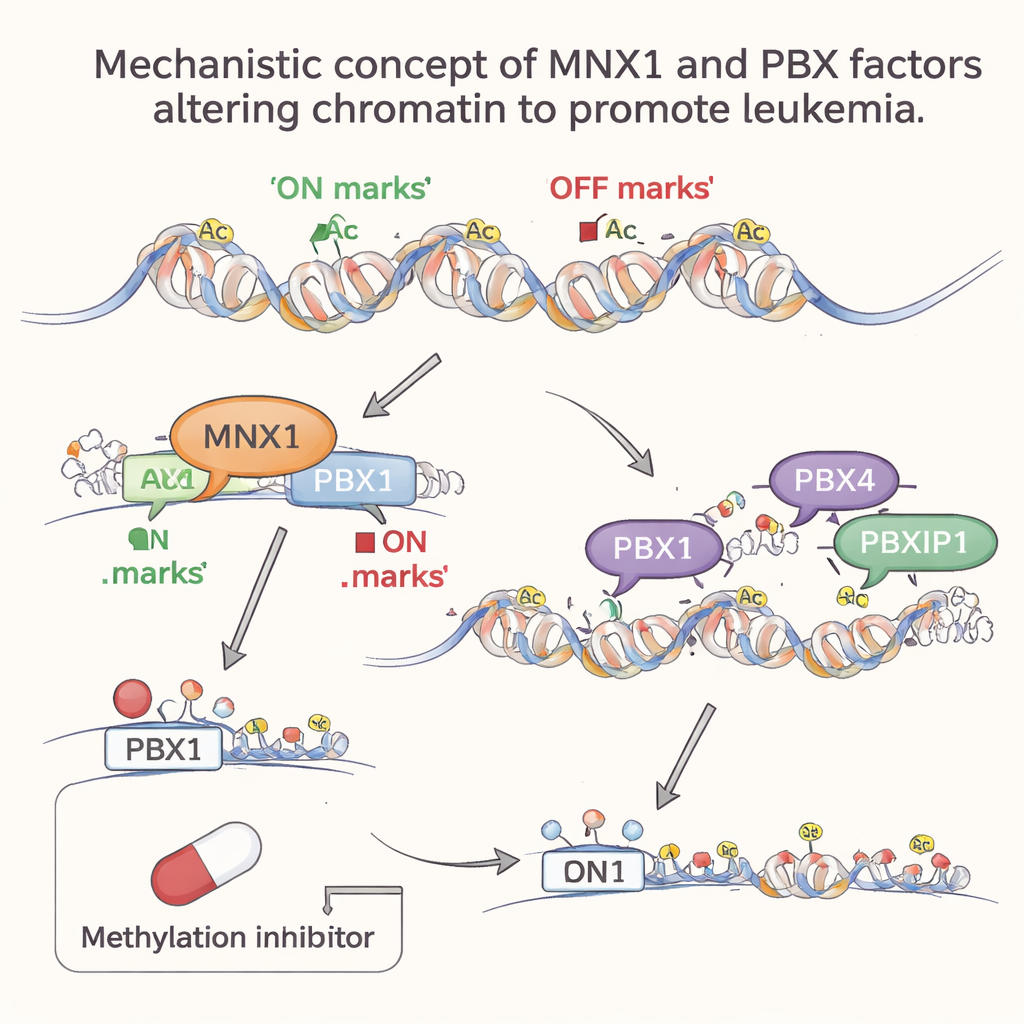
がん状態を固定するために後から加わる協力者たち
白血病が進行するにつれて、PBXファミリーの他のメンバーであるPBX4とPBXIP1がより活性化しますが、これは後期に限られます。ゲノムワイド解析は、これらの因子が好むDNA配列モチーフが、MNX1活性の結果として再構築された開いた活性クロマチン領域に強く濃縮していることを示しました。言い換えれば、MNX1がまずクロマチンの景観を再形成してPbx1をオンにし、その後PBX4とPBXIP1が新たにアクセス可能になった領域に入り込んで異常な遺伝子プログラムを強化し、細胞分裂を促進し、正常な血液分化を阻害し、DNA修復を損なうのです。この段階的な関与は分業を示唆します:PBX1はMNX1依存の早期スイッチとして働き、PBX4とPBXIP1は白血病プログラムを維持するのに寄与します。
白血病を助長する化学的印を阻む
MNX1はヒストンにメチル基を付加する酵素を介して働くため、研究チームは広範なメチルトランスフェラーゼ阻害剤であるシネファンギン(Sinefungin)がこの連鎖を妨げられるかを試しました。MNX1を発現する前白血病段階の胎児血液細胞において、シネファンギンはPbx1のレベルを鋭く低下させ、MNX1が依存するプロモーター特異的なメチル化を阻害した結果と一致しました。対照的にPBX4とPBXIP1のレベルはほとんど変わらず、これはこれらが病気の進行中に間接的かつ後期に活性化されることと整合します。これらの結果は総じて、t(7;12)を伴う乳児AMLは単なる遺伝子の破損だけでなく、MNX1が引き起こす持続的なエピジェネティック変化の連鎖によって駆動されるという強い根拠を提供します。
将来の治療にとっての意味
非専門家に向けた要点は次のとおりです。本研究は連鎖反応の地図を描きます:過剰に活性化したMNX1はDNAを包むタンパク質の化学的印を書き換え、早期にPBX1をスイッチオンし、続いてPBX4とPBXIP1が細胞を白血病状態に固定するのを助けます。これらの段階は特定のヒストンメチル化パターンに依存しているため、その印に干渉する薬剤の明確で検証可能な標的を提供します。長期的には、MNX1–PBX軸やこれらのエピジェネティックなタグを付ける酵素を標的とする治療は、この攻撃的な乳児白血病で誤った指示をオフにし、治癒の可能性を高める助けになるかもしれません。
引用: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
キーワード: 乳児急性骨髄性白血病, MNX1, PBX1 PBX4 PBXIP1, エピゲノム的ヒストンメチル化, t(7;12) 染色体転座