Clear Sky Science · ja
CDC25Cのダウンレギュレーションはミトコンドリアストレス誘導性オートファジーとアポトーシスを介して肝細胞がんの増殖を抑制する
この肝臓がん研究が重要な理由
肝臓がんは世界で最も致死率の高いがんの一つで、多くの患者は手術や標準治療が十分に効かない段階で診断されます。本研究はCDC25Cというタンパク質という単一の細胞内“スイッチ”に着目しており、これが肝がんの増殖を促進する一方で健康な肝細胞にはそれほど重要でない可能性を示しています。このスイッチの働きを低下させると、研究者らはがん細胞がミトコンドリアのストレスを受け、自身のセルフクリーニング(オートファジー)と自己破壊(アポトーシス)によって最終的に死に至ることを見いだしました。これはより選択的で有望な治療戦略を示唆します。
肝腫瘍内の増殖スイッチ
すべての細胞はいつ分裂するか、いつ止まるかを決める必要があります。CDC25Cは細胞分裂サイクルを推進する主要なタンパク質の一つです。肝がんではこのスイッチがしばしば“オン”のままになり、腫瘍の成長と転移を助けます。研究チームはマウスの肝がん細胞と正常マウス肝細胞、ならびに腫瘍をもつマウスを用いてCDC25Cの発現を人為的に低下させました。標準的な遺伝子およびタンパク質解析により、実験群でCDC25Cが対照より著しく低下していることを確認し、この増殖スイッチを下げた時に何が起きるかを研究する確かなモデルを確立しました。
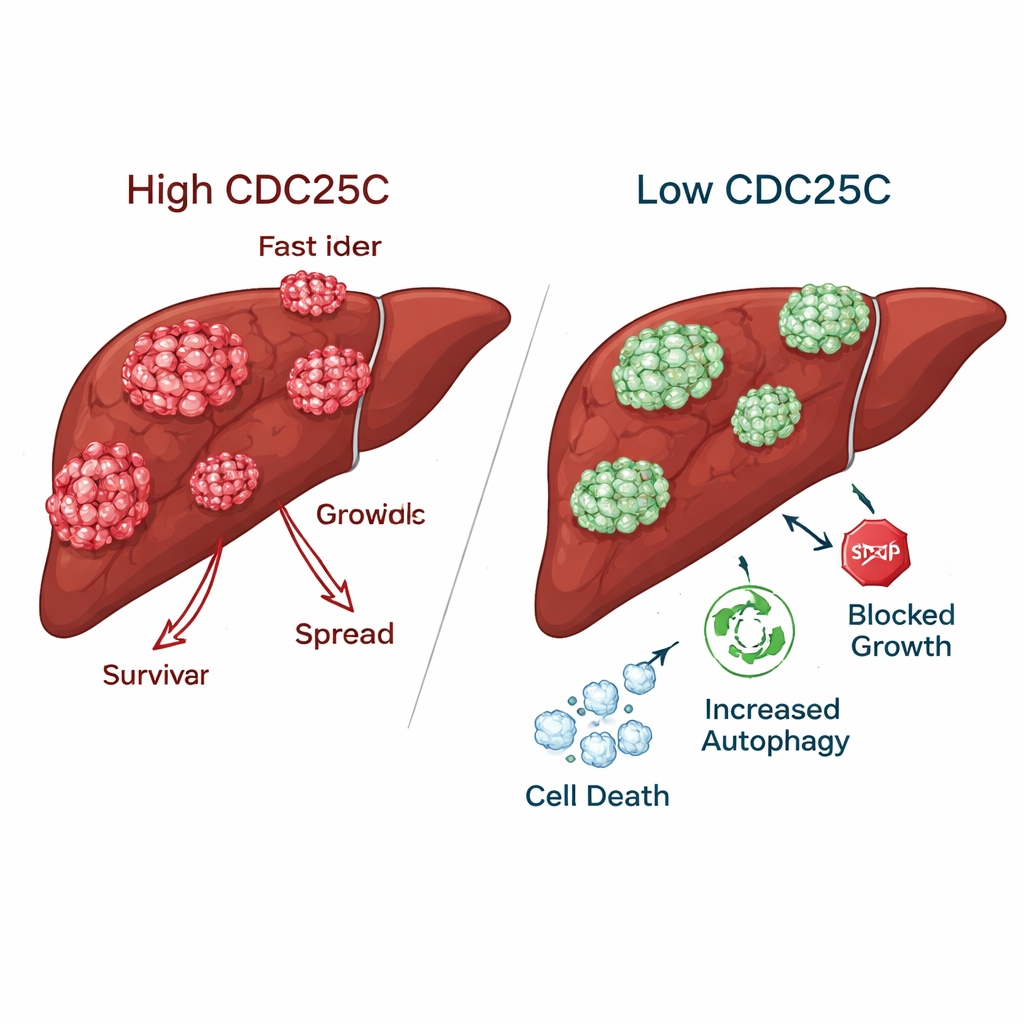
がんは抑え、健康な肝細胞は温存する
肝がん細胞でCDC25Cを低下させると、腫瘍は多くの攻撃的な性質を失いました。がん細胞はコロニー形成が大幅に減り、人工的な“創傷”上での移動が遅くなり、実験室での移動・浸潤能も低下しました。対照的に、正常肝細胞はCDC25Cを下げると成長や移動がむしろ改善する様子を示し、健康組織はCDC25C阻害を許容するか恩恵を受ける可能性が示唆されました。マウスでは、CDC25Cを低下させた腫瘍が遺伝子・タンパク質の両面でこのタンパク質の低下を示し、生体内でも同様の効果が起きることが確認されました。
エネルギー源のストレスと細胞の掃除班
電子顕微鏡で細胞内部を観察すると、CDC25Cが低下したがん細胞ではミトコンドリアが膨張・損傷し、オートファゴソームと呼ばれる泡状構造が見られ、細胞内のリサイクルシステムであるオートファジーが活性化していることが示されました。研究者らは続いてミトコンドリアストレスの主要な指標を測定しました:カルシウム濃度と活性酸素種(ROS)は、CDC25C低下後にがん細胞で上昇していました。HSP60のような補助タンパク質や二つのミトコンドリアの“品質管理”酵素など、ミトコンドリアストレス応答のマーカーも増加し、ミトコンドリアの異常をより広範な細胞応答につなげるストレス関連因子CHOPも上昇しました。注目すべきは、これらのストレスシグナルが正常肝細胞では逆方向に動いたことで、CDC25C欠損に対するがん細胞と正常細胞の応答が大きく異なることが強調されます。
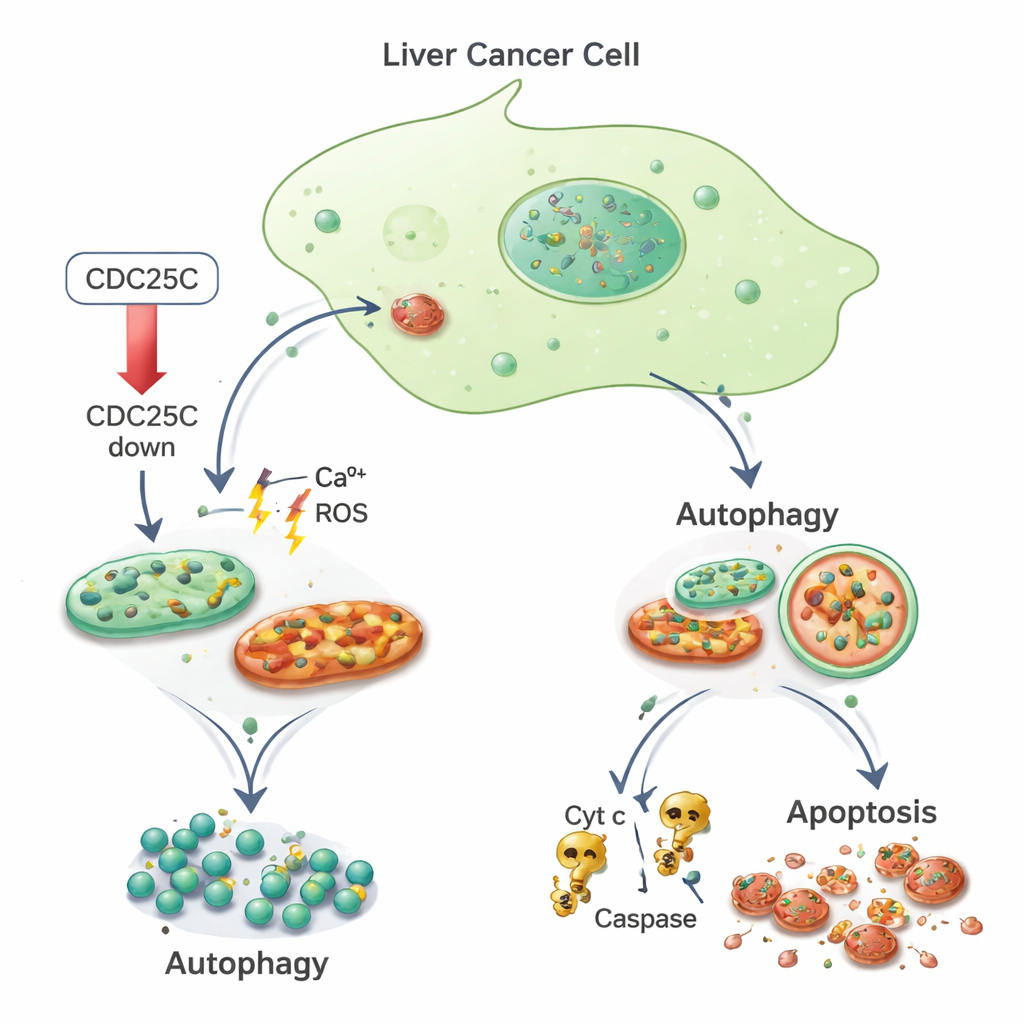
ストレスから自己消化、そして細胞死へ
次に研究チームは、これらのストレスを受けたがん細胞がどのように対処しているかを調べました。CDC25Cが低下すると、がん細胞と正常肝細胞の両方でオートファジーのマーカーが上昇しました。オートファゴソームの形成と活性を反映するLC3やp62のようなタンパク質が増加し、細胞が掃除機能を強化していることが示されました。一方で、がん細胞に限りミトコンドリア損傷が修復不能な状態を引き起こし、プログラム化された細胞死(アポトーシス)へ導いていました。蛍光染色とフローサイトメトリーを用いた解析では、断片化した明るく染まった核を持つがん細胞が増加し(アポトーシスの特徴)、ミトコンドリア膜電位が低下していました。また、シトクロムcやCaspase-3、Caspase-9といったミトコンドリア駆動の死経路の古典的構成要素の増加も確認されました。対照的に、正常肝細胞では同じCDC25C低下条件下でアポトーシスはより少なく見られました。
将来の治療にとっての意味
非専門の読者にとって重要なメッセージは、CDC25Cを低下させることが肝がん細胞の脆弱性を突き、エネルギー源を過負荷にし、リサイクルシステムを過活動に追い込み、最終的にきれいな自己破壊(アポトーシス)を誘導する一方で、主に正常な肝細胞を温存するように見える、という点です。著者らはCDC25Cが単なる増殖スイッチ以上の役割を持ち、細胞がストレス、掃除、死にどう対処するかを形作ると結論づけています。がん細胞がCDC25Cに強く依存し、その喪失に対して致命的なミトコンドリアストレスとアポトーシスで応答することから、このタンパク質やその下流のストレス経路を標的とする薬剤は、将来的に健康な肝組織への害を減らしつつより選択的に肝がんを治療する方法を提供する可能性があります。
引用: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
キーワード: 肝細胞癌, CDC25C, ミトコンドリアストレス, オートファジー, アポトーシス