Clear Sky Science · ja
γ線照射はブタ脳における筋萎縮性側索硬化症および前頭側頭型認知症マーカーの領域特異的な細胞内変化を誘導する
なぜ微少線量の放射線とブタの脳が重要なのか
多くの人は放射線を脳に対しても完全に有害なものと考えます。しかし私たちの周りには医療検査や航空機での移動、自然環境から来る低線量の放射線が常に存在します。同時に、野球選手ルー・ゲーリッグを麻痺させた致死的な病気である筋萎縮性側索硬化症(ALS)や、行動や性格を侵す近縁疾患の前頭側頭型認知症(FTD)の原因はまだ完全には解明されていません。本研究は驚くほど希望に満ちた問いを投げかけます:単回の穏やかなγ線の照射が、必ずしも単純に損傷を与えるだけでなく、ALSやFTDに関連する分子変化に対してむしろ保護的または調節的な形で脳内化学を微妙に変える可能性はあるのか?
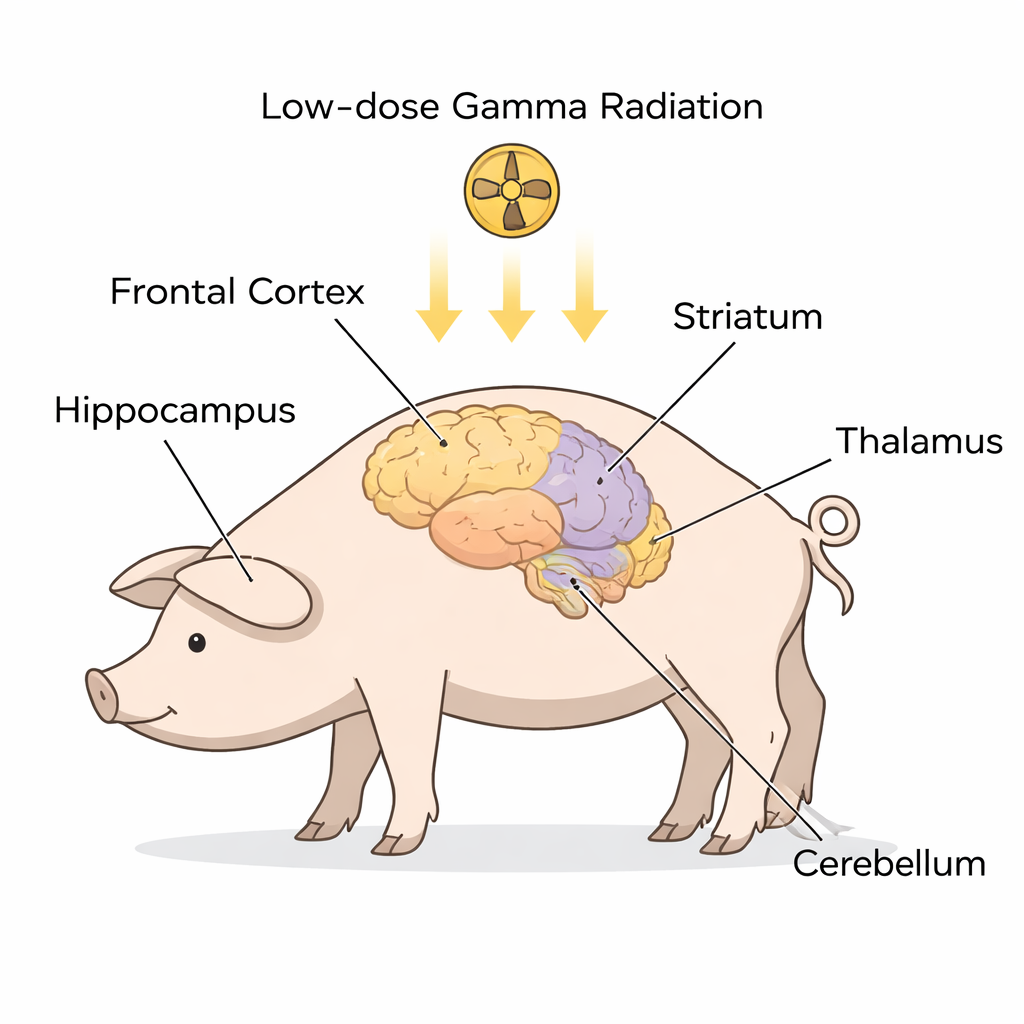
脳内のALS前兆を詳しく見る
患者ですでにALSを発症している人を調べる代わりに、研究者たちは我々の脳と解剖学的に類似したゴットンゲン・ミニブタの健康な個体を用いました。9頭は一度きりの全身低線量γ線照射を受け、6頭は麻酔のみで照射はせず対照群としました。約1か月後、研究者たちはALSやFTDと関連してしばしば議論される5つの重要な脳領域――前頭皮質、海馬、線条体、視床/視床下部、および小脳――を解剖しました。各領域で細胞内容物を主に2つの区画、細胞質(細胞の流動的内部)と核(DNAを収める区画)に分けました。ウエスタンブロットという手法を用いて、SOD1、FUS、C9orf72、STMN2、ユビキチン、TDP‑43、およびそのリン酸化型TDP‑43など、ALSやALS‑FTDに強く結びつく複数のタンパク質の量を測定しました。
放射線で変わらないマーカーと変動するマーカー
ひとつ安心できる所見は、遺伝性ALSの一部を引き起こすSOD1の総量が放射線後にいかなる領域でも変化しなかったことです。同様に、ALS関連の脳内凝集で最も頻繁に見られるタンパク質であるTDP‑43の主要な形態は、核内・細胞質のいずれにおいても全領域で安定していました。しかし、すべてが静的だったわけではありません。研究チームは他のいくつかのタンパク質について領域特異的かつ区画特異的な変化を観察しました。例えば、通常は核に存在するがALSで誤局在や凝集を起こすことがあるFUSは、視床/視床下部の細胞質で減少した一方、前頭皮質の核内レベルは上昇し、海馬では低下しました。ALSに関連するタンパク質C9orf72は細胞質では変化しなかったものの、海馬の核内で低下を示しました。神経線維の維持に重要なタンパク質STMN2も海馬核内で減少し、記憶に関わるこの領域におけるこれら二つの分子の協調した応答を示唆しています。
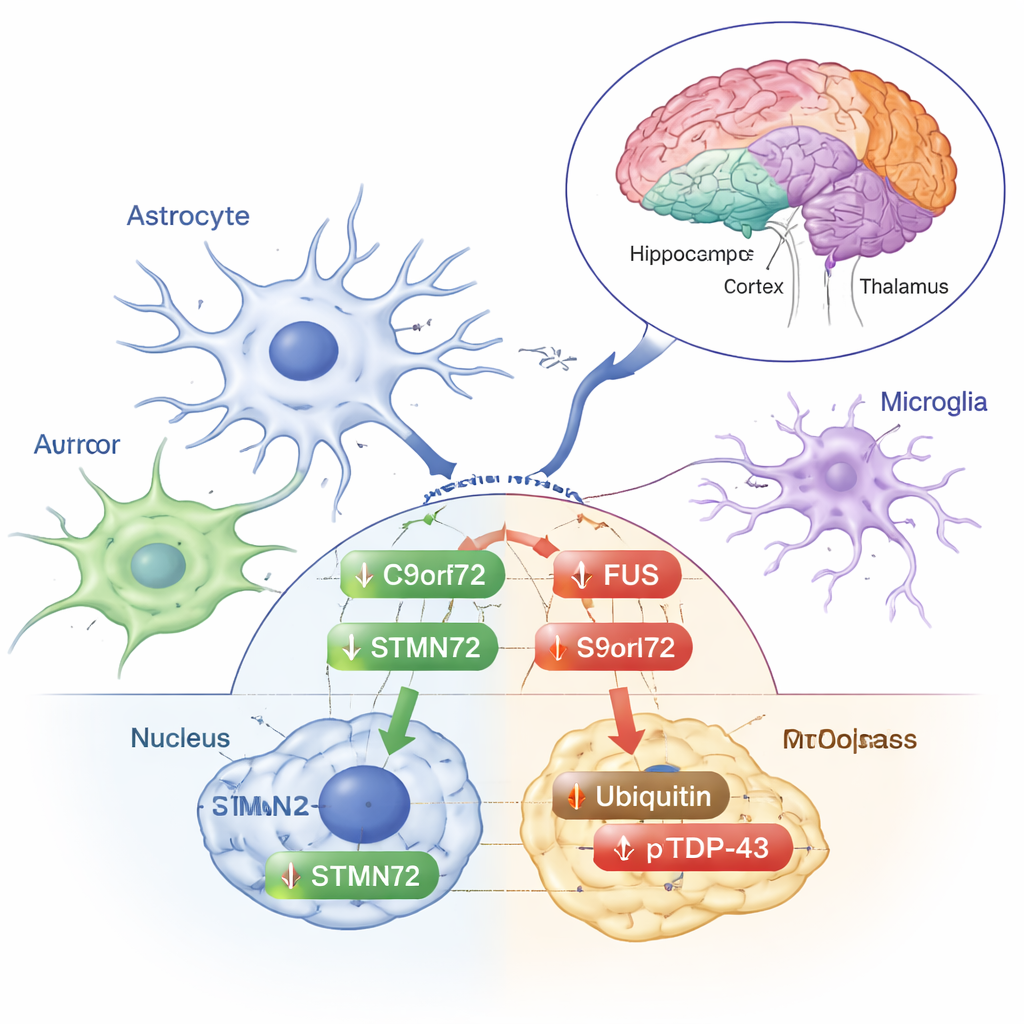
ストレスシグナルか初期の保護か?
他の変化はより古典的なストレス応答に似ていました。損傷タンパク質を除去するために細胞が付ける小さなタグであるユビキチンは、前頭皮質の細胞質画分で増加しました。TDP‑43のリン酸化型は、ALSやFTDで見られる異常沈着物にしばしば豊富に含まれる形で、総TDP‑43自体は変わらないにもかかわらず前頭皮質、線条体、および視床/視床下部の細胞質で増加しました。これらの変化は、低線量放射線が誤った折りたたみや凝集という病的パターンを引き起こすことなく、脳のタンパク質処理機構をそっと刺激することを示唆します。著者らは、これらの応答が脳領域ごと、そしてタンパク質が核内か外かによって異なることを強調しており、脳のストレス反応がどれほど精密に調節されているかを浮き彫りにしています。
ALSリスクと潜在的利益についての意味
これは低線量放射線がALSを引き起こすということを意味するのでしょうか?データは単純なイエスにはなりません。研究者たちは主要なALSタンパク質の誤局在や蓄積という特徴的な所見を観察せず、多くの変化は明白な損傷というよりは調節の変化を示していました。興味深いことに、これらの結果は同グループや他の研究者による以前の研究と整合し、少量の放射線が時に“ホルミシス”を誘導し、軽度のストレスが修復経路を活性化して、動物モデルでアルツハイマー病やパーキンソン病に関連する有害なタンパク質を減らすことがあるという現象を支持します。本研究は、少なくとも短期的には、単回の低線量γ線がALS関連マーカーを破壊的というよりは適応的に再配列する可能性を示唆しています。
大きな疑問と慎重な希望
一般読者への主要な結論は、放射線と脳の健康との関係は「放射線はすべて有害だ」という単純化した見方よりも複雑であるということです。この大型動物モデルでは、低線量のγ線曝露がALSおよびFTDに関連するタンパク質に対して微妙で領域特異的な変化を引き起こし、患者の脳で見られるような損傷パターンを再現することはありませんでした。これらの変化は脳がストレスに対処し修復しようとする試みを反映している可能性があり、場合によっては有益であることすら考えられます。ただし、本研究は単回曝露の1か月後のみを観察し、ALSが最も深刻に影響を与える脊髄は調べていません。長期的かつ反復曝露の研究がなされるまでは、人への応用を検討するべきではありません。それでも、この研究は日常レベルの放射線が壊滅的な神経変性疾患の根底にある分子とどのように相互作用するかに新たな視界を開き、慎重に制御された条件下では小線量が脳自身の防御を促すために将来的に利用される可能性を示唆しています。
引用: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
キーワード: 筋萎縮性側索硬化症, 前頭側頭型認知症, 低線量放射線, 脳タンパク質, ミニブタモデル