Clear Sky Science · ja
前立腺がん放射線療法後の白血球テロメア短縮:前向き研究
なぜこの研究ががん生存者にとって重要か
がんの生存期間は延びていますが、多くの生存者は疲労、虚弱、早めに現れる慢性疾患といった「加速した」老化のように感じられる問題を経験します。本研究はシンプルだが重要な問いを立てます:前立腺がんに対する放射線治療は、染色体の中にある私たちの基本的な老化時計に持続的な影響を残すのか?
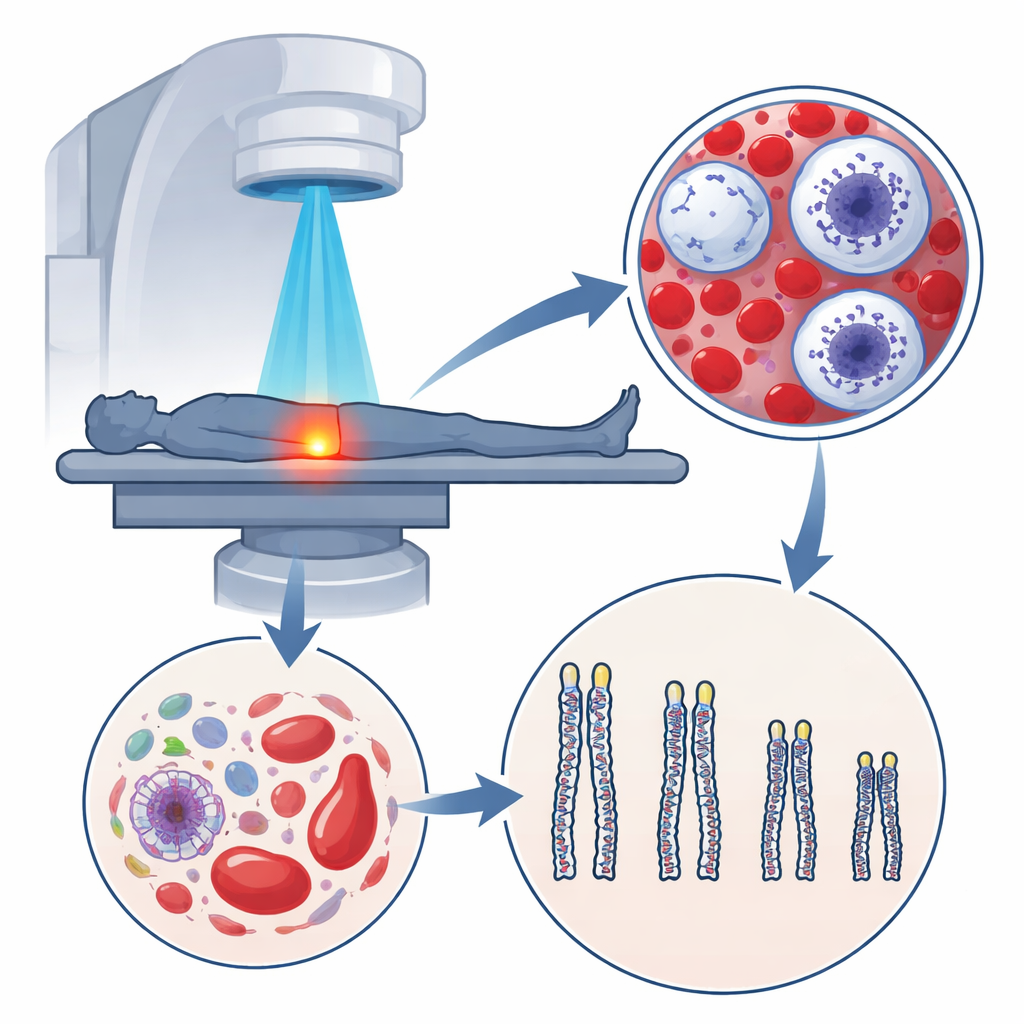
DNAを守る小さなキャップ(テロメア)
染色体の末端にはテロメアと呼ばれる小さなDNA配列があり、靴ひものプラスチックの先端のように遺伝情報のほつれを防いでいます。細胞が分裂するたびにこれらのキャップはわずかに短くなります。一定以上に短くなると、細胞は機能停止状態に入るか死に至り、これは自然な老化と結びついています。白血球は採血で容易に得られ、さまざまな組織の変化を反映するため、そのテロメア長は人生年齢とは異なることのある「生物学的年齢」を測る指標としてしばしば使われます。
治療中と治療後を詳しく追う
現代の前立腺放射線療法がこの老化の指標にどう影響するかを調べるため、研究者らは1つの医療機関で根治的放射線療法を受ける65歳以上の男性314人を追跡しました。採血は治療前、数週間にわたる放射線治療終了時、そして治療後3カ月と15カ月の計4回行われました。各サンプルで、チームは感度の高いDNA検査を用いて白血球の平均的な相対テロメア長を測定しました。このデザインにより、個々の被験者のテロメア長が時間とともにどう変化するかを追跡でき、単一の時点で異なる人を比較するだけの方法よりも変化を明確に捉えられます。
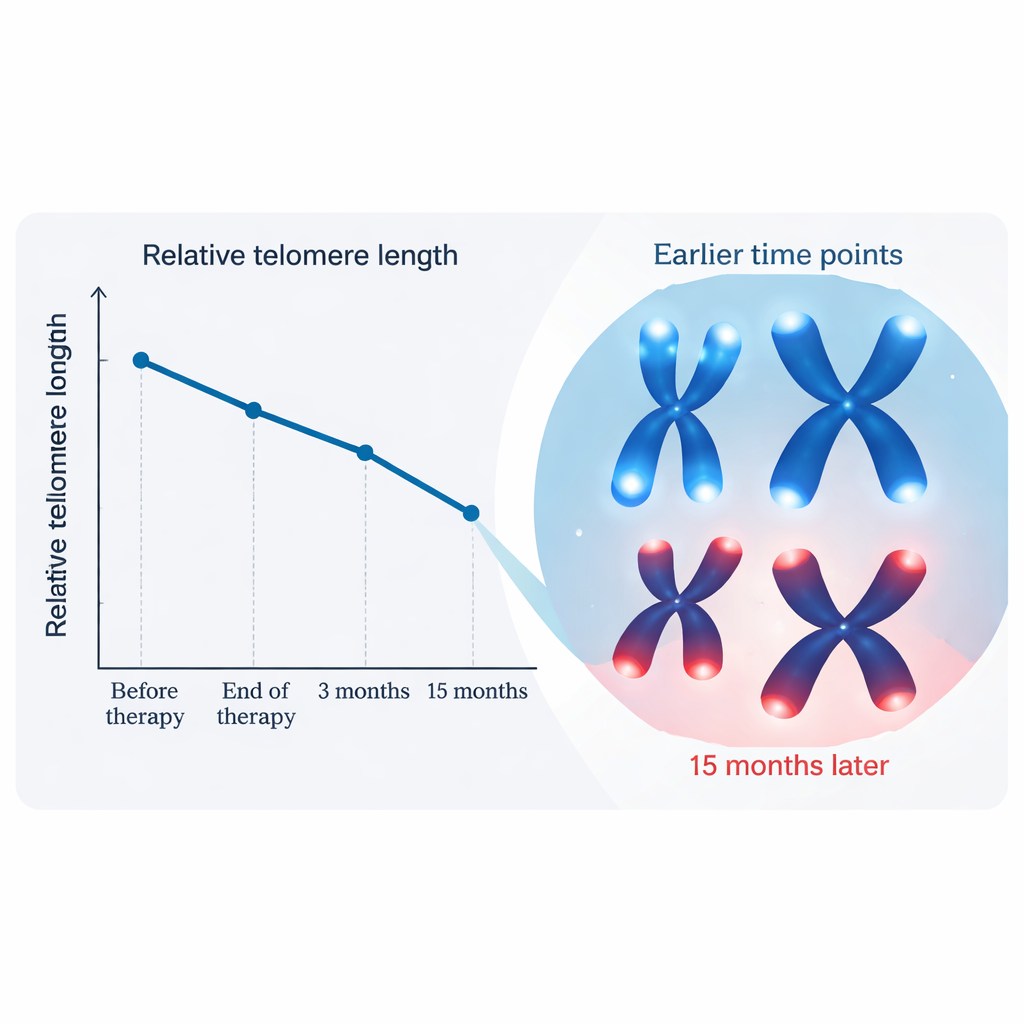
テロメアは時間とともにどう変化したか
テロメア長は治療前から放射線終了時、さらに3カ月時点までは概ね大きな変化を示さず、小さな増減は統計的に有意ではありませんでした。注目すべき変化は15カ月時点で現れました:平均してテロメアは開始時より約15%短くなっており、これは高齢者で1年余りに通常見られる加齢による短縮をはるかに上回る減少です。このパターンは、放射線が血液に与える長期的な生物学的影響が、目に見える副作用が消えた後にゆっくりと現れる可能性を示唆します。研究者らは年齢、高血圧、喫煙、治療の詳細、近傍リンパ節への照射などがこれらの変化に影響するかも検討しました。年齢と高血圧は短縮の程度とある程度関連していましたが、この集団では大半の治療の差異は明確な影響を示しませんでした。
放射線が細胞の摩耗を速めるしくみ
局所的な前立腺照射がなぜ循環する白血球のテロメアに影響を及ぼすのか。著者らは二つの連動する過程を指摘します。まず、電離放射線はDNAを傷つける反応性酸素分子を生み出し、テロメアはこの種の損傷を受けやすく、他の領域に比べて修復が効率的でないことが多いこと。次に、放射線療法は体内に持続する炎症反応を引き起こし、白血球の分裂回数を増やしてさらに酸化的副産物を放出させることがあります。これら両方の機序がテロメアの徐々の侵食を加速し、細胞を不可逆的な「老化」状態であるセネセンスへと押しやる可能性があります。セネセント細胞は分裂しなくなる一方で周囲の組織に影響を与え続けます。
患者にとって何を意味するか
この研究の男性にとって、前立腺放射線療法は根治治療であり続けましたが、同時に治療から1年後に血球での生物学的老化の加速を示す所見と関連していました。テロメアの短縮だけでその人が虚弱や疾病になると断定することはできませんが、短いテロメアは心血管疾患、糖尿病、認知低下など年齢関連の問題リスクの上昇と関連しています。これらの知見は、がん治療の成功が潜在的な長期的コストを伴うことを強調し、腫瘍制御だけでなく老化関連の健康を考慮したフォローアップケアの必要性を示しています。著者らは、非放射線治療群との比較を含むより大規模で長期の研究がこれらの結果を裏付けるために必要であり、炎症や酸化ストレスを標的にした保護的アプローチなど、治療後に患者の生物学的回復力を維持する方法を検証する必要があると主張しています。
引用: Langsenlehner, T., Paal, K., Thurner, E.M. et al. Leukocyte telomere attrition following radiotherapy in prostate cancer: a prospective study. Sci Rep 16, 5905 (2026). https://doi.org/10.1038/s41598-026-36205-x
キーワード: 前立腺がん, 放射線療法, テロメア, 生物学的老化, 細胞老化(セルラーセネセンス)