Clear Sky Science · ja
高次元ゲノムデータの精度の高い分類のためのハイブリッド深層学習フレームワーク
遺伝子データ洪水を意味ある形にする
現代のDNA解析技術は、単一の実験で数万もの遺伝子を測定でき、より早期の疾患検出やより精密な治療を約束します。しかし、この膨大なデータはノイズが多く複雑であるため、強力な計算モデルであっても信頼できる明確なパターンを見つけるのに苦労することが多いです。本稿は、こうした圧倒的なゲノムデータを扱うために特化して設計された新しいタイプの人工知能(AI)システムを紹介し、予測精度を高めると同時にその予測がどのようになされたかを説明することを目指します。
なぜゲノムデータは扱いにくいのか
ゲノム研究では、患者やサンプル数に比べてはるかに多くの測定値が得られるのが常です。これらの多くは無関係、冗長、あるいは技術的ノイズによって歪められています。従来の機械学習法は、どの遺伝子が重要かを専門家が手動で選ぶことを必要とするか、あるいはすべてを使おうとして過学習に陥りやすくなり、訓練データでは良好でも新しいケースでは失敗するリスクがあります。画像認識などで革新をもたらした深層学習は、生データから自動でパターンを学習できますが、ゲノミクスではしばしばブラックボックスのように振る舞い、正確な答えを出してもその理由がほとんど示されないため、透明性が重視される医療分野での受け入れが制限されます。
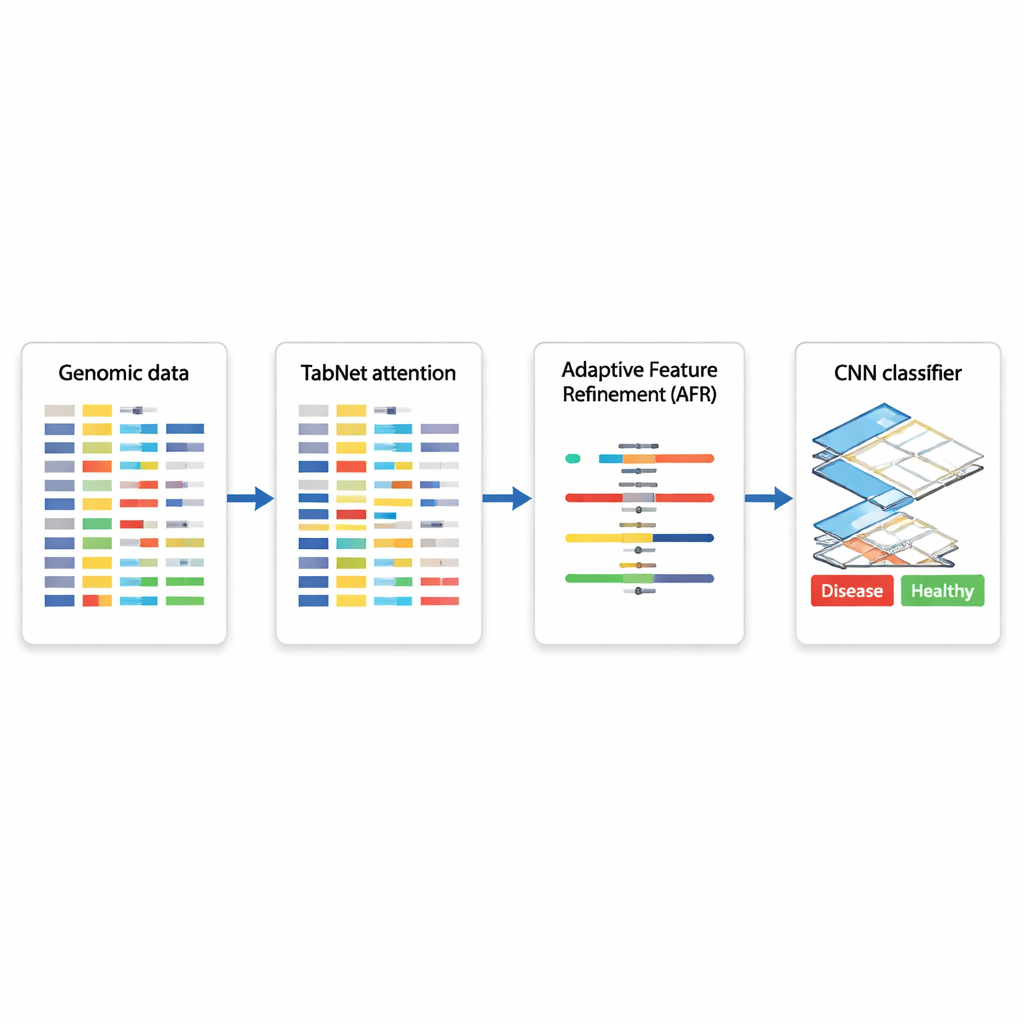
遺伝子ベースの判断のためのハイブリッドAI設計図
著者らは、三つの専門化されたモジュールを連結するハイブリッド深層学習アーキテクチャを提案します。最初に、TabNetと呼ばれるコンポーネントがスポットライトのように全てのゲノム測定値を走査し、特定の課題(例えばがん組織と非がん組織の識別)にとって最も情報を持つ特徴を学習します。すべての遺伝子を均等に扱うのではなく、TabNetは最も関連性の高いまばらなサブセットに注意を集中させます。次に、適応的特徴精緻化(AFR)層がこれら選択された信号を受け取り、それらを再重み付けして、一貫性があり意味のあるパターンを強化しつつノイズをさらに抑えます。最後に、主に画像解析で用いられる畳み込みニューラルネットワーク(CNN)が精緻化された特徴の局所的な相互作用を検出し、特定の疾患サブタイプや生物学的状態を示すような遺伝子群間の微妙な関係を捉えます。
モデルの検証
このフレームワークは三つの主要な公開データ資源で評価されました:The Cancer Genome Atlasの乳がんデータセット、Gene Expression Omnibusの単一細胞メラノーマデータセット、そしてENCODEプロジェクトのエピゲノムデータセットです。これらの集合は合わせて数千のサンプルとサンプルごとに数万の特徴を含み、遺伝子発現やDNA上の化学的標識をカバーしています。すべてのデータセットでハイブリッドモデルは幾つかの最先端手法を上回り、受信者動作特性曲線下面積(AUC)やF1スコアといった主要な分類指標で概ね5〜8ポイントの改善を示しました。重要なのは、これらの改善が透明性の犠牲を伴わなかった点です:モデルはTabNetによる注意マップとCNNによる活性化マップを生成し、各予測でどの遺伝子や領域が最も影響を与えたかを強調します。
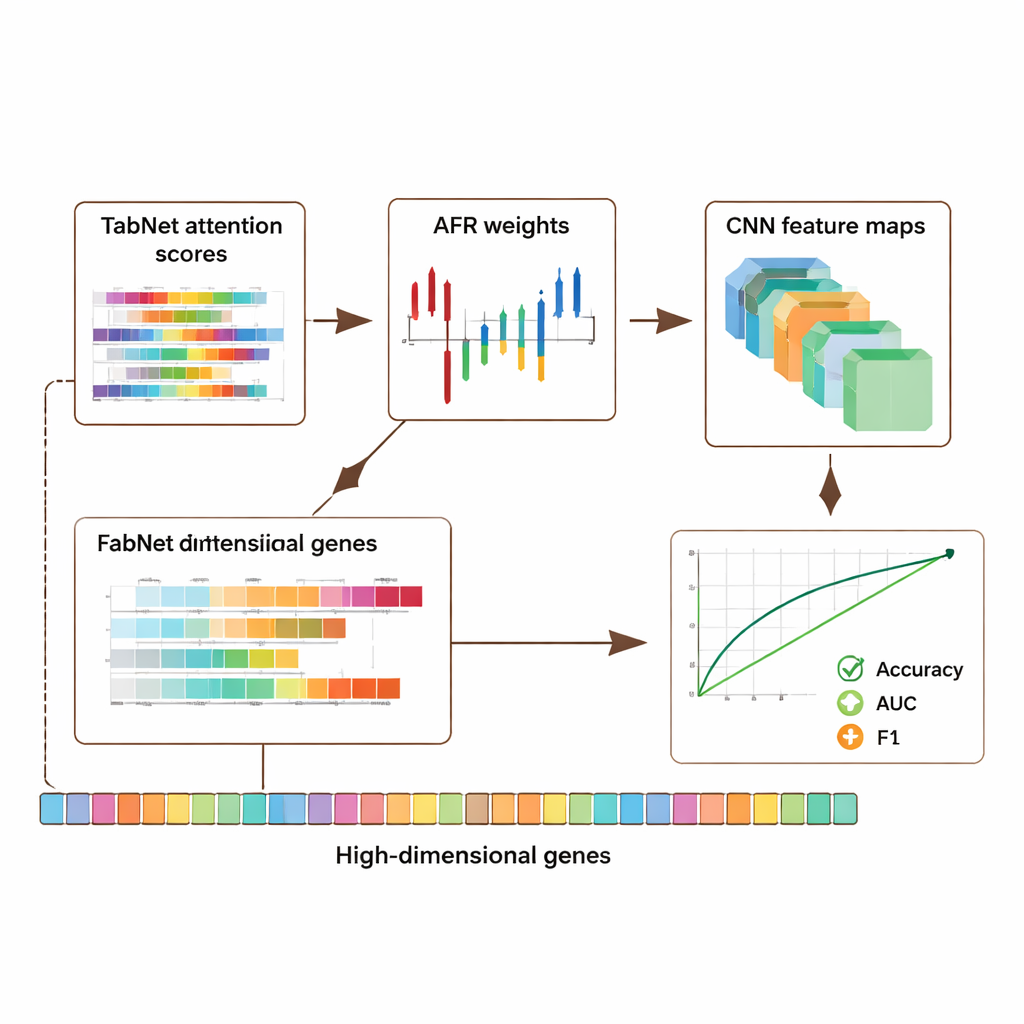
精度、プライバシー、信頼のバランス
ゲノムデータは極めて個人的な情報であるため、著者らは有用な信号を保持しつつプライバシーを保護する方法も検討しました。彼らは、感度の高い特徴にはより大きなノイズを、そうでない特徴にはより少ないノイズを加える適応的プライバシーメカニズムを導入し、選択的入力のマスキングと組み合わせました。中程度のノイズを導入した場合でも、モデルは高い精度と識別力を維持し、保護が強まるにつれて性能は段階的に劣化しました。同時に、解釈可能な注意や活性化パターンは、しばしば既にがんや免疫調節に関与すると知られる遺伝子を指し示しており、モデルが単にデータを記憶しているのではなく生物学的に意味のある信号を捉えていることを示唆します。さらに、アブレーション研究(アーキテクチャの一部を体系的に除去する実験)により、特にAFR層を含む各モジュールが性能に実測可能な寄与をしていることが確認されました。
将来の医療にとっての意義
平易に言えば、本研究は巨大なゲノム表を賢くふるい分け、疾患に関連するパターンを見つけ出す手法を提供すると同時に、どの項目が最も重要だったかを示します。ターゲットを絞った特徴選択、慎重な精緻化、そしてパターン認識を組み合わせることで、ハイブリッドモデルは予測精度を向上させ、計算面でも実行可能であり、臨床医や生物学者が解釈できる視覚的手がかりを提供します。より広く多様な患者群での追加検証は必要ですが、このようなフレームワークは新たなバイオマーカーの発見や疾患サブタイプの精緻化、精密医療における臨床意思決定ツールの支援に寄与し、DNA解析のAIを実用に一歩近づける可能性があります。
引用: Swain, M.K., Kamila, N.K., Jena, L. et al. Hybrid deep learning framework for accurate classification of high dimensional genomic data. Sci Rep 16, 5919 (2026). https://doi.org/10.1038/s41598-026-36128-7
キーワード: ゲノム深層学習, がんバイオマーカー発見, 解釈可能なAI, 精密医療, プライバシー保護ゲノミクス