Clear Sky Science · ja
フルオロキノロン骨格のR5およびR7部位がF-アクチンフィラメントの破壊を促進する
抗生物質を脳の助け手に変える
アルツハイマー病やパーキンソン病など多くの一般的な脳疾患には、共通する潜在的な犯人があります。それは神経細胞内の小さな構造的な棒状体で、時間とともに詰まり硬くなっていきます。これらの棒はアクチンというタンパク質でできており、通常は細胞内部の柔軟な足場の一部として働きます。本研究は、よく知られた抗生物質群であるフルオロキノロンを、これら有害なアクチン束を穏やかに分解するように再設計できるのではないかという意外な可能性を探ります。そうすることで脳を保護する助けになる可能性があります。
細胞の足場が誤作動するとき
健全な脳細胞は絶えず内部の骨格を再形成し、シナプス接続を作り替えます。アクチンフィラメントはこの過程の中心であり、必要に応じて形成・崩壊します。しかしストレス下では、アクチンが頑固な棒状の凝集体にロックされ、細胞を詰まらせ、重要な貨物の輸送を妨げ、アミロイドやタウといった病態関連タンパク質の蓄積を助長します。長年にわたりこれらの棒はHirano体として知られる高密度構造へと成熟し、いくつかの神経変性疾患の患者の脳でよく見られます。既存のアクチンを標的とする薬はしばしば強い毒性を示すため、研究者たちは細胞を傷つけずにこれらの凝集体をゆるめられるより安全な小分子を見つけたいと考えています。
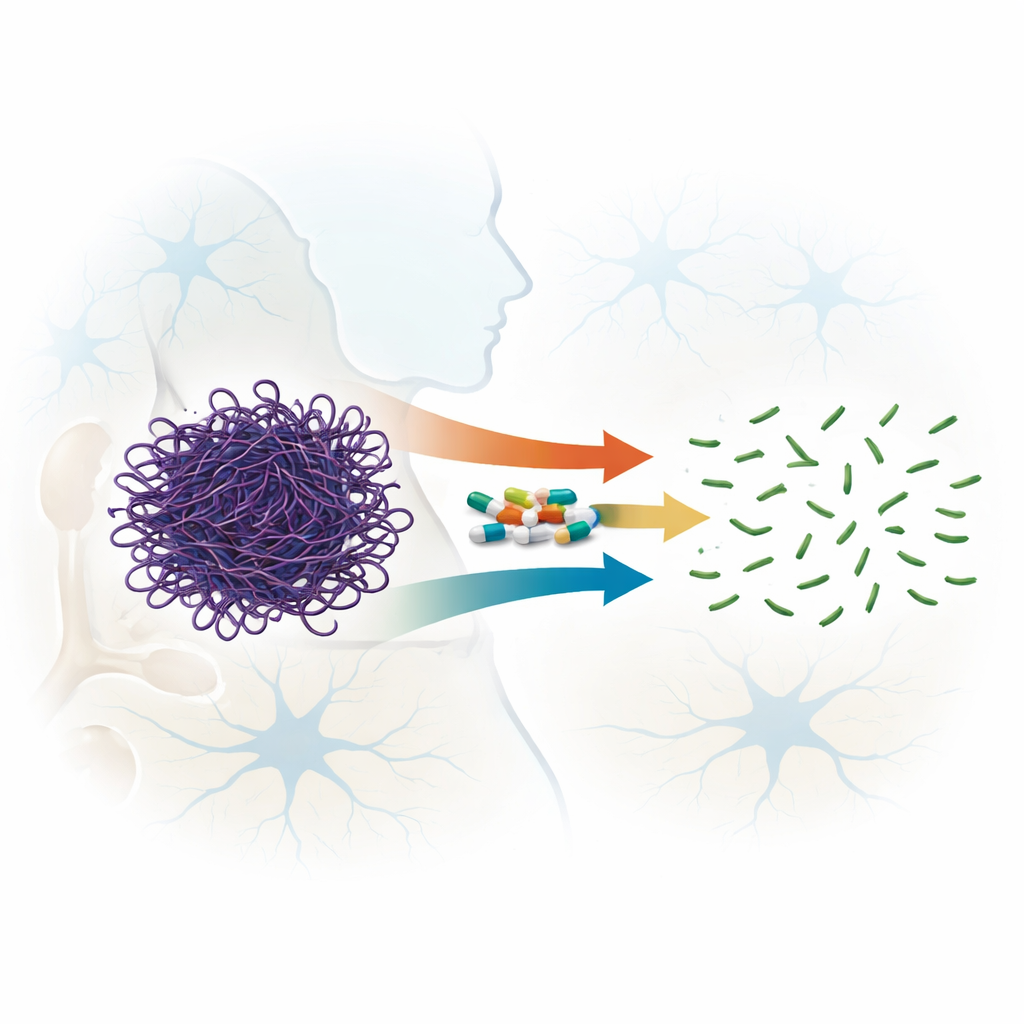
馴染みの薬の予期せぬ能力
フルオロキノロンは世界中で感染症治療に用いられる広域抗生物質で、一部の新しい系統は血液脳関門を通過することができます。以前の示唆により、特定のフルオロキノロンがアクチンフィラメントを不安定化する可能性があることが示されていました。本研究では、著者らが四つの世代にわたる関連化合物7種を系統的に比較し、フィラメントの形成を単に防ぐのではなく、既に形成されたアクチンフィラメントをどれだけ分解できるかを評価しました。光散乱測定、電子顕微鏡、およびゲル濾過を用いて、試験したすべての薬剤がアクチンフィラメントを破壊し得ることを示しましたが、その効果には大きな差がありました。特にスパルフロキサシン(第3世代)とモキシフロキサシン(第4世代)は、比較的低い薬剤対タンパク質比でも、長いフィラメントを迅速かつ不可逆的に非常に小さな断片へと切断しました。
フィラメントが崩れる様子を可視化する
高解像度イメージングと生物物理学的試験により、薬剤処理下でフィラメントがどのように変化するかが明らかになりました。電子顕微鏡では、未処理のアクチンは長く連続した鎖を形成する一方で、効果的なフルオロキノロンはこれらを短く散在した断片へと変換しました。効果の低いメンバーはフィラメントに曲がりや折れを生じさせたものの、完全には切断しませんでした。タンパク質の安定性に関する熱測定はこの物理的破壊を裏付けました。処理後のアクチンは、溶解した自由な単体に近い振る舞いを示し、融解温度が低下しましたが、その基本的な構成単位の構造はほとんど変わりませんでした。これは薬剤がアクチン自体を変性させたり破壊したりしているのではなく、主にフィラメント内でユニット同士が結びつく仕方をこじ開けていることを示唆します。
分子レベルでの結合様式を詳しく調べる
なぜ一部のフルオロキノロンが他より優れているのかを理解するため、研究チームは高度な核磁気共鳴実験と薬剤–タンパク質相互作用のコンピュータシミュレーションを組み合わせました。すべての化合物がリング状の共通“コア”を介してアクチンと接触し、特にフィラメントに繰り返し触れる二つの位置で作用することがわかりました。しかし、R5およびR7と呼ばれる特定部位に付加された余分な化学基が、各分子の結合の強さと位置に強く影響します。最も効果的な破壊剤では、これらの位置にアミノ基や嵩高い環状骨格があり、近接するアクチン鎖の界面にある小さなポケットへと到達します。そこでそれらは、フィラメントを保持する主要な塩橋を含む重要な安定化相互作用を阻害します。
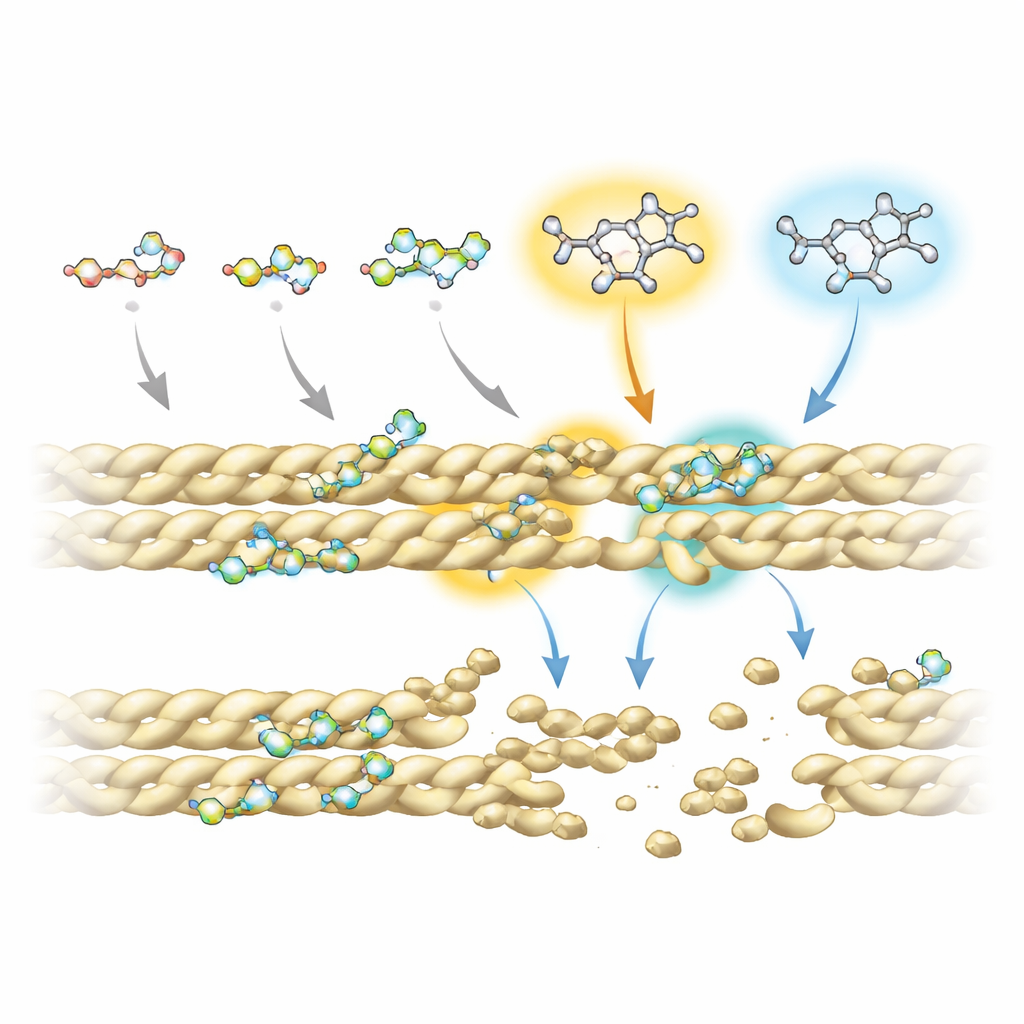
酵母細胞から将来の治療へ
研究者らは、自然にアクチン束を蓄積する酵母株でも薬剤を試験し、病的な細胞の側面を模倣しました。顕微鏡下で未処理の酵母は大きく明るいアクチン塊を示しましたが、フルオロキノロン(特にスパルフロキサシン、モキシフロキサシン、および高用量ではナリジクス酸)に曝露された細胞ははるかに拡散し点状のパターンを示し、束が分解されたことを示しました。重要なのは、薬剤の作用が比較的穏やかに見えた点です:フィラメントの詰まりを弱める一方でアクチンの基礎的な形状を大きく歪めず、結合の強さは古典的なアクチン毒素よりも弱く、重篤な副作用のリスクを低減する可能性があります。
より賢いアクチン標的薬の設計
総じて本研究は、よく知られた抗生物質にわずかな修飾を加えるだけで、それらが細胞内部の足場とどのように相互作用するかを劇的に変えられることを示しています。R5およびR7の位置を、アクチン破壊と脳浸透の両方を制御する重要な“コントロールノブ”として特定することで、著者らは有害なアクチン凝集体を選択的に分解する新しいフルオロキノロン類縁分子を創出するための設計図を示しました。これらの知見はまだ初期の実験室段階の概念実証に留まりますが、将来的に馴染み深い抗生物質を出発点として改変された薬剤が、神経細胞内の有害な足場を除去し、ある種の神経変性を遅らせるか予防する可能性を示唆しています。
引用: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
キーワード: アクチン凝集体, フルオロキノロン系抗生物質, 神経変性疾患, 薬の再適応, 細胞骨格