Clear Sky Science · ja
グラフ上の自己教師あり学習が非コードRNAと疾病の関連を予測する
見えにくいRNAが私たちの健康に重要な理由
多くの人はRNAの主な役割はタンパク質合成の助けをすることだと学びます。しかし過去10年で、タンパク質にならない「非コード」RNAが多数見つかり、それらが細胞の働きを制御することが明らかになってきました。これらの分子の多くは、がんや他の複雑な疾患を促進したり抑制したりすることが知られています。どの非コードRNAがどの病気に関連するかを突き止めれば、早期診断やより精密な治療設計の新しい手がかりになる可能性がありますが、すべての組み合わせを実験室で検証するのは現実的に不可能なほど遅い作業です。本研究は、大規模な生物学的ネットワークをふるいにかけ、実験で確かめる価値のある有望なRNA–疾病のつながりを確実に提案できる強力な計算手法を紹介します。
ゴミ扱いから主要な細胞因子へ
長年、非コードRNAは遺伝子活動の意味のない残り物と見なされてきました。現在では、マイクロRNA、長鎖非コードRNA、環状RNAなどのファミリーが、DNAの梱包から遺伝子のオン・オフ、細胞内シグナルの伝達に至る重要なプロセスを調整することが確認されています。これらは多数の制御点に位置しているため、わずかな変化でもがんや他の疾患への傾きを生む可能性があります。臨床現場でも、バイオマーカーや薬物標的として注目され始めています。課題はスケールです:RNAの種類は何千とあり、疾患も何百と存在し、それぞれの結びつきを伝統的な実験で検証するのは費用と時間がかかります。そこで計算予測が役立ち、探索領域を絞る手段を提供します。
生物学的ネットワークの読み方
これまでの計算手法は、大規模なデータ表を単純化したり、既知の例を用いて機械学習モデルを訓練したりしてRNA–疾患の結びつきを予測しようとしました。これらは有用でしたが、多くの場合RNAと疾患がネットワークとしてどのように織り合わされているかを無視していました。現代の「グラフニューラルネットワーク」は、RNAと疾患を点(ノード)として線でつながれた社会的ネットワークのように扱い、誰が誰とつながっているかのパターンを学習できます。しかし、多くのグラフ手法は信頼できる訓練データと精巧に設計された入力特徴を大量に必要とします。そのため、欠測データやノイズの多い測定、過学習に弱く、既知データでは良い性能を示しても新しい関連を予測する際に失敗しがちです。
データ自身から学ぶ
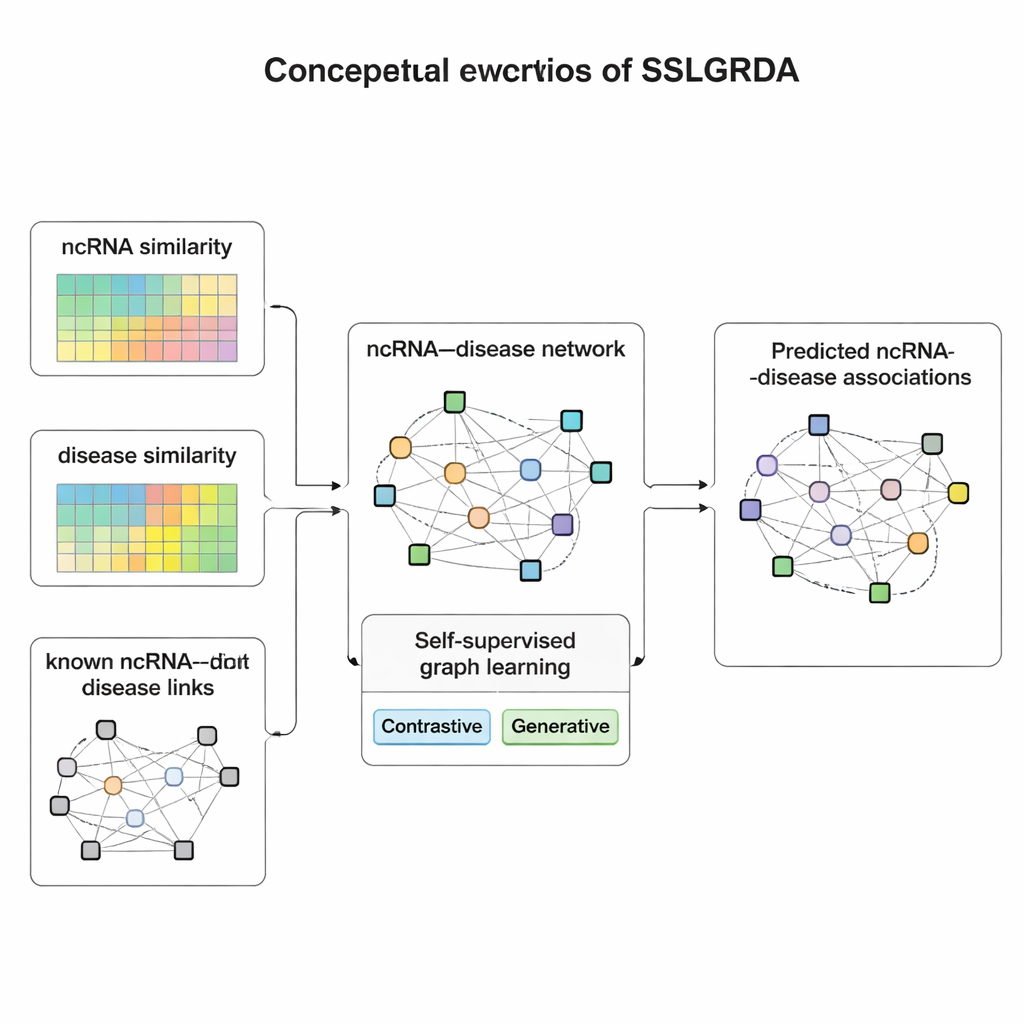
著者らはSSLGRDAという新しいフレームワークを提示し、ラベル付き訓練データに過度に依存せずにグラフモデルに有用なパターンを学習させます。鍵となる考え方は「自己教師あり学習」です:どのRNAがどの疾患に対応するかを与えられる代わりに、モデルはネットワークの構造や属性だけに基づいて自分で練習課題を作り出します。研究者たちは二種類のグラフを構築します。ひとつはRNAと疾患を異なるノード型として既知のリンクでつなぐグラフ、もうひとつはそれらを混合して同種ノードの類似性情報(例えば二つのRNAや二つの疾患がどれだけ似ているか)も含む単一の大きなネットワークにしたものです。後者により、つながりが希薄な項目にも近縁のノードが補助的に加わります。これらのグラフ上で、SSLGRDAは二つの自己学習様式を使います。コントラスト学習は同じノードの異なる「ビュー」(例えば接続関係と属性)が似た内部表現をもつべきであり、無関係なノードとは明確に分離されるべきだとモデルに学習させます。一方、生成的手法は入力特徴の一部を意図的に隠してそれを再構築させることで、ノイズの丸暗記ではなく深い構造を捉えるよう促します。
手法の検証
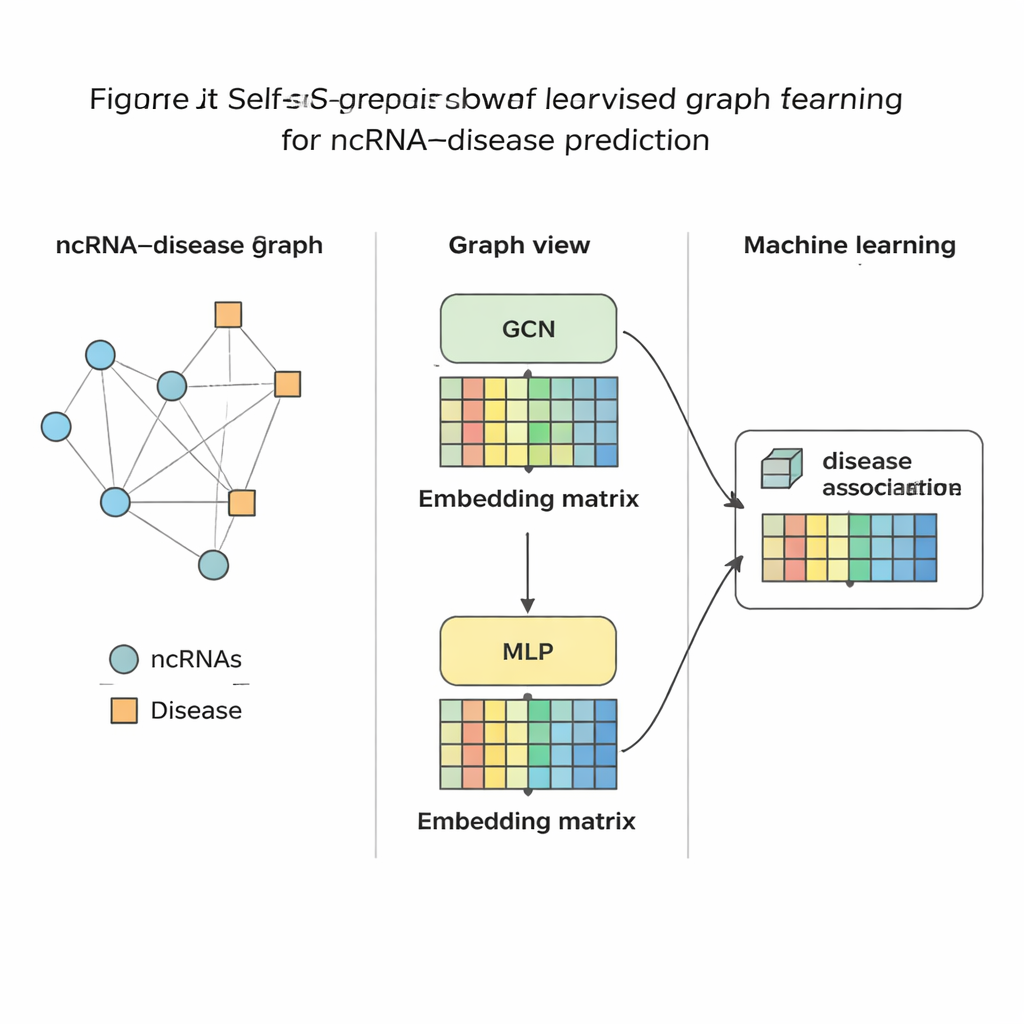
SSLGRDAが各RNAと疾患をコンパクトな数値フィンガープリントに蒸留した後、標準的な機械学習分類器を訓練してそれらの間にリンクがあるかどうかを判定します。著者らは三つの主要なRNAタイプと何百もの疾患を含む9つの異なるデータセットでこの手法を評価しました。結果として、混合(同種化)グラフ上のコントラスト自己教師あり変種が全体的に最良の成績を示し、強力なグラフベースの既存手法を含む複数の競合手法を上回りました。この手法はグローバルな精度で高い性能を示しただけでなく、個々のRNAや個々の疾患に焦点を当てたときにも正しい相手を上位にランク付けする能力がありました。これは、生物学者が特定のがんから出発してどのRNAを研究すべきかを尋ねる実用場面で重要です。さらに、同じ考え方が微生物と疾患や薬物を結ぶ他の生物医学ネットワークにも良く適用できることを示しました。
予測から潜在的治療へ
実用価値を示すために、チームはSSLGRDAを用いて乳がん、結腸がんなど複数の状態に関与する新たな非コードRNAを探索しました。上位にランクされた多くの提案は独立したデータベースや科学報告で後に確認され、モデルが生物学的に意味のあるパターンを見出す能力を裏付けました。専門外の読者への要点は、この研究が増え続ける生物データのもつれから隠れた疾病の手がかりを掘り出すより賢い方法を提供するということです。自己教師ありグラフ手法(SSLGRDAのような)がRNAと疾患のクラスタリングや相互作用を自動的に学習することで、実験室の研究者をもっとも有望な標的へ導き、生データからより良い診断や治療への道を短縮する可能性があります。
引用: Wu, Q., Tang, S. Self-supervised learning on graphs predicts non-coding RNA and disease associations. Sci Rep 16, 5231 (2026). https://doi.org/10.1038/s41598-026-36030-2
キーワード: 非コードRNA, 疾病関連, グラフニューラルネットワーク, 自己教師あり学習, 計算生物学