Clear Sky Science · ja
細菌プロテオームにおける分子圧密がタンパク質安定性に与える影響
なぜタンパク質の「混雑した生活」が重要なのか
生きた細胞の内部では、タンパク質はほかの分子で非常に混み合った空間の中で働いており、体積のほぼ半分が占有されることさえあります。ところが多くの実験は希薄でほとんど何も入っていない溶液中でタンパク質を調べます。本稿は単純だが重要な問いを投げかけます:このような混雑した現実はタンパク質の安定性や振る舞いをどのように変え、それが分子レベルでの生命活動にとって何を意味するのか?
混み合った細胞世界をのぞく
これを調べるために研究者たちはCupriavidus necatorという細菌を用いました。これは炭素回収やバイオプラスチック生産などのグリーン技術で注目される微生物です。研究者らは細胞を丁寧に破砕し、数百種類のタンパク質をできるだけ自然に近い状態で保持しました。次に、細胞内部の高密度さを模すためによく使われる大きな親水性高分子—PEG、デキストラン、Ficoll といった一般的な“圧密試薬”を高濃度で加えました。
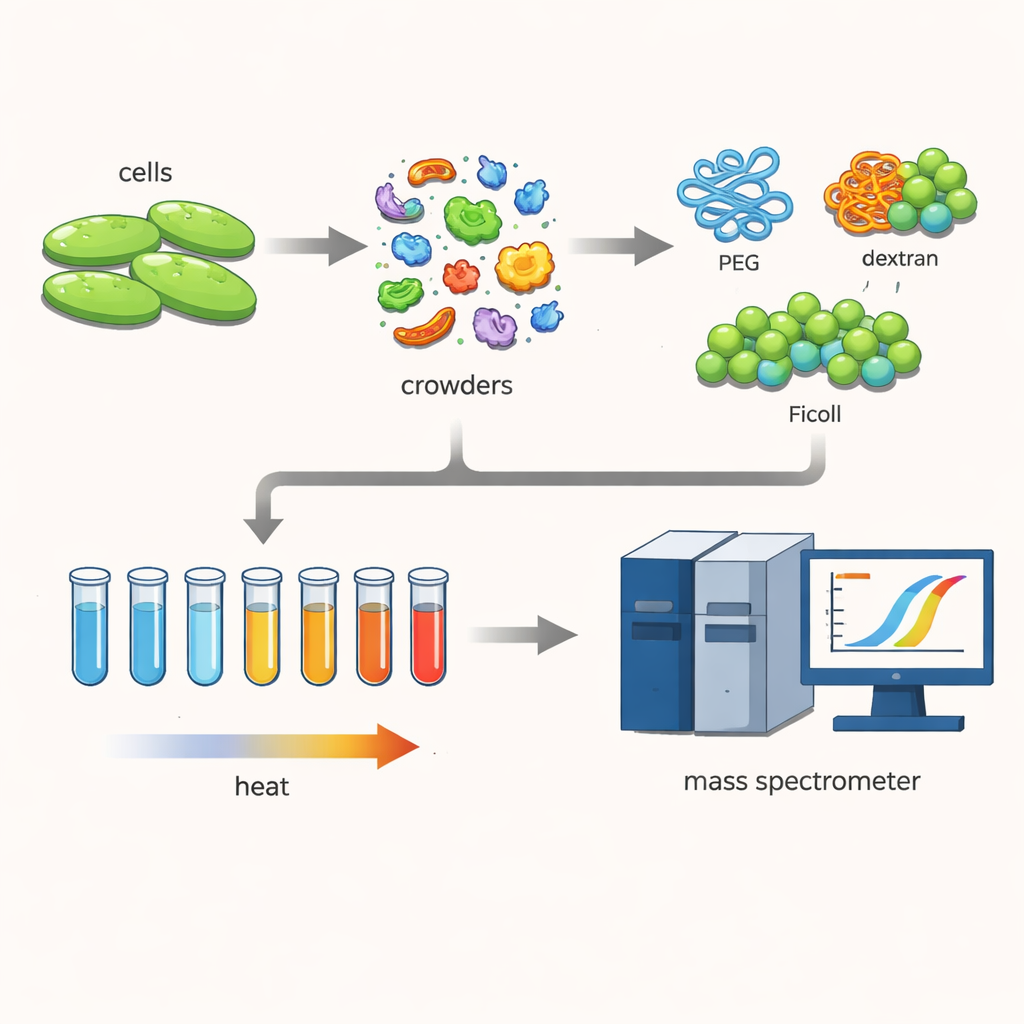
タンパク質の“溶け具合”を観察する
チームは熱プロテオームプロファイリングと呼ばれる手法を用いました。彼らはタンパク質混合物の多数の小さなサンプルを段階的に30度から70度まで加熱しました。温度が上がると、安定性の低いタンパク質は変性して凝集し、溶液から除かれていきます。残存する可溶性タンパク質をタグ付けして高感度の質量分析計で測定することで、各タンパク質の溶解曲線を再構築し、半分が可溶性の働く状態を離れる温度、すなわち融点を決定できました。圧密試薬の有無でこれらの温度を比較することで、混雑した環境がタンパク質の安定性をどのように変えるかが明らかになりました。
入り混じった結果:安定化するタンパク質もあれば不安定化するものも
全体としては、6種類の高分子圧密剤のいずれかを加えると細菌プロテオーム全体の融点は下がる傾向があり、わずかな全体的な不安定化効果を示しました。しかしこの全体傾向はもっと微妙な事情を覆い隠していました。数十種類の個別タンパク質では、圧密剤が明確に安定化あるいは不安定化を引き起こし、変化は時に数度にも及びました。ほとんどのタンパク質は6つの試薬のうち1つにしか影響されませんでしたが、ごく一部は複数の試薬に反応し、それらの多くは一貫して安定化されるか一貫して不安定化される傾向があり、圧密剤との相互作用に共通する特徴があることを示唆しています。
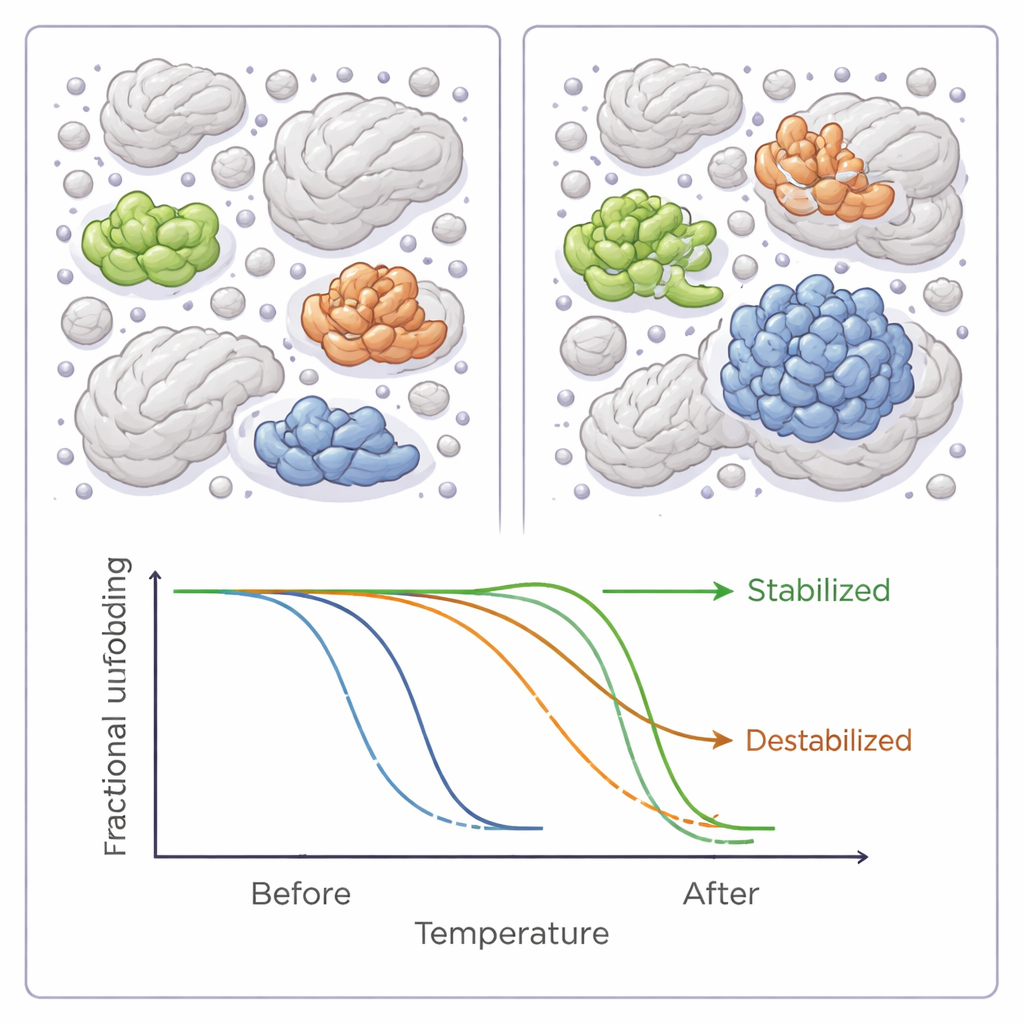
混雑の中で勝ち組・負け組を分けるもの
感受性の高いタンパク質の性質を詳しく調べると、いくつかのパターンが浮かび上がりました。混雑条件でより安定になるタンパク質は、より疎水性(つまり水をはじく表面が多い)である傾向があり、明確な活性部位を持つ古典的な酵素であることが多かったです。またタンパク質間相互作用に関与することが多く、機能を調節する化学修飾を受けていることもありました。一方で不安定化されるタンパク質は平均すると小型で、そのような修飾も少ない傾向がありました。これらの発見は、混雑がタンパク質の大きさや形、通常のパートナーとの相互作用の仕方によって一部を有利にし、他を脆弱にするという計算機モデルや他の実験結果と一致します。
単なる圧迫以上:圧密剤は本当にどう作用するのか
分子圧密の従来の説明は「除外体積」に着目します。つまり大きな分子が空間を占めるため折りたたんだ状態が有利になるという考えです。もしそれだけが全てなら、圧密剤は主にタンパク質を安定化し、高分子のかさ高さや粘性と強く結び付くはずです。しかし著者らは高分子の大きさや粘度との関連は弱いことを観察しました。彼らのデータはむしろ「優先的排除」の図式に適合します:圧密剤とタンパク質が化学的に互いを避けることで、間接的に特定の折りたたみ状態を有利にする一方、他のタンパク質の微妙な相互作用を乱すこともあるというものです。要するに、単なる物理的な圧迫だけでなく、化学的な押し引きがタンパク質の振る舞いを形作っているのです。
生命の化学を理解する上での意義
専門外の読者にとっての要点は、細胞内のタンパク質は透明なバッファー中で孤立して調べるだけでは決して完全に理解できない、ということです。周囲の密な分子ジャングルは、あるタンパク質をより頑丈にし、別のものをより脆弱にし、反応ネットワーク全体の振る舞いを変え得ます。本研究は数百のタンパク質の安定性変化を同時に測定することで、圧密効果が複雑でタンパク質ごとに異なり、単純な詰め込み効果だけでなく直接的な相互作用によっても駆動されている可能性が高いことを示しています。薬剤設計、工業用酵素、あるいは設計微生物を開発する際には、この「混雑した現実」を認識することが、生体内でタンパク質が実際にどのように振る舞うかを予測する上で重要になるでしょう。
引用: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
キーワード: 分子圧密, タンパク質安定性, 熱プロテオームプロファイリング, 細菌プロテオーム, 細胞内環境