Clear Sky Science · ja
統合型単一細胞解析と機械学習フレームワークが予後を示す線維芽細胞サブタイプを明らかにし、肺腺癌における線維芽細胞関連リスク署名を構築する
肺腫瘍周辺の「助っ人」細胞が重要な理由
肺腺癌は最も一般的で致命的な肺がんの一つですが、見た目が似た腫瘍でも患者ごとに経過や治療反応が大きく異なります。本研究はがん細胞そのものを超えて、組織の構築と再編成に関与する周囲の「助っ人」細胞、すなわち線維芽細胞に着目します。これらの細胞を一つずつ精密に観察し、高度な計算モデルを組み合わせることで、線維芽細胞には患者の予後や最新の免疫療法への反応を予測する異なるタイプが存在することを示しています。
腫瘍近傍の詳細な観察
最先端の単一細胞RNAシーケンシングを用いて、研究チームは治療前の肺腺癌サンプルから14万を超える個々の細胞を解析しました。この手法は各細胞でどの遺伝子が発現しているかを読み取り、腫瘍を主要な居住者――免疫細胞、がん細胞、血管細胞、線維芽細胞――に分類することを可能にします。解析の結果、腫瘍はそれぞれの細胞型の比率において大きく異なることが明らかになりました。免疫細胞で満たされた腫瘍もあれば、線維芽細胞や構造組織が優勢な腫瘍もあります。追跡解析により、これらの各細胞型が免疫応答の指揮から腫瘍の構造的足場の構築まで、専門的な役割を担っていることが示されました。
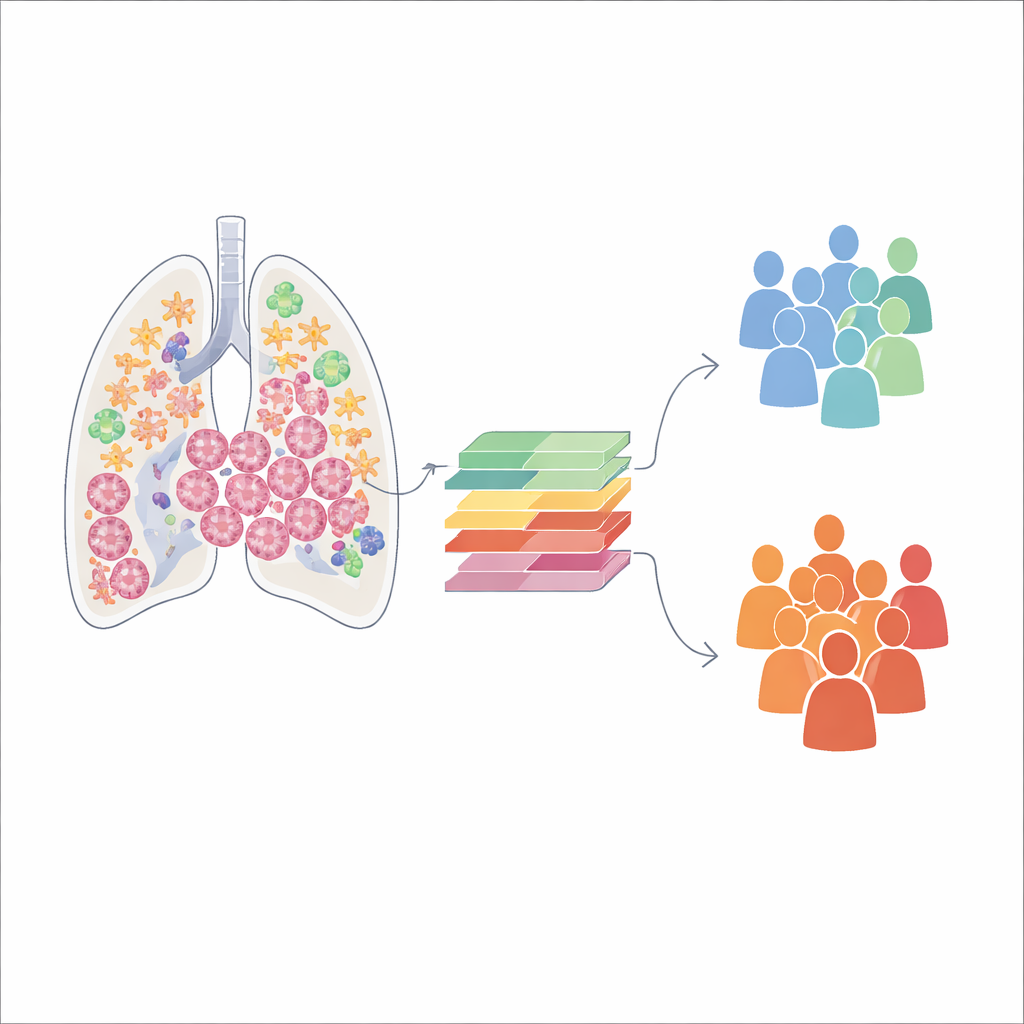
すべての線維芽細胞が同じではない
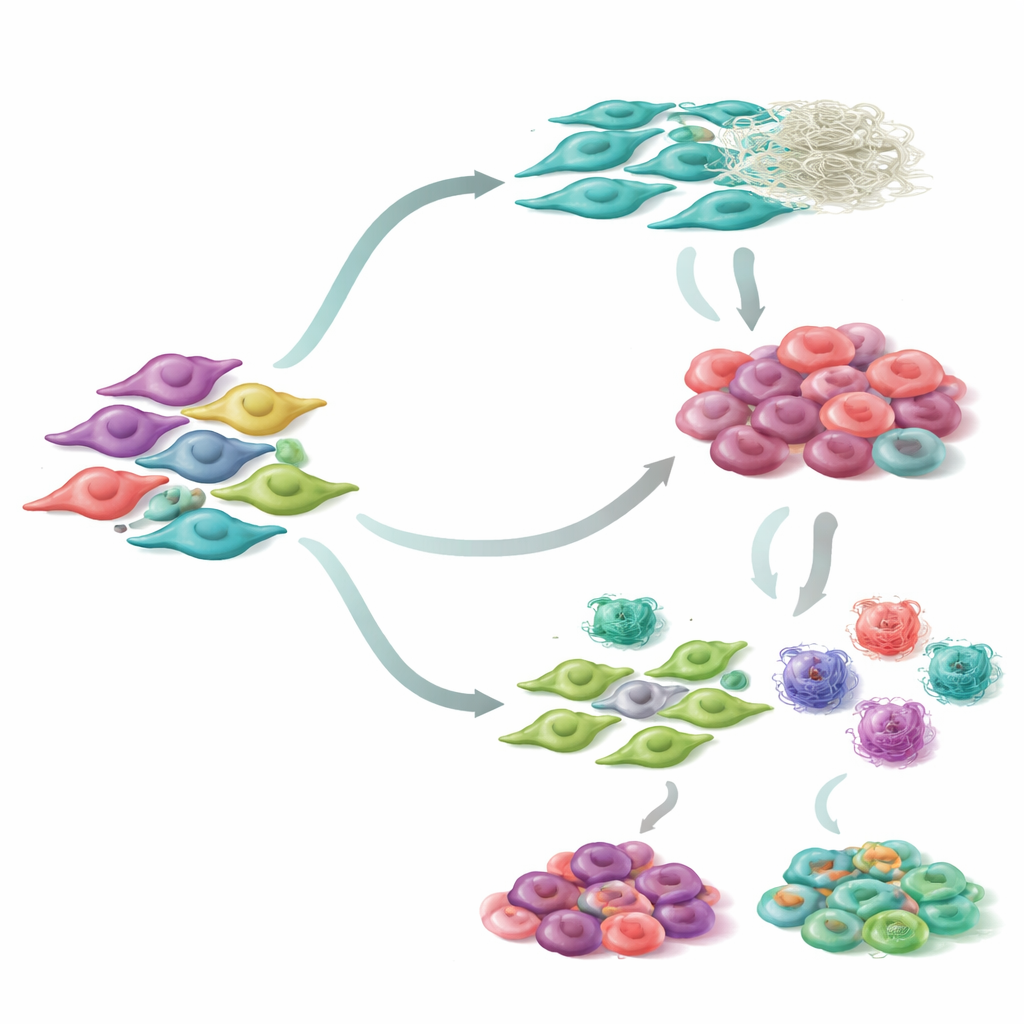
線維芽細胞に焦点を絞ると、研究者らは肺腫瘍内に7つの明確な線維芽細胞サブグループを同定しました。これらの細胞が時間とともにどのように変化するかを再構築すると、主に二つの発生経路が観察されました。一方の経路では、線維芽細胞が徐々に収縮性や組織硬化を引き起こす性質を帯び、腫瘍周囲の環境を再形成します。もう一方では、線維芽細胞が免疫系との相互作用に関与し、免疫細胞を引き寄せたり抑制したりします。各サブグループは遺伝子発現パターンが独特で、筋様の収縮、移動、免疫調節など異なる生物学的役割と結びついていました。重要なことに、特定の線維芽細胞サブタイプが豊富な腫瘍を持つ患者は生存期間が長い傾向があり、線維芽細胞状態の組成は単なる興味深い現象にとどまらず臨床的な結果と関連していることが示されました。
線維芽細胞シグナルからリスクスコアを構築する
これらの生物学的知見を臨床で役立てるために、研究チームは単一細胞データから得られた線維芽細胞マーカー遺伝子を、何百人もの患者を含む大規模公開データのバルク腫瘍データと組み合わせました。次に10種類の機械学習手法を駆使し、101のモデル組み合わせを検証して、どの線維芽細胞関連遺伝子の組み合わせが患者生存を最もよく予測するかを探しました。最良モデルとして得られた線維芽細胞関連署名(fibroblast-related signature、FRS)は29遺伝子を用いて各患者にリスクスコアを割り当てます。主要データセットおよび6つの独立コホートにおいて、FRSが高い患者は一貫して生存率が低いことが示されました。FRSは年齢、性別、腫瘍ステージを考慮しても依然として強力な予測因子であり、標準的なTNM分類と組み合わせることで予測精度が向上しました。
免疫回避と治療反応の手がかり
多くの患者が免疫療法を受ける現在、著者らは線維芽細胞ベースのスコアが腫瘍の免疫環境の特徴を捉えているかを検討しました。低FRSスコアの腫瘍は、CD8陽性T細胞やナチュラルキラー細胞などのがんと戦う免疫細胞の浸潤が豊富であり、腫瘍断片を免疫系に提示する遺伝子の発現も高いことが分かりました。一方、高FRS腫瘍は有益な免疫細胞が少なく、腫瘍細胞割合が高く、遺伝的不安定性が大きく、免疫排除の兆候、すなわち免疫細胞が排除されている様相を示していました。免疫チェックポイント阻害薬への反応を模擬する指標は、低FRS患者がこれらの療法でより利益を得やすく、高FRS患者は抵抗性である可能性を示唆しました。
有望な標的遺伝子の強調
FRSを構成する遺伝子群の中で、研究チームはTIMP1という遺伝子を予後不良の強いマーカーとして特に注目しました。TIMP1は多くのがん種で高発現を示し、正常肺組織と比べて肺腺癌組織で特に高く発現していました。実験室の検討では、肺がん細胞株でTIMP1の発現を下げると、基質を越えて侵入する能力や新しいコロニーを形成する能力が低下し、TIMP1が腫瘍増殖や転移を促進していることが示唆されました。これらの結果は、腫瘍の構造的および免疫調節的な機能を弱めることを目的とした将来の薬剤の候補標的としてTIMP1を指し示しています。
患者にとっての意味
本研究は、肺腫瘍の周囲にいる補助的な細胞――とりわけ線維芽細胞――が、病勢の挙動や治療反応に関する貴重な情報を保持していることを示しています。単一細胞計測と機械学習を組み合わせることで、著者らは患者を高リスク群と低リスク群に分け、どの腫瘍が免疫療法に抵抗しやすいかについての手がかりを与える線維芽細胞ベースのリスクスコアを作成しました。こうしたスコアが日常診療で用いられる前にはさらなる検証が必要ですが、本研究は肺がんを効果的に治療するにはがん細胞自体を攻撃するだけでなく、腫瘍の成長と隠蔽を助ける周囲の線維芽細胞も制御する必要があることを強調しています。
引用: Cheng, S., Zhang, H., Mu, Q. et al. Integrative single-cell and machine learning framework reveals prognostic fibroblast subtypes and constructs a fibroblast-related risk signature in lung adenocarcinoma. Sci Rep 16, 7965 (2026). https://doi.org/10.1038/s41598-026-35830-w
キーワード: 肺腺癌, がん関連線維芽細胞, 単一細胞シーケンシング, 腫瘍微小環境, 免疫療法反応