Clear Sky Science · ja
制御された機械的応力がヘテロな肺がん細胞の狭いチャネルへの移動を促進し、狭所を移動した細胞が形成する腫瘍スフェロイドの増殖を調べる
なぜがん細胞の「絞り込み」が重要なのか
がんは開けた空間で散らばるわけではありません。腫瘍細胞が発生部位を離れる際には、組織や血管壁、その他の込み入った構造の小さな隙間を押し通らなければなりません。本研究は単純だが強力な問いを投げかけます:混ざり合った肺がん細胞の集団の中で、実際にこうした狭い場所を通り抜けるのはどの細胞か、そしてそれらは後にどのような腫瘍を作るのか。答えは、なぜ一部のがん細胞がより危険なのかを説明し、転移を予測したり遅らせたりする新たな方法の指針となり得ます。
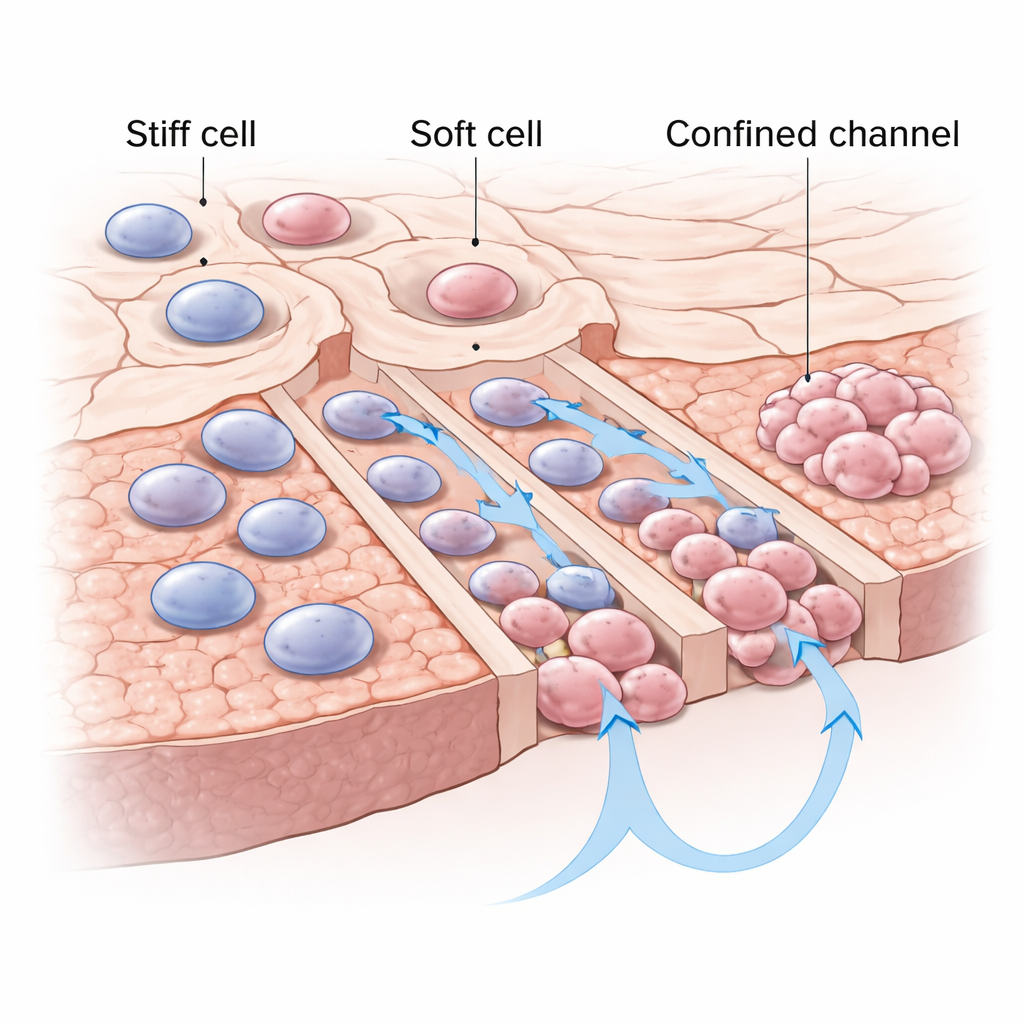
狭い空間では柔らかい細胞が有利
著者らは多くの人が聞いたことのない細胞の物理的特性、すなわち「剛性」に注目しました。がん細胞の中には比較的硬いものもあれば、柔らかく変形しやすいものもあります。幅が典型的な細胞よりも狭いチャネルを刻んだ特殊なマイクロ流体チップを用い、個々の肺がん細胞を狭い(閉所)と高くて開いた(非閉所)チャネルの入り口に配置しました。24時間後、単一細胞はより多くが狭く閉ざされたチャネルを選び、そこでより速く移動していることが分かりました。原子間力顕微鏡(ナノスケールの“指”のような装置)で後から細胞の力学特性を調べると、閉所を移動した細胞は、残ったり非閉所チャネルを移動したりした細胞より一貫して柔らかいことが示されました。
柔らかさの分子的シグネチャー
なぜ一部の細胞が柔らかいのかを理解するため、研究チームはビメンチンという構造タンパク質と、核を支持するタンパク質をコードするLMNA遺伝子に注目しました。ビメンチンは細胞内部の足場の一部で、変形に抵抗するのを助けます。閉所を通過した細胞は、広いチャネルや標準的なシャーレ上にある細胞と比べてビメンチンの量が低下していました。高解像イメージングでは、閉所を移動した細胞ではビメンチンネットワークが細胞体や核の周囲で密な束ではなく、より緩やかに配置されていることが明らかになりました。一細胞レベルの遺伝子発現解析でも、ビメンチン遺伝子(VIM)と核を機械的に頑丈に保つLMNAが、閉所経路を好む細胞で低下していることが確認されました。
細胞を柔らかくすると閉所移動が促進される
研究者らは次に、意図的に細胞を柔らかくして挙動が変わるかを確かめました。彼らは二つの手法を用いました:細胞骨格を再構築することが知られている生化学的処理(TGF-β1)と、柔らかいシリコーン板で細胞に穏やかな機械的圧迫を加える方法です。両手法とも細胞の剛性を低下させ、ビメンチン量を減少させましたが、細胞を死滅させることはありませんでした。こうして前もって柔らかくされた細胞をマイクロ流体デバイスに入れると、未処理の細胞に比べてさらに大きな割合が狭いチャネルへ移動しました。これは、柔らかさが単なる閉所の副次的な結果ではなく、調節可能であり、細胞が小さな隙間に入り通過できるかどうかに強く影響する性質であることを示唆します。
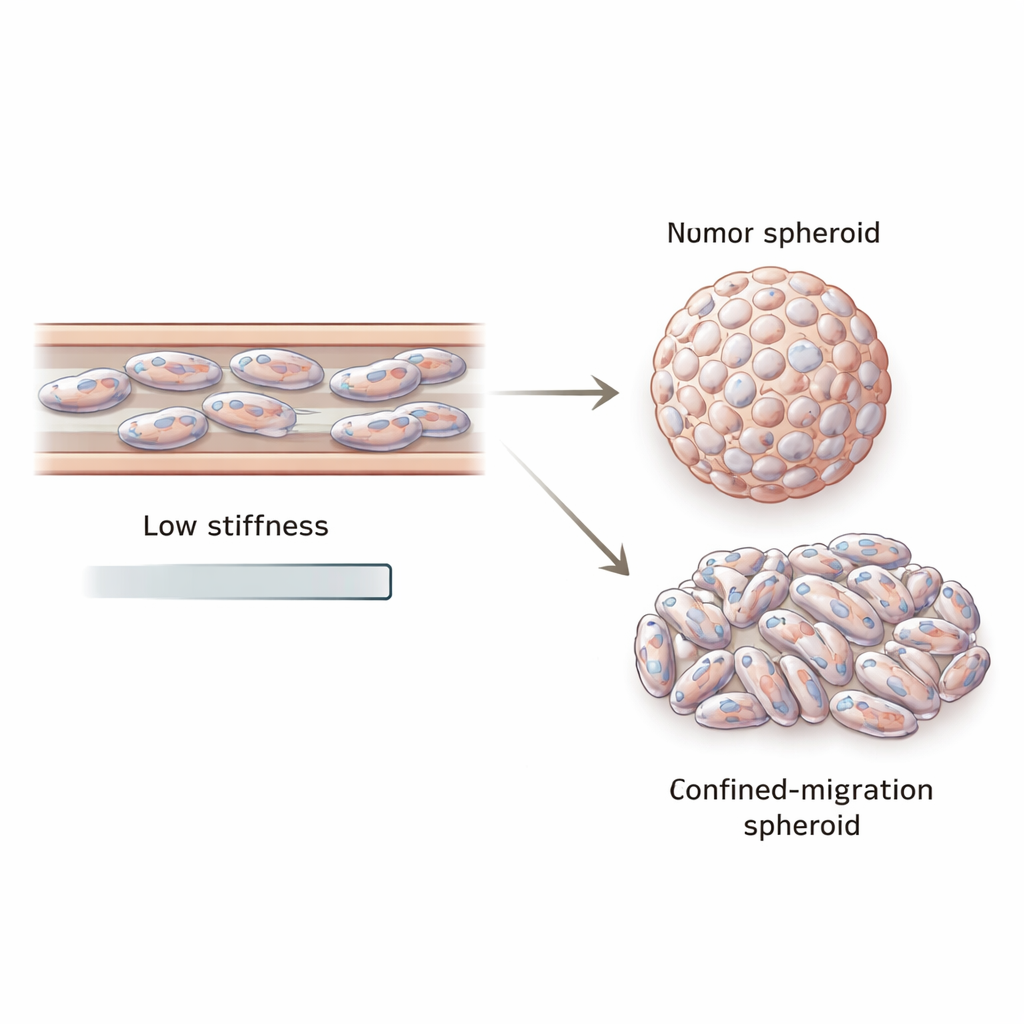
絞られた細胞からゆがんだ腫瘍塊へ
しかし転移は移動だけの話ではありません。脱出した細胞は新しい場所で再増殖して腫瘍を形成しなければなりません。この段階を模倣するため、チームは細孔を通過させてから回収し、非付着性ウェルで三次元の腫瘍“スフェロイド”として増殖させるトランスウェルと呼ばれる別の閉所系を用いました。閉所移動した細胞から育てたスフェロイドは、絞られていない同じ細胞株から育てたものよりも小さく、見た目に丸みが乏しかった。核はより細長く変形しており、これらのスフェロイドではVIMとLMNAの発現低下が持続していました。個々のスフェロイド内でもビメンチンのレベルは中心から縁へと変動しており、娘腫瘍内における力学的・遺伝的多様性を示唆しています。
転移理解への含意
率直に言えば、本研究は多くの肺がん細胞の中で柔らかい細胞ほど狭い場所をすり抜けやすく、その旅を生き延び、後に奇妙な形で機械的に脆弱な腫瘍クラスターを作り、核がゆがむ傾向があることを示しています。これらの細胞は、移動様式と増殖様式を結びつける低いレベルの主要な構造遺伝子という明瞭な分子的シグネチャーを保持し続けます。研究は患者ではなく厳密に制御されたラボの装置で行われましたが、『閉所移動する』がん細胞の物理的・遺伝的な設計図を提示します。長期的には、細胞の柔らかさやそれに対応する分子マーカーを測定したり標的化したりすることが、最も侵襲的ながん細胞亜集団を理解・追跡・最終的に妨げる戦略の一部になる可能性があります。
引用: Alam, M.K., Ma, Y., Zhai, J. et al. Mechano-stress endorsing heterogeneous lung cancer cells migration into confined channels and investigating tumor spheroids growth of confined space migrating cells. Sci Rep 16, 6649 (2026). https://doi.org/10.1038/s41598-026-35818-6
キーワード: がん細胞の剛性, 狭所移動, 肺がんスフェロイド, ビメンチンとLMNA, 腫瘍力学