Clear Sky Science · ja
肺腺がんの予後を示す潜在的バイオマーカーとしてのHROBに関する、バイオインフォマティクス解析と実験結果を統合した包括的研究
なぜこの肺がんタンパク質が重要なのか
肺がんは依然として世界で最も致命的ながんの一つであり、どの患者が予後不良になるか、誰が治療に最もよく反応するかを予測することは臨床上の大きな課題です。本研究は、DNAの複製や修復が行われる細胞内に存在する、あまり知られていないタンパク質HROBに注目します。大規模な遺伝子データベースの解析と実験室での検証を組み合わせることで、HROBが肺腺がんと呼ばれる攻撃的な形式のがんを促進する可能性があり、予後マーカーや将来的な薬物標的になり得ることを示しています。
肺腫瘍における隠れた関係者
研究チームはまず基本的な問いを立てました:HROBは腫瘍で正常組織よりも活性化されているのか?The Cancer Genome Atlas(TCGA)やGene Expression Omnibus(GEO)といった主要ながんリソースから得られた数千件のRNA測定値を用いて、多くのがん種でHROBの発現レベルを比較しました。その結果、複数のがんでHROBの活性が明らかに高く、特に肺腺がんでは正常な肺組織と比べて顕著に上昇していることが分かりました。この傾向は、腫瘍と近接の非がん性サンプルの両方を持つ患者に解析を限定しても維持されており、HROBの増加は単一データセットの偶然ではなく疾患の一貫した特徴であることを示唆しています。
HROBレベルと患者転帰の関連
次に研究者たちは、HROBが患者の将来について何か示唆するかを調べました。肺腺がん患者をHROB高発現群と低発現群に分け、生存期間および無増悪期間を追跡しました。HROBレベルが高い患者は総生存期間が短く、がん関連死亡が多いことが示されました。腫瘍の大きさやリンパ節転移、治療反応といった従来の臨床因子を考慮に入れても、高HROBは独立した予後不良の警告因子として残りました。統計的には、HROBが高い患者は死亡リスクが約80%高いと報告されました。また、喫煙者の肺腺がん患者はHROBレベルが高く、転帰が悪い傾向があり、この分子が既知の環境リスクと結びついていることが示唆されました。
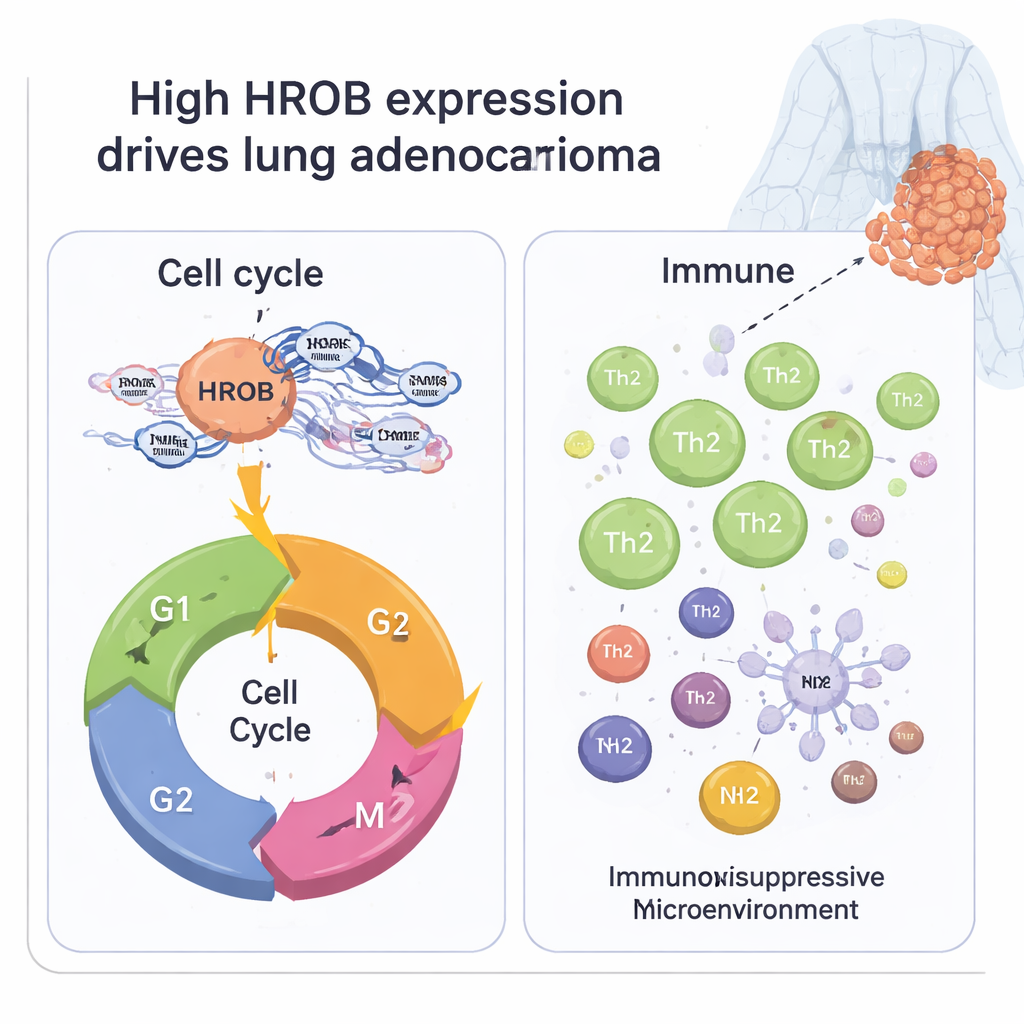
HROBががん細胞の増殖を助ける仕組み
HROBが腫瘍細胞内で何をしているかを探るため、チームはHROB高発現群と低発現群の遺伝子発現パターンを比較しました。数千の遺伝子が差異を示しましたが、最も強いシグナルは細胞周期――細胞が成長・分裂する厳密に制御されたプロセス――に関係していました。染色体の分配、細胞内部の骨格の組織化、重要なチェックポイントの通過に関与する遺伝子群がHROBとともにより活性でした。ネットワーク解析では、細胞分裂の古典的ドライバーである一群のパートナー遺伝子が浮かび上がりました。実験室では、肺がん細胞株でHROBをサイレンシングすると、細胞の増殖が遅くなり、人工膜を介した浸潤が減り、分裂へ進む代わりに休止期(G1期)に滞留することが観察されました。これらの結果は、HROBが肺がん細胞の増殖に対するアクセルペダルのように働くことを示唆しています。
腫瘍の免疫局所環境を形作る
がんは孤立して成長するわけではなく、周囲の免疫細胞と絶えず相互作用しています。したがって本研究では、HROBレベルが肺腫瘍の「免疫微小環境」とどのように関連するかを調べました。HROBが高い腫瘍は、支持的な間質細胞や免疫細胞が全体的に少なく、いわゆる“純度”が高く、がん細胞がより支配的であるように見えました。免疫細胞の種類を詳しく見ると、高HROB腫瘍は腫瘍に有利な条件を作りやすいTh2と呼ばれるヘルパーT細胞のサブセットが豊富であり、樹状細胞、肥満細胞、B細胞、特定のマクロファージなど抗腫瘍反応に関与する他の免疫細胞が乏しいことが示されました。このパターンは、HROBが腫瘍の回避を助ける免疫抑制的な環境を形成する可能性を示しています。
新たな治療に向けてと今後の展望
HROBの役割を記述することに加え、研究者らは公開されている薬剤マッチングリソースを用いて、HROBに結びつく遺伝子発現パターンを反転させ得る既存の低分子化合物を6種類提案しました。これらの薬の一部は既にがん関連のシグナル伝達経路を標的としています。これは初期の計算的探索に過ぎず、これらの薬がHROB自体に直接作用するという証明ではありませんが、今後の検証のための手がかりを提供します。大規模データ解析と細胞実験の組み合わせは一貫した図を描いています:HROBは肺腺がんで過剰活性化し、腫瘍細胞の分裂と浸潤を助け、腫瘍の生存に有利な免疫環境と結びついています。患者や臨床医にとっての意味は、HROBが将来的に血液や組織のマーカーとしてリスク評価に役立ち、さらに臨床および動物での追加検証が行われれば、より精密な治療のための分子標的になり得るということです。
引用: Zhang, F., Liu, X. & Zhou, S. A comprehensive study integrating bioinformatics analysis and experimental results on HROB as a potential biomarker for the prognosis of lung adenocarcinoma. Sci Rep 16, 5056 (2026). https://doi.org/10.1038/s41598-026-35798-7
キーワード: 肺腺がん, HROBタンパク質, がんバイオマーカー, 細胞周期, 腫瘍免疫微小環境