Clear Sky Science · ja
DFT計算、分子ドッキング、およびADMET研究を用いた、トランスサイレチンの潜在的安定化剤としてのAcoramidis基イオン液体の検討
なぜ希少な心疾患の経口薬は作るのが難しいのか
トランスサイレチンアミロイドーシス(ATTR)は、血液中のタンパク質が心臓や神経に蓄積して徐々に損傷を与える深刻な病気です。新薬Acoramidisはこの蓄積を抑えるのに有効ですが、実用的な問題があります:薬剤が水に溶けにくく、錠剤として服用した際に体内へ吸収されにくいのです。本研究は、Acoramidisをイオン液体と呼ばれる塩様の新しい形態に仕立て直すことで、服用しやすく効果的にするという巧妙なアプローチを検討しています。
有望な薬を飲める形に変える
錠剤が機能するためには、まず胃や腸の水性流体に溶け、次に腸壁を通過して血流に入る必要があります。Acoramidisはトランスサイレチン(TTR)タンパク質を安定化させ、有害なタンパク質凝集を防ぐのに有効ですが、溶解性が低く経口薬としてのバイオアベイラビリティが乏しいという課題があります。研究者らはこれに対処するため、Acoramidisをさまざまな帯電性の相手分子と化学的に組み合わせ、3種類の新しいイオン液体(IL1、IL2、IL3)を作製しました。これらは硬い結晶よりも流動性のある塩のように振る舞うことを目指して設計され、薬の溶解性や体内での分布を改善する可能性があります。 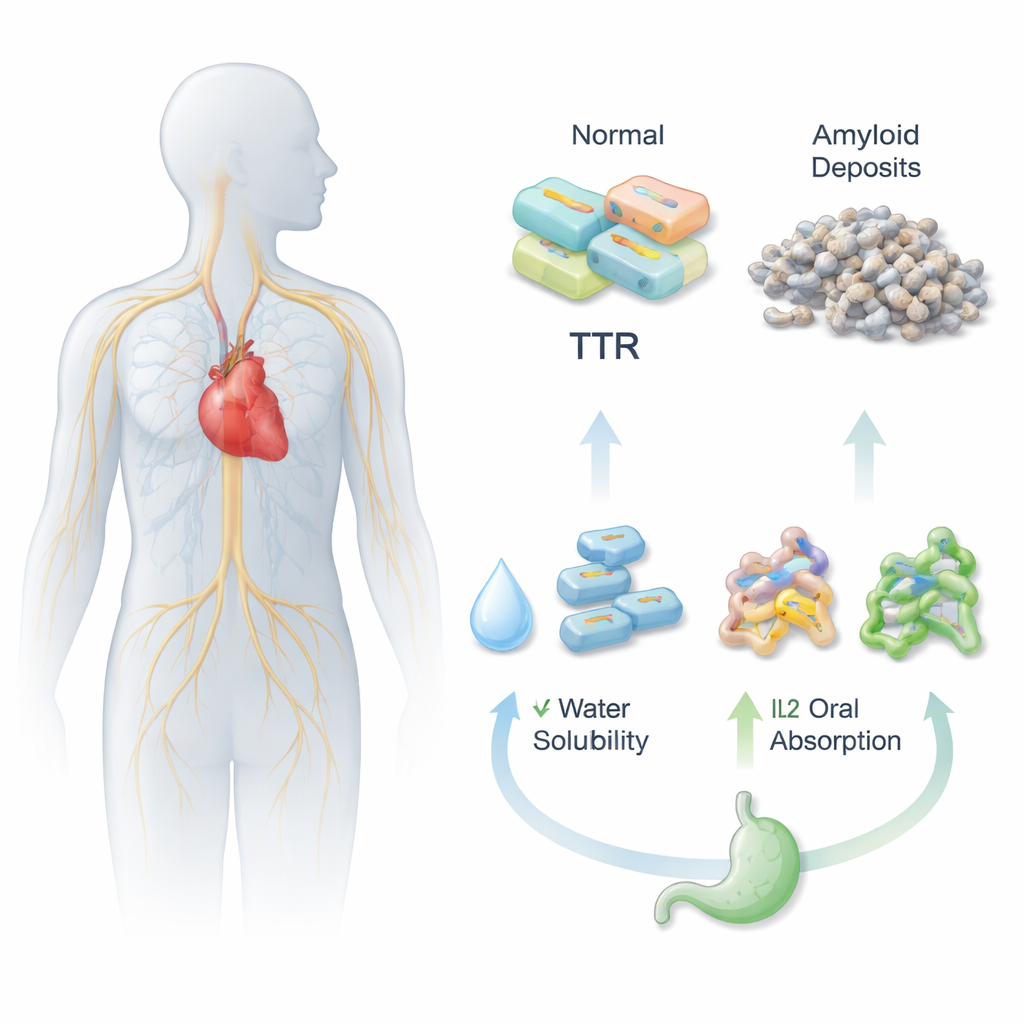
コンピュータ上で新分子を探る
動物やヒト試験に直行する代わりに、チームはこれら新形態がどのように振る舞うかを予測するために高度な計算手法を用いました。量子化学計算により各分子の極性(これが水溶性の主要因)や電子の移りやすさが推定され、これはタンパク質との相互作用の可能性に関係します。IL1は最も高い双極子モーメントと強い電子応答性を示し、水により溶けやすく、標的とより強く柔軟に接触することが期待されました。エネルギー計算はまた、IL1が元の薬や他の2つのイオン液体よりも熱安定性が高いことを示唆しており、目的地に到達する前に分解しにくい可能性を示しています。
薬が標的にどれだけ強く結びつくか
次に研究者らは分子ドッキング、いわば仮想のロックとキー試験を用いて、Acoramidisとその3つのイオン形態がTTRタンパク質の結合チャネルにどれだけ適合するかを評価しました。4つの化合物はいずれもTTRの正しい領域にドッキングしましたが、IL1は最も有利な結合エネルギーと、特にタンパク質の重要なアミノ酸との水素結合を含む複数の安定化相互作用を形成し、最も堅固な結合を示しました。この強い結合は、IL1が親化合物よりもTTRを四量体の安全な構造に保つ能力に優れ、アミロイド沈着を引き起こす有害な分解や誤折りたたみを防ぐかもしれないことを示唆します。
これらの新形態は体内でどのように吸収・排泄されるか?
最後にチームはオンラインの薬物動態ツールを使って、これらの化合物が体内でどのように扱われるかを調べました—どれだけ溶けるか、腸壁を通過するか、血中でどのように循環し、最終的にどのようにクリアされるかなどです。3つのイオン液体はいずれもAcoramidisより水溶性が高いと予測され、IL3が最も高い原始溶解度を示しました。腸透過性や全体的な経口吸収の指標は3種とも改善し、IL1とIL2は腸侵達と予測バイオアベイラビリティのバランスが最も良好でした。血中でのタンパク質結合、クリアランス率、半減期も変化し、イオン液体形態は経口投与後により安定した曝露をもたらす可能性があることを示唆しており、IL1は再び特に有利なプロファイルを示しました。 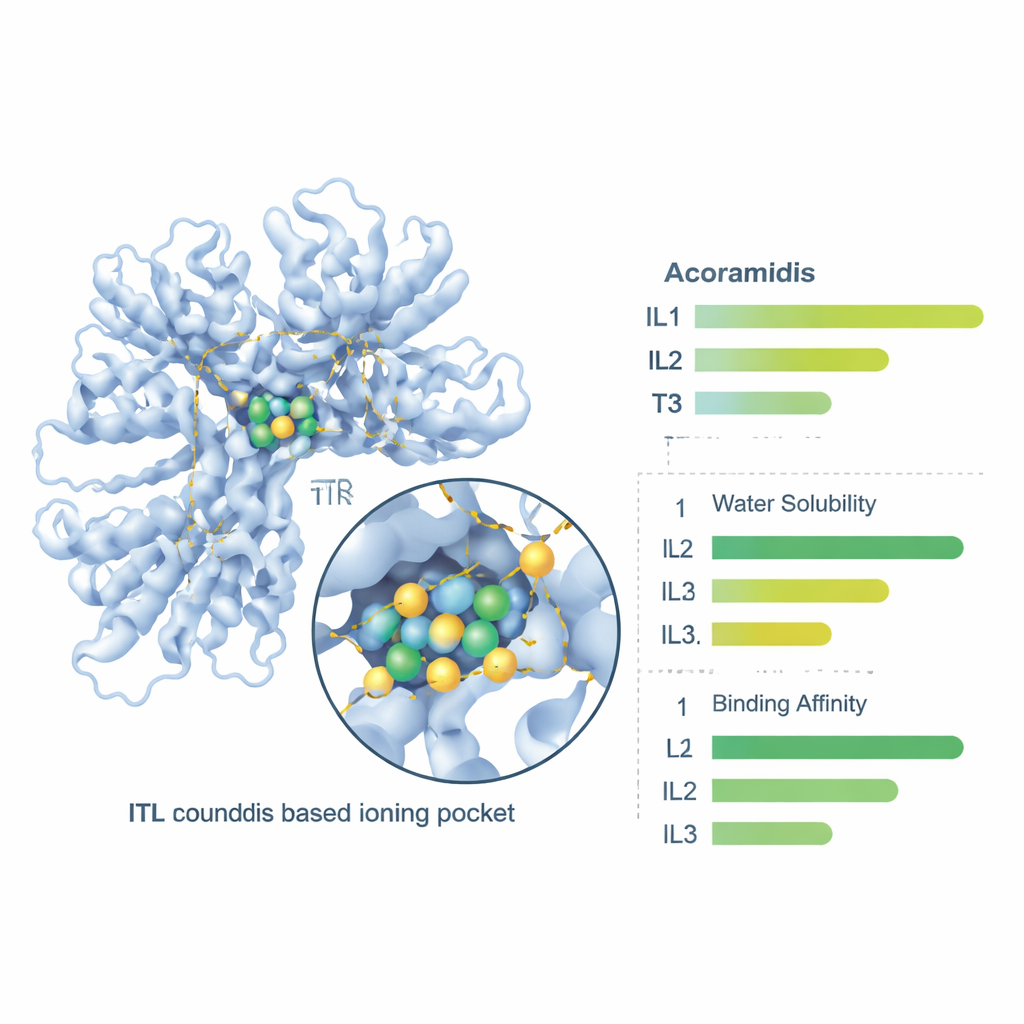
将来のATTR治療にとっての意義
専門外の人にとっての主要なメッセージは、Acoramidisは希少だが深刻な心・神経疾患に対して既に有望である一方、溶解性の低さが経口での効果を制限しているという点です。Acoramidisを特別に設計したイオン液体に変換することで、本研究は完全に計算ベースの検討で、溶解性が向上し、標的タンパク質への結合が強化され、吸収が効率化される可能性があるバージョンを作り得ることを示しています。3つの候補のうち、IL1は安定性、結合力、溶解性、予測される経口吸収のバランスが最も良く、将来の実験室および臨床開発に向けた有力なリードとなり、より効果的で服用しやすいATTR治療の提供に貢献する可能性があります。
引用: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
キーワード: トランスサイレチンアミロイドーシス, Acoramidis, イオン液体, タンパク質の誤折りたたみ, 経口薬物送達