Clear Sky Science · ja
標的化アルファ線治療のためのハイブリッドキレータ 3p-C-DEPA と Ac3+/Bi3+ の錯形成に関する密度汎関数理論計算
がん治療においてこの研究が重要な理由
現代のがん医療は、腫瘍を細胞単位で追跡・破壊できる放射性薬剤にますます依存しています。標的化アルファ線治療と呼ばれる強力な手法は、個々のがん細胞を極めて高精度に死滅させうる高エネルギー粒子を利用します。しかし、これらの粒子を安全に届けるためには、放射性金属を小さな分子『ケージ』にしっかりと閉じ込め、健常組織へ漏れないようにする必要があります。本研究は、アクチニウム‑225 やビスマス‑213 のように特に取り扱いが難しい金属を保持するために設計された新しいケージ分子 3p‑C‑DEPA を調べ、既存の標準的キレータである DOTA よりも安定に結合できるかを問います。
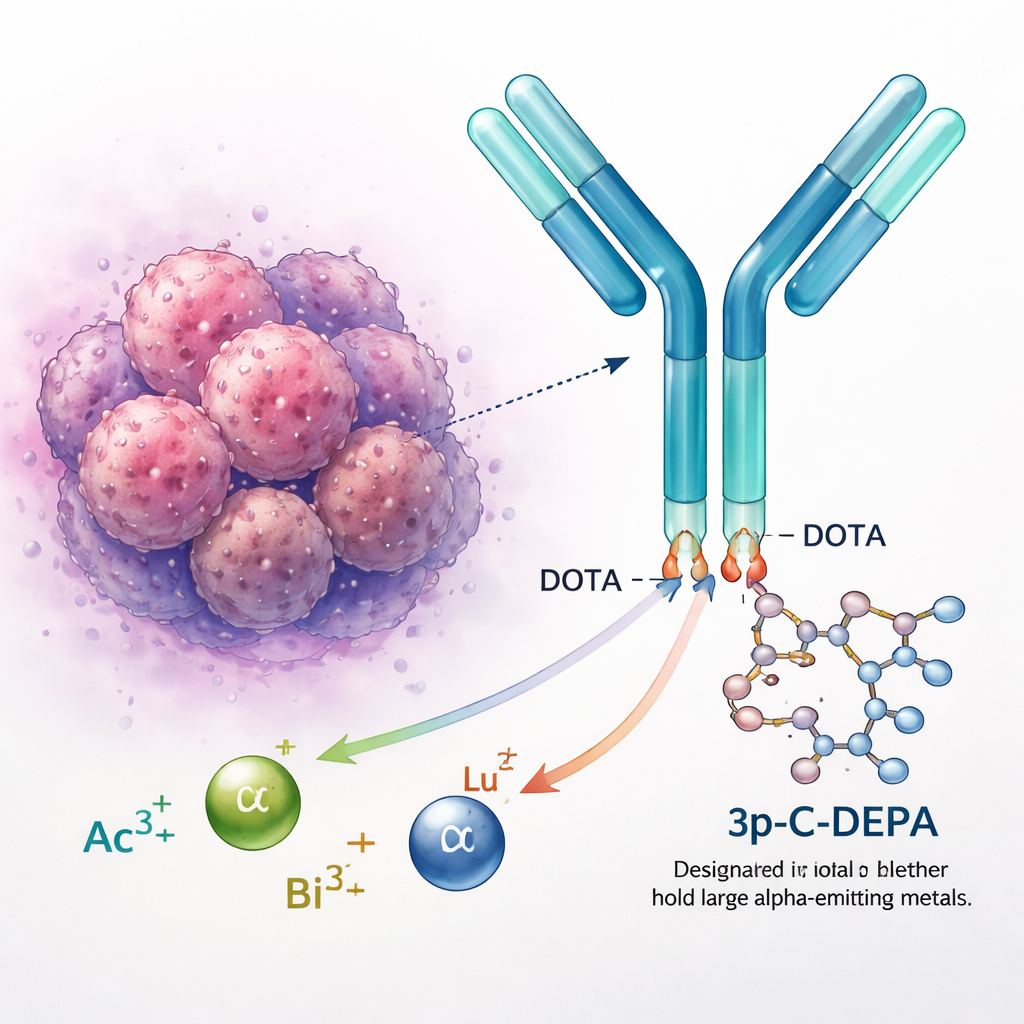
放射性金属を安全に固定する
アクチニウム、ビスマス、ルテチウムなどの放射性金属は、がんの診断や治療に用いられます。しかし単体ではこれらの正に帯電した金属イオンは体内で自由に反応し、健常臓器に害を及ぼす可能性があります。そこで化学者はこれらを『キレータ』と呼ばれる環状分子に結合させ、金属を包み込んで固定します。ゴールドスタンダードであるキレータ DOTA はいくつかの承認薬で用いられていますが、アクチニウム‑225 のようなより大きく電子密度が拡散したイオンには苦戦します。これらの金属は時間とともに脱離する可能性があり、長期的な安全性に懸念を生じさせ、標的化アルファ線治療の普及を制限しています。
大きな原子のために作られたハイブリッドケージ
新しいキレータ 3p‑C‑DEPA は、二つの確立された設計の特徴を組み合わせています:DOTA の剛直な環状骨格と、別のキレータ DTPA のより柔軟で開いた構造です。このハイブリッドな構造により、3p‑C‑DEPA は DOTA の八つに対して十個の強い結合『手』(窒素および酸素原子)を持ち、より広い空孔を備えて大きな金属イオンをよりよく収容できます。先行する実験では、3p‑C‑DEPA が穏やかな温度で抗体を迅速に標識でき、血清中でビスマス系放射性核種を安定に保持することが示唆されていました。本研究は次の段階として、量子レベルの計算を用い、3p‑C‑DEPA と DOTA がルテチウム‑177、ビスマス‑213、アクチニウム‑225 をどの程度結合するかを体系的に比較します。
分子間の握手を覗く
短寿命のアルファ線放出核種を直接扱うのは困難であるため、研究者は密度汎関数理論(DFT)という強力な計算手法に頼りました。DFT は分子内で電子がどのように配列し、原子同士がどれほど強く引き合うかを推定します。研究では、各金属イオンを水中モデルで扱い、続いて DOTA または 3p‑C‑DEPA との錯体をモデル化し、金属が水からキレータのケージに移るときの自由エネルギー変化を計算しました。このエネルギー変化は『安定定数』に変換され、値が大きいほどキレータが金属をより強く保持することを意味します。現実的な溶液条件を模擬し、単一の計算設定によるアーティファクトを排するために、二種類の異なる DFT アプローチと二つの溶媒化モデルが用いられました。
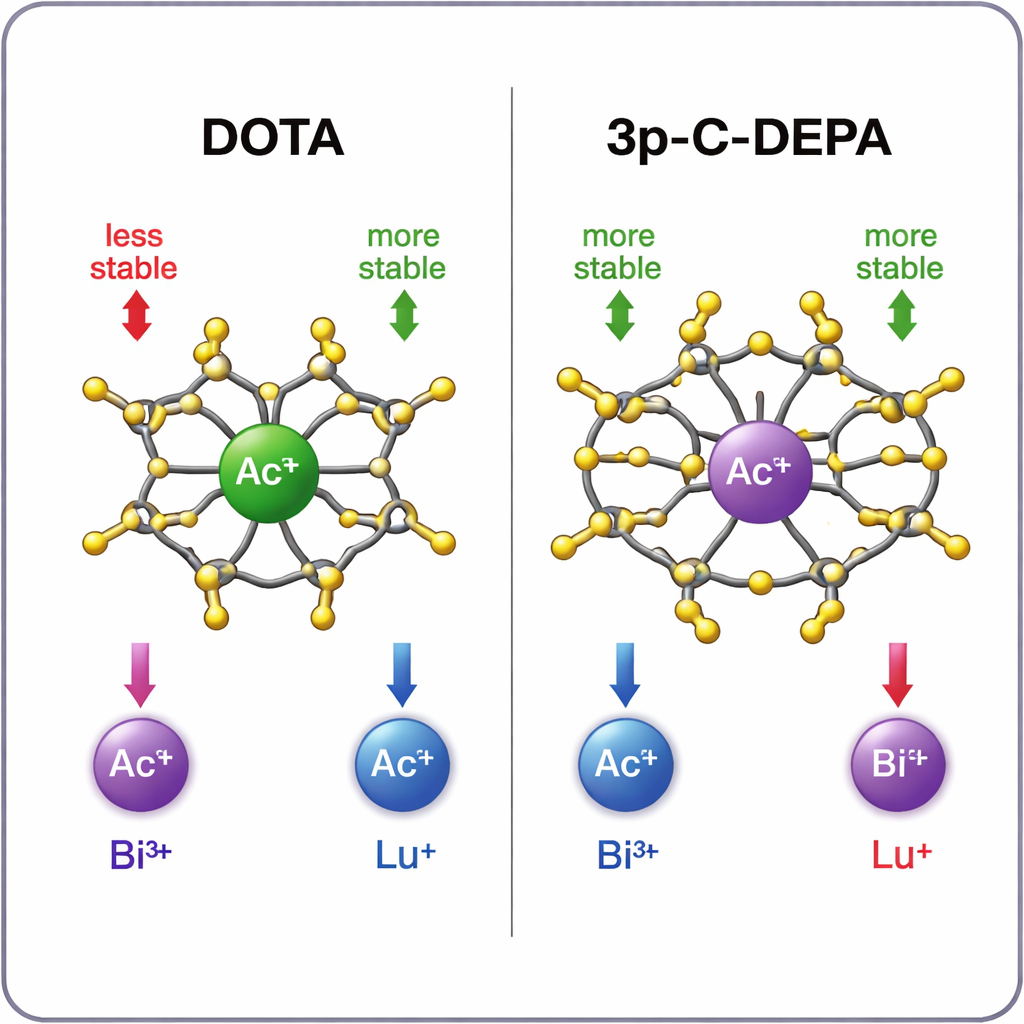
どのケージがどの金属を最もよく保持するか?
シミュレーションは明確なパターンを示します。大きなアクチニウムイオンに対しては、3p‑C‑DEPA はその大きな空腔と、金属を把握できる酸素供与体の数の多さにより、DOTA より著しく安定な錯体を形成します。ビスマス‑213 も 3p‑C‑DEPA にうまく収まり、サイズと電子受容性の両面から利益を受けます――これはキレータの電子供与基と良くマッチします。一方で小型のルテチウム‑177 は DOTA のより引き締まった八腕の環境に快適に収まります。3p‑C‑DEPA では余分な供与体群が小さなイオンの周りで混み合い、反発的相互作用を生じさせ、標識を遅らせ最終錯体をやや弱めるように見えます。計算で得られた安定性の傾向は既存の実験データや放射標識収率と良く一致し、理論予測に信頼性を与えています。
将来のがん治療にとっての意味
日常的な表現を用いれば、本研究は DOTA が万能のケージではないことを示唆します:ルテチウムのような小さな金属には非常に適している一方で、アクチニウム‑225 のようなかさ張るアルファ放出体には最適ではありません。これに対して 3p‑C‑DEPA は、これら大きなイオンのために特注されたホルダーのように振る舞い、より緩やかな条件下でそれらをよりしっかりと掴むため、抗体のような繊細な標的分子にも向きます。さらなる実験的・臨床的検証は必要ですが、計算結果は 3p‑C‑DEPA が安全でより効果的な標的化アルファ線治療の有望な基盤となり得ることを示しており、周囲の健常組織を温存しつつ腫瘍を根絶できる高力価治療へのアクセス拡大に寄与する可能性があります。
引用: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
キーワード: 標的化アルファ線治療, 放射性医薬品, キレータ設計, アクチニウム225, 密度汎関数理論