Clear Sky Science · ja
ストレス下でMCU-1非依存的メカニズムにより生じる、プレセニリン‑1変異をもつヒトiPSC由来ニューロンのミトコンドリア機能障害とCa2+調節不全
なぜこれはアルツハイマー病に重要か
アルツハイマー病は脳内の粘着性のあるタンパク質プラークで語られることが多いが、記憶が薄れるずっと前に、神経細胞内の小さな「発電所」であるミトコンドリアやカルシウムイオンの取り扱いがすでに乱れ始めている可能性がある。本研究は、既知の家族性アルツハイマー変異を持つ人の皮膚細胞から作られたヒトニューロンを用い、単純だが重要な問いを立てる:エネルギー産生とカルシウムの恒常性はどれほど早く、どのようにして失われ始めるのか?
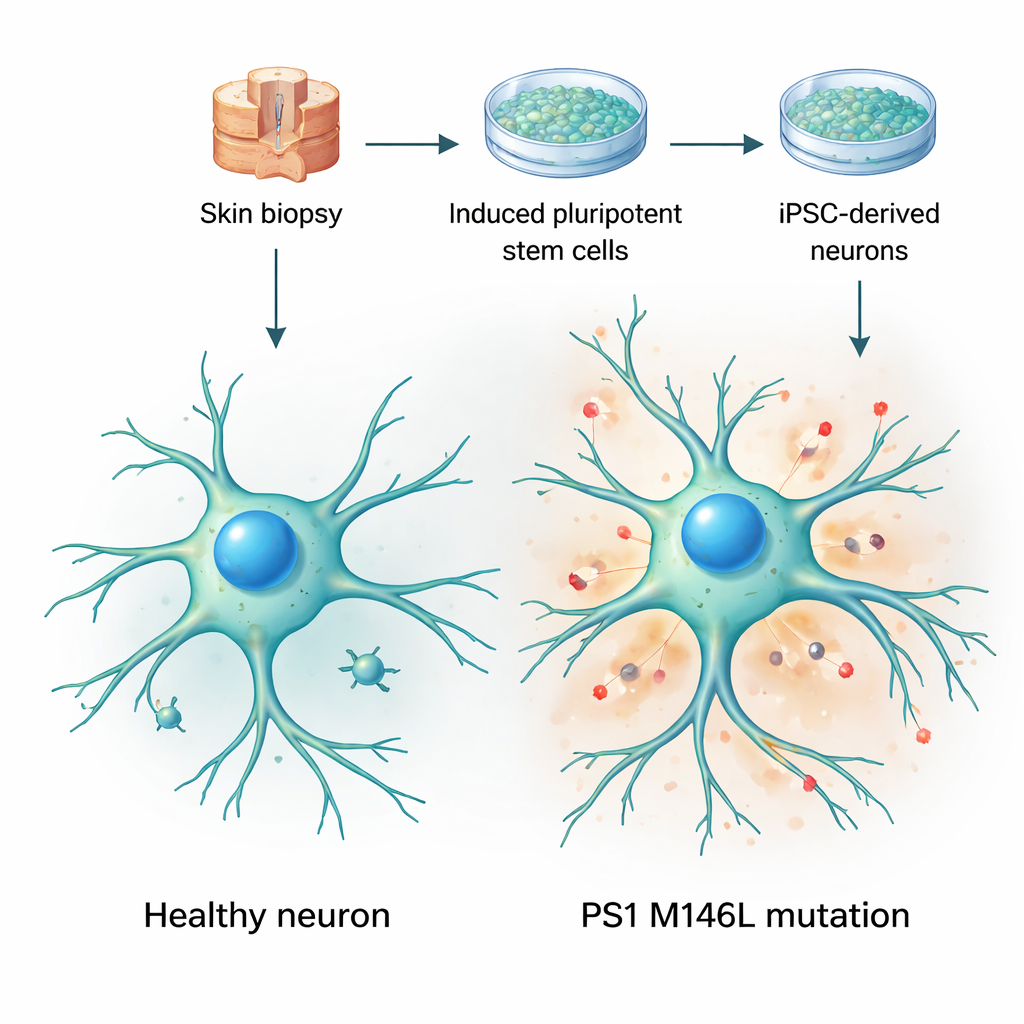
皮膚細胞を生きた脳モデルに変える
研究者らはまず2人の女性から皮膚生検を採取した:健康な被験者1名と、アルゼンチンの家系にみられる早発性アルツハイマーと関連するM146Lというプレセニリン‑1変異の無症候保因者1名である。彼らは皮膚細胞を誘導多能性幹細胞(ほぼあらゆる組織になり得る細胞)にリプログラムし、それをさらに神経細胞へと分化させた。数週間の培養で、これらの細胞は典型的な神経形態を獲得し、長く枝分かれした突起を伸ばし、標準的な神経マーカーを発現した。重要なのは、対照と変異をもつ細胞の成熟速度が類似しており、概ね健康に見えたことで、研究チームは明白な細胞死や損傷ではなく微妙な機能変化に焦点を当てられた点である。
電気信号とカルシウムの負荷下での挙動
神経細胞は多くの細胞プロセスで高速のオン/オフスイッチとして働く荷電原子であるカルシウムの厳密な制御に依存している。研究チームは蛍光色素を用いて、カリウムで電気刺激したりシグナル分子で活性化したときに細胞内カルシウム濃度がどう変化するかを追跡した。単純な脱分極刺激の下では、M146L変異をもつニューロンは対照ニューロンに比べてカルシウム上昇が弱く、通常カルシウム流入を駆動する電気的・イオン勾配の維持に問題があることを示唆した。しかし、研究者らがよりストレスのかかる状況—小胞体(ER)内の貯蔵からカルシウムを強制的に放出させた場合—を引き起こすと、差はより明瞭になった。こうしたストレスに反応して、変異ニューロンのミトコンドリアは対照細胞に比べて著しく少ないカルシウムを取り込んだ。これは危険なカルシウム急増を緩衝する能力が低下していることを示す。
カルシウム恒常性とエネルギー使用の切り離し
この変化したカルシウム処理が細胞代謝にどう影響するかを調べるため、研究者らはニューロンの酸素消費量を測定した。これはミトコンドリア活動の直接的な指標である。驚いたことに、M146L変異をもつニューロンはより多く酸素を消費していた:基底および最大の酸素消費率、ならびにATP産生に結び付く酸素量はいずれも対照細胞より高かった。しかし酸素消費とATP産生の結びつきの効率は類似しており、ミトコンドリア数や主要なATP合成酵素の増加は見られなかった。かわりに、変異ニューロンのミトコンドリアはより長く管状であり、ミトフュージン‑1という融合タンパク質のレベルが高く、慢性的で低レベルのストレス下にある細胞でよく見られるパターンを示した。これらの過活動かつ伸長したミトコンドリアは、制御されないとタンパク質やDNAを損傷しうる不安定な分子である活性酸素種をより多く生成していた。
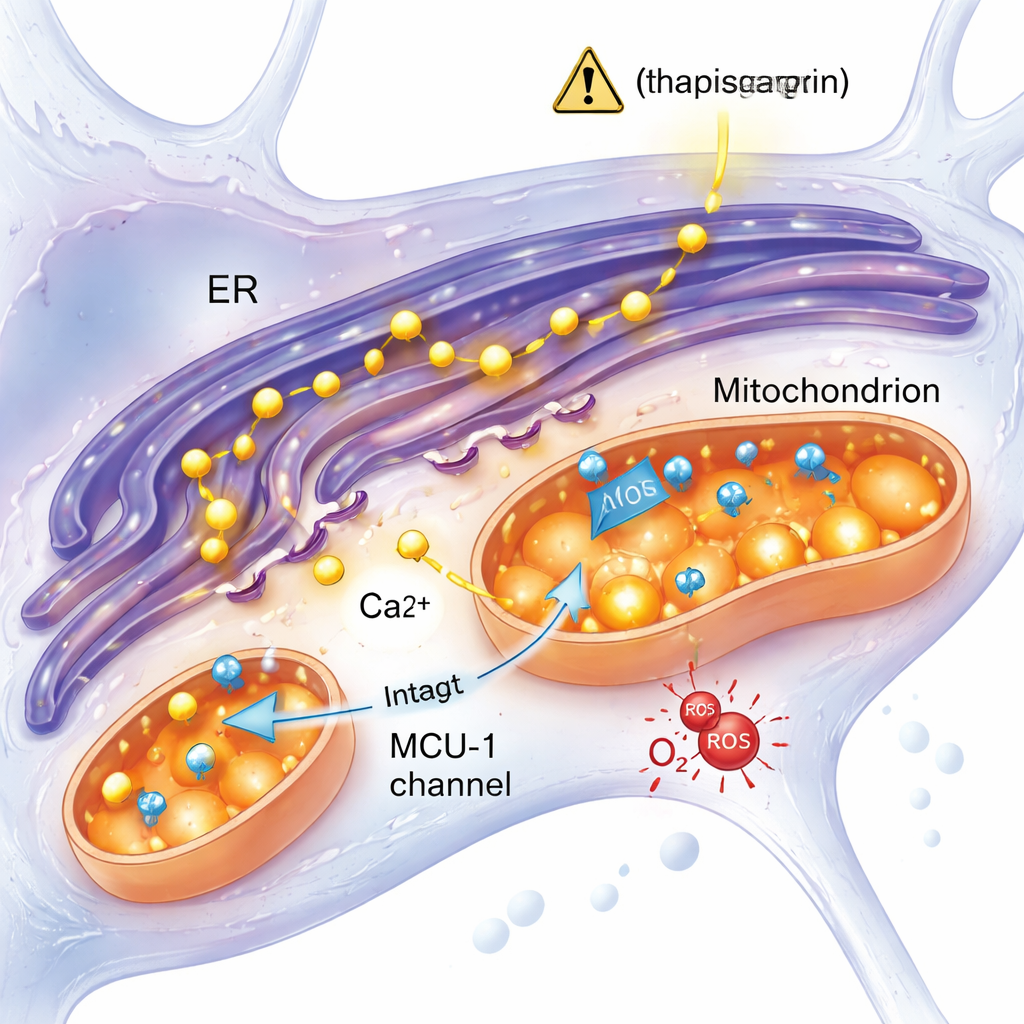
主要なカルシウムチャネルに依存しないストレス応答
アルツハイマー研究の有力な仮説のひとつは、小胞体から過剰なカルシウムがミトコンドリアへミトコンドリアカルシウムユニポーター(MCU‑1)を通して流入し、ミトコンドリアを過負荷にして機能不全を引き起こすというものである。本研究はその考えを直接検証した。チームが特異的阻害剤でMCU‑1を遮断すると、対照および変異の両ニューロンでミトコンドリアのカルシウム取り込みが大幅に減少し、チャネル自体は両群で機能していることを確認した。さらに、IP3受容体を介するより生理的な経路でカルシウム放出を誘発した場合、変異細胞と対照細胞の反応は類似していた。これらの結果は、MCU‑1チャネルの破綻からは離れ、むしろ小胞体とミトコンドリアの物理的・機能的接触やそれらの相互作用の他の側面が変異ニューロンで変化していることを示唆する。
疾患の理解と治療への含意
総じて、本研究の結果はPS1 M146Lアルツハイマー変異を持つヒトニューロンを、安静時には外見上正常だがストレス下で異常に反応する細胞として描き出す。内部貯蔵が突然放出されたときにミトコンドリアは十分なカルシウムを取り込めず、それでもエネルギー的には高負荷で稼働している—より多くの酸素を消費し、より多くの活性酸素種を生成する—ため、高コストの代償モードに固定されているかのようである。これが臨床症状の前の生きたヒト由来ニューロンで起きていることから、カルシウムシグナルの破綻と早期のミトコンドリアの過活動は、アルツハイマー病における後期の副産物ではなく上流の出来事であるという考えを支持する。専門外の読者への要点は、カルシウム信号とミトコンドリアのエネルギー産生のバランスを保つことが、よりよく知られたアミロイドプラークを標的にすることと同じくらい病気の予防に重要であり得るということである。
引用: Wilson, C., Galeano, P., Remedi, M.M. et al. Mitochondrial dysfunction and Ca2+ dysregulation in human iPSC-derived neurons carrying presenilin-1 mutation arise under stress via an MCU-1-independent mechanism. Sci Rep 16, 6002 (2026). https://doi.org/10.1038/s41598-026-35597-0
キーワード: アルツハイマー病, ミトコンドリア, カルシウムシグナル伝達, プレセニリン‑1変異, iPSC由来ニューロン