Clear Sky Science · ja
2,5-置換-1,3,4-オキサジアゾール類似体の構造的および計算的支援による開発:活性なLOX、ウレアーゼ、およびα-グルコシダーゼ阻害剤として
一般的な疾患に取り組む新しい化学ツール
潰瘍や腎結石から糖尿病や慢性炎症に至るまで、多くの日常的な健康問題は体内の酵素の過剰活性によって引き起こされます。本研究は、これらの酵素の働きを抑える「小さなブレーキ」として働くよう設計された一群の新規小分子を調べています。構造を調整し、実験室および計算機上で評価することで、研究者らは将来のより効果的で安全な医薬品の基盤を築くことを目指しています。 
なぜこれらの酵素が重要か
研究チームは、健康において非常に異なるが同様に重要な役割を果たす三つの酵素標的に着目しました。ウレアーゼは尿素を分解するのを助けますが、ある種の細菌や組織で過剰に働くと胃や尿路の潰瘍、腎結石、さらには高血圧に寄与することがあります。α-グルコシダーゼは腸管細胞の表面に存在し、複雑な炭水化物をグルコースに切断します。これを阻害することは2型糖尿病の血糖管理に有効な既存の手段です。リポキシゲナーゼ(LOX)は脂肪を炎症、ぜんそく、いくつかのがん関連プロセスを駆動するシグナル分子に変換します。これらの酵素を他のシステムに害を与えずに抑える薬は強く求められています。
候補分子ライブラリの構築
このような薬を探索するため、研究者たちは1,3,4-オキサジアゾール環にピペリジンユニットを連結した骨格に基づく、関連する15種の化合物シリーズを合成しました。この化学スキャフォールドは既存のいくつかの医薬品にも見られ、生体標的との相互作用に優れることが知られています。研究チームは、メチル、エチル、メトキシ、ベンジル、シクロヘキシルなどの小さな置換基を異なる位置に付けることでコアの「装飾」を変化させ、7aから7oとラベル付けした小さな候補ライブラリを作成しました。赤外線や核磁気共鳴などの標準的な分析手法で各構造を確認し、合成物が設計通りであることを確かめました。
分子が酵素をどれだけ阻害するかの評価
各化合物は精製されたLOX、ウレアーゼ、α-グルコシダーゼに対して試験され、酵素活性をどの程度抑えられるかを評価しました。いくつかの分子が際立ちました。α-グルコシダーゼに対しては、化合物7aおよび7nが特に有効で、低マイクロモル濃度で高い阻害率を示し、実験室試験では標準的な糖尿病薬アカルボースを上回りました。LOXに対しては7a、7h、7nが非常に強い活性を示し、場合によっては天然の参照阻害剤クエルセチンより優れていました。ウレアーゼアッセイでは、7aおよび特に7lが標準阻害剤チオ尿素に匹敵するかやや上回る結果を示し、将来的に抗潰瘍や抗結石療法のリード化合物となり得ることを示唆しました。 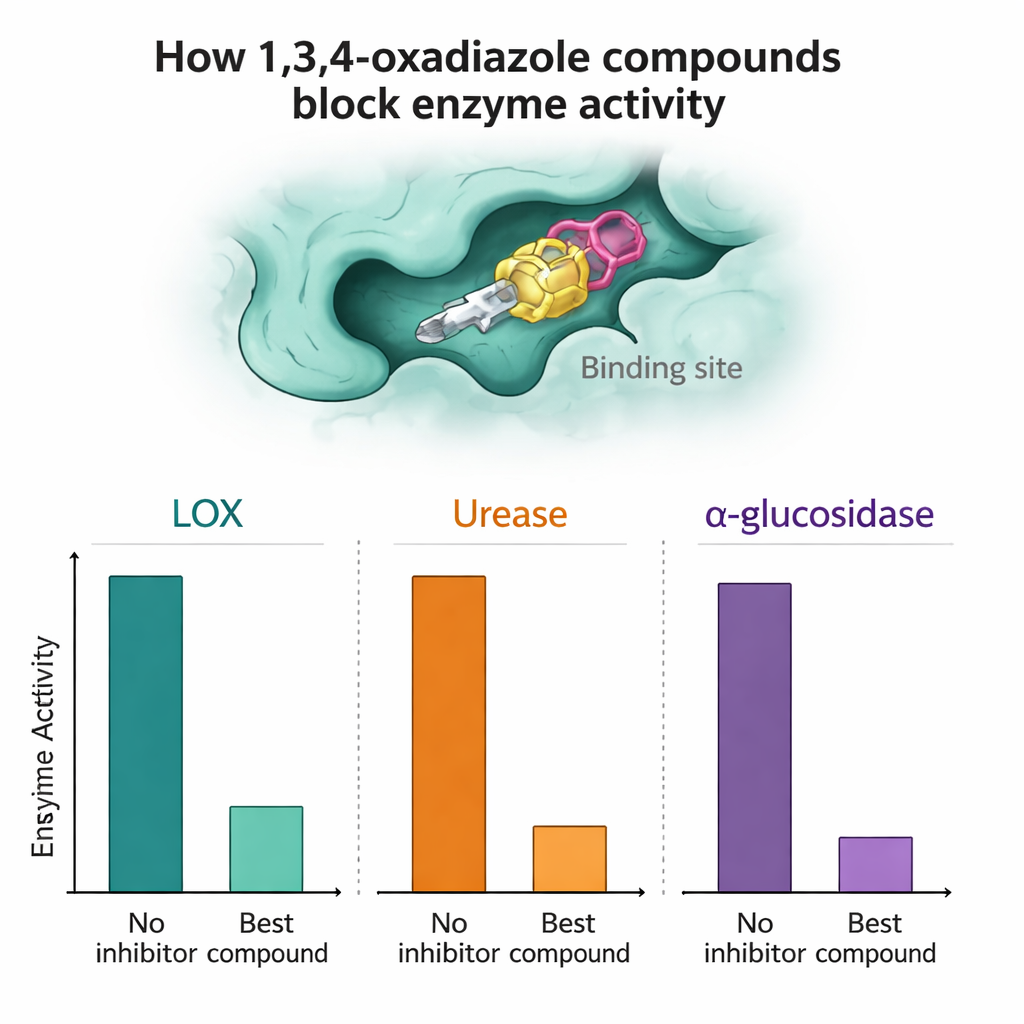
構造と性能の関連づけ
7a–7oの化合物間の違いはコア環系まわりの小さな変化だけなので、研究者らは単純な構造—活性相関を描き始めることができました。たとえば、付随する環の特定の「オルト」位置に小さな炭化水素基を導入すると、α-グルコシダーゼやLOXの阻害能が向上することが多く見られました。逆に、好ましくない位置に配置された一部のメトキシやエステル基は活性を弱める傾向がありました。その理由を理解するために、チームは計算機シミュレーションを用いました。量子化学計算は、全ての分子が熱力学的に安定であり、酵素のポケットに適応できるだけの柔軟性を持つことを示しました。ドッキング研究(各分子を酵素の三次元モデルに仮想的に当てはめる解析)は、最も活性の高い化合物が活性部位の重要な箇所で水素結合と疎水性相互作用の混合を通じてより緊密に接触している一方、弱い候補はフィットが甘かったり重要な接触点を逃していることを明らかにしました。
将来の医薬品にとっての意義
平易に言えば、本研究は三つの疾患関連「錠」にうまくはまる有望な「鍵」をいくつか特定し、なぜある鍵が他よりもよく回るのかを原子レベルで説明し始めています。これらの分子がすぐに薬になるわけではありません—安全性試験、体内での挙動の最適化、動物およびヒトでの試験がまだ必要です。しかし、本研究は1,3,4-オキサジアゾール—ピペリジン骨格が糖尿病、炎症性疾患、ウレアーゼ関連障害を標的とする将来の治療法の有望な出発点であることを示しています。入念な実験的測定と詳細な計算モデルの組み合わせは、これらの候補をより精密かつ効果的な医薬品に磨き上げるためのロードマップを提供します。
引用: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
キーワード: 酵素阻害剤, 創薬, オキサジアゾール化合物, 糖尿病と炎症, ウレアーゼとリポキシゲナーゼ