Clear Sky Science · ja
出芽酵母ではなく分裂酵母での発光補完によるタンパク質–タンパク質相互作用検出のための全ゲノムスクリーニングシステムの開発
タンパク質の隠れた営みを光で照らす
私たちの心拍、思考、呼吸の一つ一つは、細胞内でタンパク質が協働することに依存しています。こうした小さな連携、すなわちタンパク質–タンパク質相互作用は、遺伝子の発現から細胞のストレス応答に至るまであらゆる過程を制御します。しかし多くの相互作用は短時間で起こったり繊細だったりして、現在の手法では検出が困難です。本研究は、単純なモデル生物である分裂酵母を用い、これまで見えにくかった何千ものタンパク質接触を同時に明らかにする高感度な“光ベース”のスクリーニングシステムを紹介します。
なぜタンパク質の“相棒”は見えにくいのか
タンパク質はめったに単独で働きません。時と場合によって別の相手に結合し、瞬間的な結合も多く、化学修飾や細胞内の局在によってふるまいが変わります。従来の相互作用解析法は、タンパク質を本来の環境から引き離したり、すべての組合せを捕まえきれない遺伝的トリックに頼ったりするため、細胞内で誰が誰と相互作用するかの地図は未完成です。著者らは、生きた分裂酵母細胞内でほぼすべてのタンパク質を網羅的に調べられる、より柔軟で高感度なシステムを構築することでこの状況を改善しようとしました。
接触を光に変える仕組み
新しいアプローチの中核は、分割酵素による発光です。一方の断片(LgBiT)は研究対象の“餌(bait)”タンパク質に結合され、もう一方(SmBiT)は各酵母株ごとに一つずつ多様な“獲物(prey)”タンパク質に結合されます。単独ではこれら二つの酵素断片はほとんど相互作用しませんが、餌と獲物が細胞内で結びつくと断片が再結合して機能的な酵素が復元され、化学基質の存在下で光を放ちます。各酵母株が放つ光の量を測定することで、どのタンパク質が細胞内で実際に出会っているか、その結合強度を判断できます。タグがタンパク質の通常の機能を妨げて相手を見逃すのを防ぐため、餌タンパク質はLgBiTを両端のいずれかに付けた二つのバージョンで作製され、少なくとも一方の向きが機能する確率を大幅に高めています。 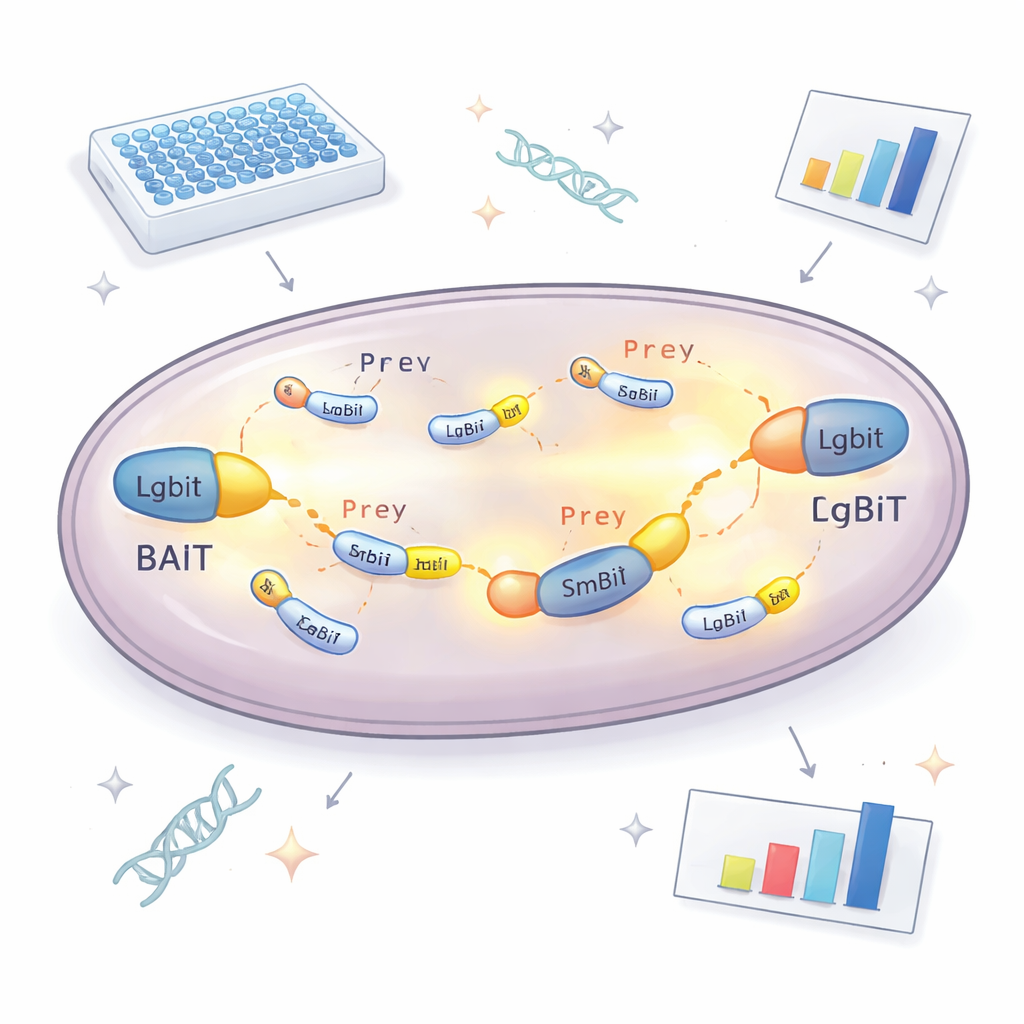
酵母ライブラリと株系の設計
このプラットフォームの構築には巧みな酵素だけでは不十分でした。研究者らは数千の獲物タンパク質を制御された単一コピーで酵母に導入する必要がありました。獲物用に設計された特別なDNAベクターは、分裂酵母ゲノムの既知の座位に挿入され、赤色蛍光マーカーを保持します。この赤色シグナルの明るさは挿入コピー数を反映し、正確に一コピーのコロニーを容易に選別できるため、信頼できる比較に不可欠です。また、LgBiTを餌タンパク質の前端または後端に配置し、柔軟なリンカーで分離する専用の餌ベクターも作製され、タンパク質が正常に折りたたまれ可動することを可能にしています。さらに、二つの餌コンストラクトと一つの獲物コンストラクトを同時に保持できるよう入念に設計された酵母株が構築され、栄養マーカーを用いて正しく組み合わされた細胞のみが生存するようにしています。
システムの実証
設計が検出を本当に改善するかを確認するため、研究者らはまず既知の相互作用を持つタンパク質群を調べました。信号強度は光るタグの取り付け位置に強く依存することが確認されました:ある相互作用はLgBiTが餌の片端にある場合にのみ検出され、逆側では見えないことがありました。両方のバージョンを同時に発現させると発光が増強され、二重餌戦略が弱いまたは配向に依存する相互作用を捕まえやすくすることが示されました。また、このシステムは膜結合タンパク質を含む接触も検出できました。膜タンパク質は従来の酵母二分子ハイブリッド法では特に扱いが難しいクラスです。この検証を経て、研究チームは全ゲノムスクリーニングへと規模を拡大し、転写に関わるタンパク質Tfs1を餌に使用しました。4,600を超える獲物タンパク質をスクリーニングした結果、31件の強い候補が見つかり、その中には既知の相互相手も含まれ、多くは新規で、ミトコンドリアや細胞表面のような核外の位置にあるものもありました。 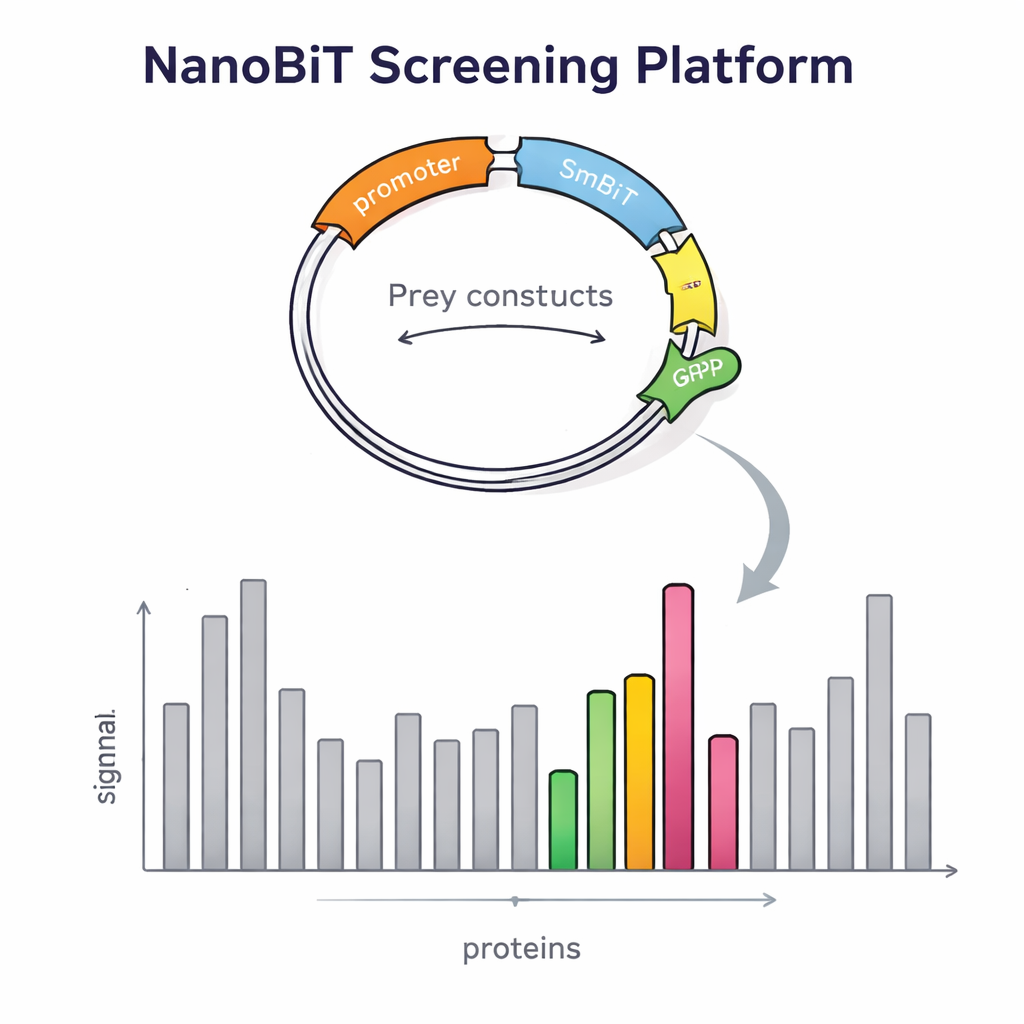
生物学と創薬への意義
専門外の方に向けた要点は、著者らがより高感度な“相互作用レーダー”を酵母細胞内に構築したことです。短時間のタンパク質のやり取りを測定可能な光の閃光に変換し、三つのタグ付きタンパク質を同時に発現させるよう遺伝学を巧みに配置することで、既知の相手だけでなくこれまで見えなかった相手も明らかにします。各新規の結合については他手法による追加検証が依然必要ですが、このプラットフォームは細胞ネットワークの地図の重要な穴を埋めます。さらに株株系が小分子に対して感受性を高めるよう設計されているため、同じ設定を用いて有害なタンパク質間相互作用を遮断する薬や有益な相互作用を安定化する薬を探索することも可能であり、基礎生物学と創薬の初期段階の両方にとって強力な新手段を提供します。
引用: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
キーワード: タンパク質相互作用, 分裂酵母, 発光アッセイ, ハイスループットスクリーニング, 創薬ツール