Clear Sky Science · ja
連続したプラチナ系化学療法とPARP阻害がマウスBRCA2変異膵臓がんにおけるPD1免疫療法の有効性を高める
患者にとってこの研究が重要な理由
膵臓がんは最も致死率の高いがんの一つで、腫瘍がBRCA2遺伝子のような治療上の脆弱性を持つと分かっていても、現在の治療は長期にわたって病勢を抑え続けることがめったにありません。本研究は現実的なマウスモデルを用い、多くの患者や腫瘍医が直面する実用的な問いを扱います。強力な化学療法とPARP阻害を行った後に現代の免疫療法を追加することで生存が有意に延びるのか、そしてなぜ腫瘍がしばしば再発するのかを検証します。
遺伝的弱点を持つ扱いにくいがん
膵管腺がんは治療が極めて難しく、5年生存率は依然として一桁台です。患者のごく一部は、壊れたDNAを修復するために必要なBRCA2に先天的または腫瘍特異的な欠損を持ちます。こうした腫瘍は、プラチナ系化学療法のようなDNAを損傷する薬剤や、がん細胞のDNA修復能力をさらに弱めるPARP阻害剤に特に感受性があります。進行したBRCA変異膵臓がんの現在の標準治療は、数ヶ月のプラチナ系化学療法の後にPARP阻害剤で維持療法を行うことです。しかし主要なPOLO臨床試験ではこの戦略が全生存期間を延長しなかったため、耐性の理解とより良い維持療法の設計が必要であることが示されています。
より実態に即したマウスモデルの構築
既存の多くの実験室モデルは、患者の腫瘍を取りまく免疫や間質成分を取り除いてしまいます。これを克服するために、著者らは完全に機能する免疫系を持つ状況下でBRCA2欠損の膵腫瘍を発生させるマウスを設計しました。これらの自然発生腫瘍からクローン性細胞株を樹立し、遺伝的に一致するマウスに移植できるようにしました。これらのBrca2変異腫瘍はヒトの膵臓がんに非常によく似ており、密な線維化を示し、T細胞がほとんど浸潤せず、自発的なDNA損傷の高レベルを示していました。重要なことに、腫瘍は一般的なプラチナ併用(ジェムシタビン+シスプラチン)に非常に感受性が高かったのに対し、PARP阻害剤単独の投与は動物内では控えめで短期間の効果しか示さなかった(同じ細胞をシャーレで扱うと強い活性を示したにもかかわらず)。 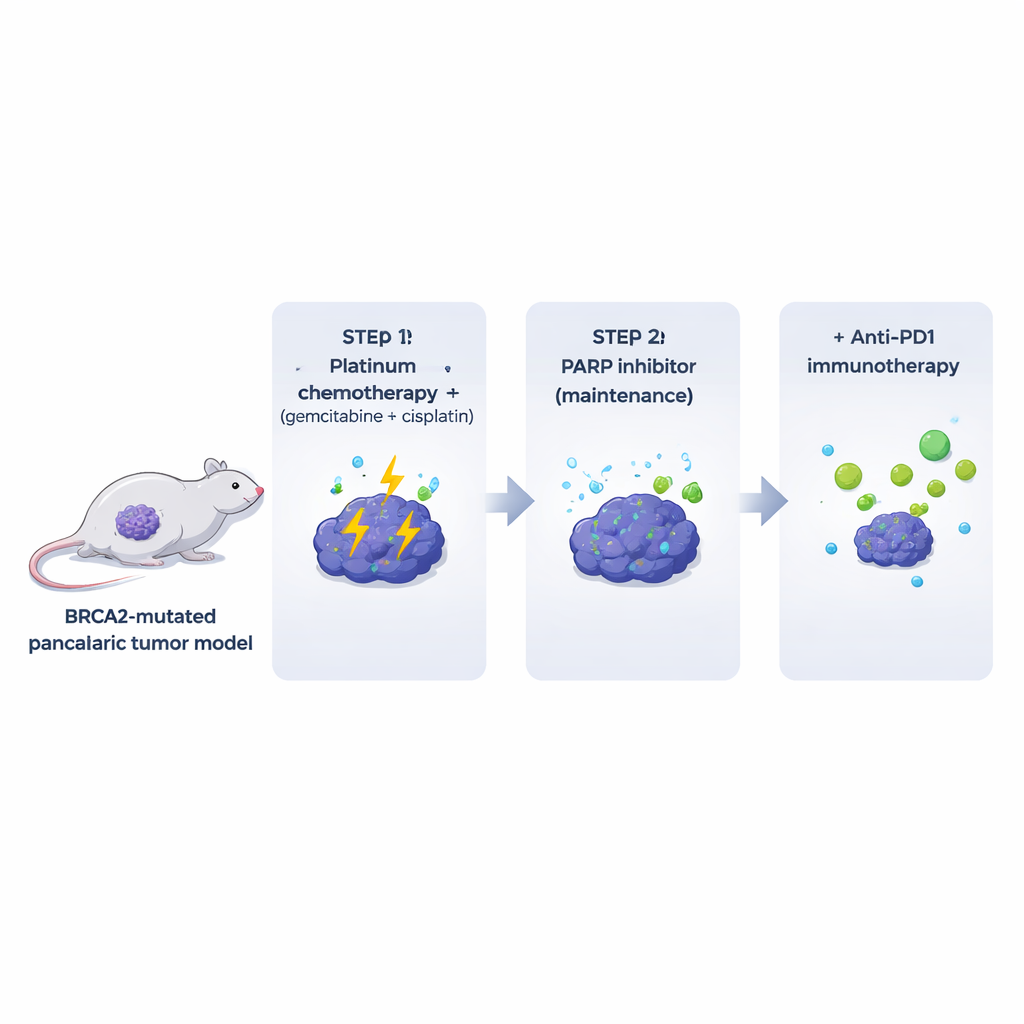
化学療法が腫瘍周囲の環境を変える
研究チームは次に、プラチナ系化学療法後に腫瘍内で何が起きるかを調べました。治療から10日後、腫瘍は縮小していたが根絶はされていませんでした。遺伝子発現解析は免疫関連の活動への顕著なシフトを明らかにしました:T細胞活性化や適応免疫に関連する経路がオンになっていました。処置後の腫瘍内にはより多くのT細胞が存在し、その多くは疲弊(エグゾースト)マーカーを示しており、活性化されたものの効果を失いつつある徴候が見られました。同様のT細胞増加パターンは、術前にプラチナ系化学療法を受けたBRCAや関連するPALB2変異を持つヒトの膵がんでも観察されました。同時に、腫瘍細胞はPD-1受容体と結合してT細胞をオフにできる表面タンパク質PD-L1の発現を上げており、腫瘍がこの新たな免疫圧に対して防御を構築していることを示唆していました。
なぜPARP単独では不十分か—耐性が生じる場所
患者治療を反映して、研究者らはマウスに最初にジェムシタビンとシスプラチンを投与し、その後PARP阻害剤オラパリブで維持療法を行いました。この順序は化学療法単独と比べて腫瘍制御と生存を改善し、事前の化学療法が腫瘍をPARP阻害に感受性にする可能性を確認しました。しかし、治癒したマウスはいませんでした:腫瘍は最終的にPARP維持下で再増殖しました。耐性腫瘍はより分化した外観を示し、発生を制御する因子CDX2の発現が大幅に増加していました。これは少なくともこのモデルでは、耐性が元のDNA修復欠損を単に修復することから生じるのではなく、腫瘍の細胞的アイデンティティの変化を伴う可能性があることを示唆します。CDX2は患者における耐性の萌芽を示すバイオマーカーになり得ます。
適切な順序で免疫療法を解き放つ
抗PD1抗体などの免疫チェックポイント阻害薬は複数のがん治療を変革しましたが、膵臓がんはほとんど反応を示しませんでした。それに一致して、治療未経験のBRCA2変異腫瘍に対して抗PD1(別のチェックポイント薬である抗CTLA4の有無を問わず)は効果を示さず、PARP阻害療法に単純に追加してもほとんど効果がありませんでした。状況が変わったのは完全なシーケンスを用いたときです:まずプラチナ系化学療法、その後にPARP阻害と抗PD1を維持療法として併用しました。この条件では、腫瘍はより深く縮小し、マウスの生存は化学療法+PARP阻害または抗PD1単独よりも長くなりました。PARP維持療法に抗CTLA4を追加しても同様の利益は得られず、化学療法で“準備された”腫瘍環境は特にPD-1阻害に反応しやすい状態になっていることを示唆しています。 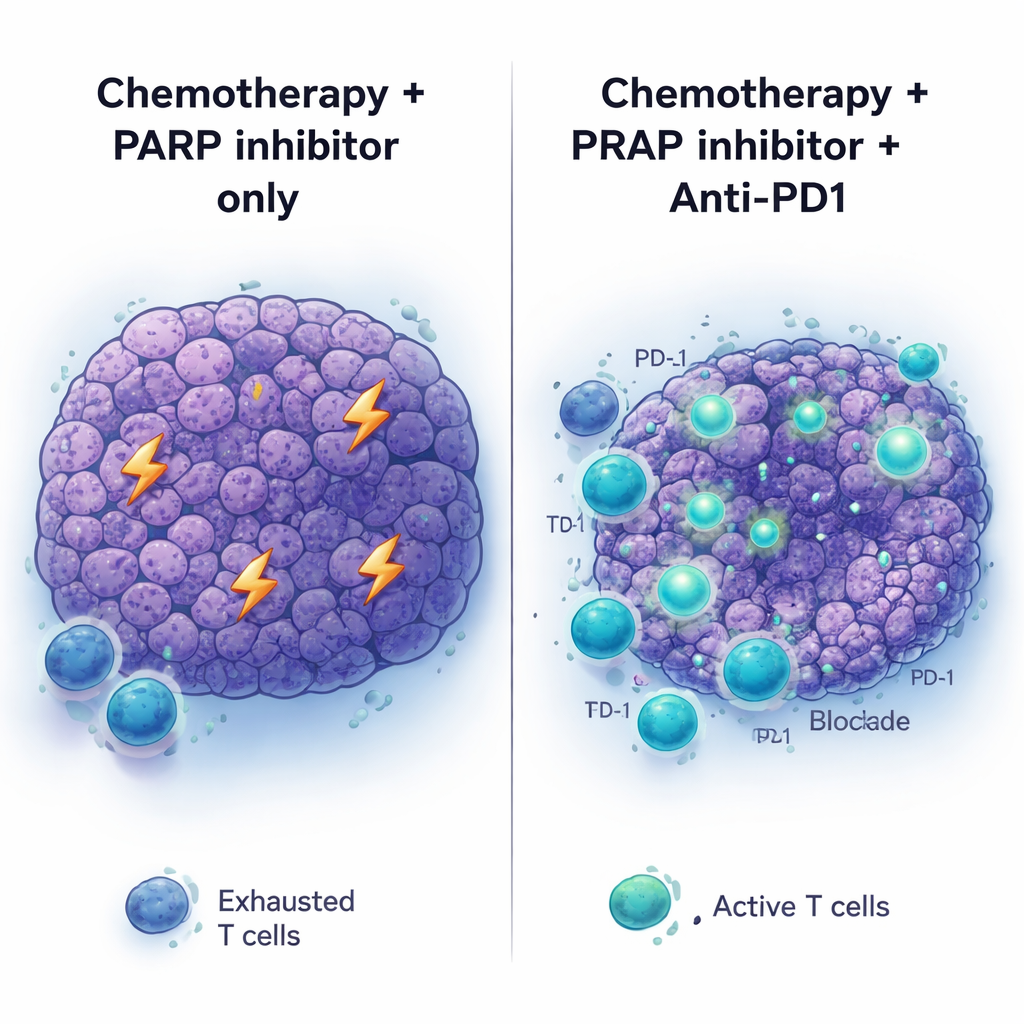
将来の治療にとっての意味
まとめると、本研究はBRCA変異を持つ膵臓がんにおいては治療の順序と組み合わせが極めて重要であることを示しています。強力なDNA損傷化学療法は腫瘍細胞を直接攻撃するだけでなく、たとえその免疫応答が当初は疲弊やPD-L1による抑制で弱められていても免疫反応をかき立てます。PARP阻害剤はその利益を延長し得ますが単独で治癒をもたらす可能性は低く、腫瘍を耐性化したCDX2高発現の状態へと駆動することがあります。プラチナ化学療法後にPARP維持へ抗PD1を重ねることで、この一時的に炎症を呈し疲弊した免疫環境をより効果的で持続的な抗腫瘍攻撃に変換できる可能性があります。BRCA関連膵臓がんでPARP阻害剤と免疫療法を組み合わせる臨床試験が進行中であり、この綿密にタイミングされた戦略が患者のより長くより良い生活へ翻訳できるかどうかを明らかにする鍵となるでしょう。
引用: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
キーワード: 膵臓がん, BRCA2変異, プラチナ系化学療法, PARP阻害剤, PD-1免疫療法