Clear Sky Science · ja
ATP13A2発現抑制に関連するミトコンドリア機能障害を介した細胞内鉄恒常性の破綻
なぜ脳細胞内の鉄が重要なのか
パーキンソン病は振戦や動作の硬さでよく知られていますが、影響を受けた脳細胞の内部では別の深刻な事態が進行しています。必須金属である鉄が、本来あってはならない場所に蓄積し始めるのです。本研究は単純だが重要な疑問を投げかけます:この鉄の蓄積はどのように起こり、神経細胞内の小さな発電所やリサイクルセンター(ミトコンドリアやリソソーム)にどのようにダメージを与えるのか?これに答えることで、パーキンソン病や関連疾患で特定の脳領域が変性する理由への手掛かりが得られ、ドーパミン補充を超えた新たな治療法の方向性が示されます。
希少な遺伝的手掛かりを詳しく見る
研究者らは、ATP13A2という遺伝子の欠陥によって生じる希少な遺伝性パーキンソン病型(PARK9)に着目しました。この遺伝子は細胞の廃棄物処理・リサイクル区画であるリソソームに存在するタンパク質を作ります。ATP13A2変異を持つ人は脳内に鉄沈着を示す症状を発症することもあり、この関連性がATP13A2を鉄バランス異常を研究する格好の出発点にしました。研究チームは、パーキンソン病関連タンパク質α‑シヌクレインを過剰発現するヒトの神経様細胞株を用い、小さなRNA断片でATP13A2の発現を低下させ、鉄、エネルギー産生、および細胞の健全性がどのように変化するかを追跡しました。
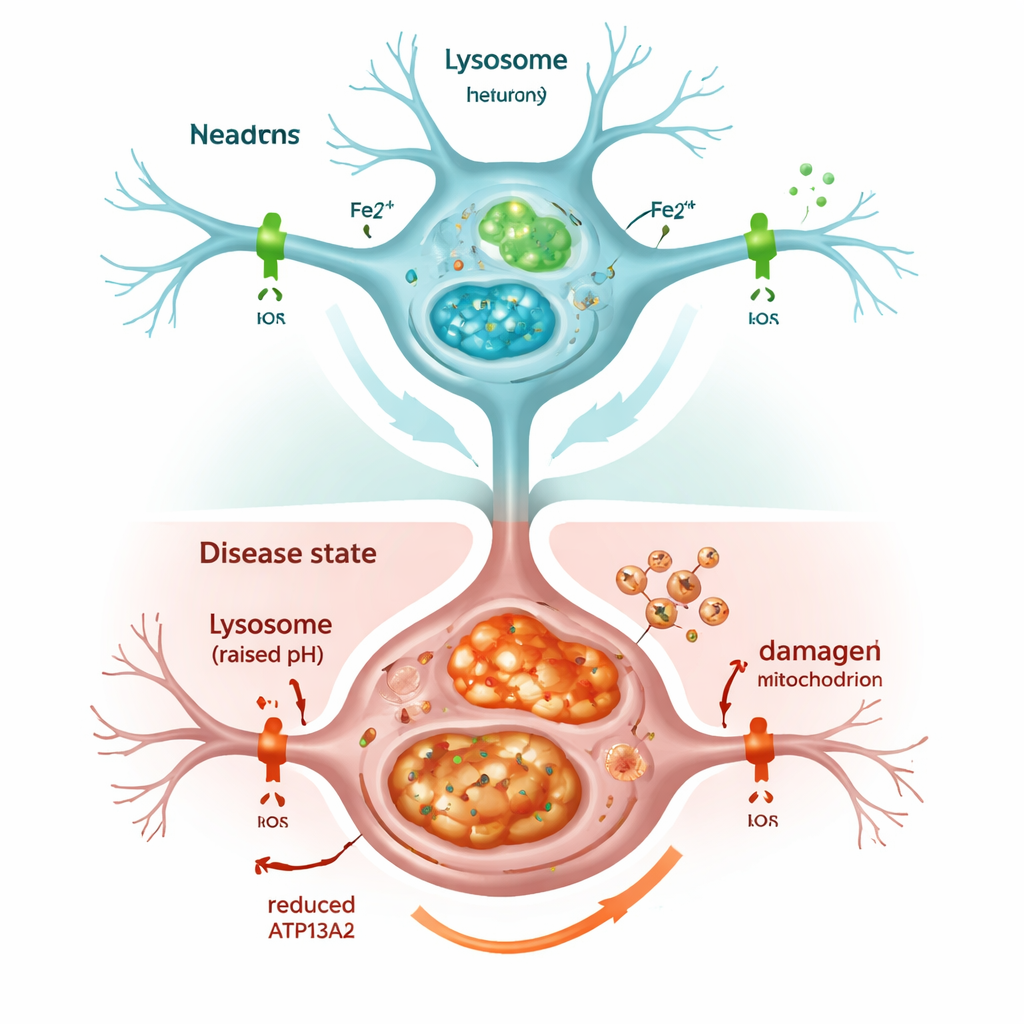
細胞のリサイクルシステムが停滞すると
ATP13A2を遮断するとリソソームは急速に弱体化しました。不要物を分解するために重要な内部の酸性度が低下し、オートファジーとして知られる細胞の掃除プロセスの指標がクリアされずに蓄積しました。その結果、α‑シヌクレインが蓄積し、パーキンソン病の脳で見られる現象を反映しました。細胞は全体的に鉄が増加し、特に化学的に活性な形態であるFe2+がリソソームとミトコンドリアの両方で増えていました。細胞は鉄を貯蔵するタンパク質フェリチンを増やして応答しましたが、それでも不十分で、過負荷となったミトコンドリアは過剰な活性酸素種を生み出し、細胞生存率は低下しました。臨床で使われるものに似た鉄結合薬で細胞を処理すると、この酸化ストレスは軽減し、細胞生存が部分的に救われ、過剰な鉄自体が損傷の主要因であることが示されました。
鉄センサーが金属の信号を聞かなくなる
通常、細胞には鉄レベルの上昇を感知して鉄取り込みを抑えるフィードバックシステムがあります。IRP2と呼ばれるタンパク質は、部分的にミトコンドリア由来のヘム依存的な信号を通じて鉄を感知し、その後、細胞表面の鉄運搬タンパク質の産生を調整します。ATP13A2欠損細胞ではこの安全装置が働きませんでした。鉄がすでに上昇しているにもかかわらず、鉄を細胞内に取り込むトランスポーターは高いままでした。IRP2タンパク質レベルはほとんど変わらず、外から余分な鉄を加えても通常の分解は誘導されませんでした。研究チームはこの故障をミトコンドリアに起因すると突き止めました:損傷したミトコンドリアは呼吸効率が低下し、ミトコンドリア品質管理(ミトファジー)の異常を示し、重要なことにヘムを作る能力を失っていました。ヘムが不足するとIRP2は「鉄過剰」の信号を受け取れず、鉄の流入を止められませんでした。
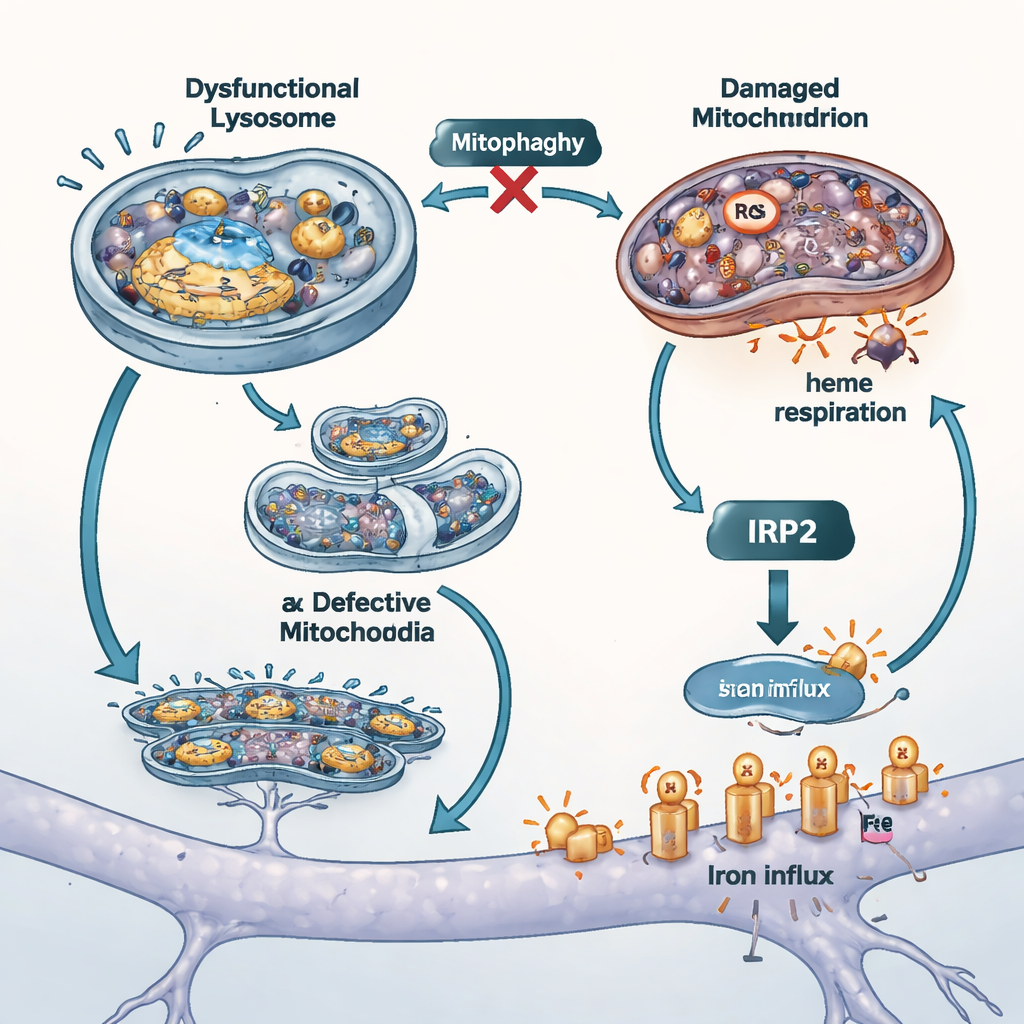
鉄の供給を遮断し、他モデルで検証する
この制御不能な鉄流入が細胞障害にどれほど寄与するかを探るため、研究者らは主な二つの鉄取り込み経路を遮断しました。一つの輸入体に対しては鉄を含まないトランスフェリンを用いて競合させ、もう一方のトランスポーターであるDMT1の活性を小さな薬で抑えました。どちらの手段も細胞内の総鉄および遊離鉄を低下させ、ミトコンドリアの酸化ストレスを減らし、生存率を改善しました。これは、ATP13A2が失われた場合、表層の鉄チャネルが損傷を増幅する重要な要因であることを示唆します。研究者らはまた、ミトファジーを損なうことが知られる別のパーキンソン関連遺伝子PINK1欠損細胞でも主要実験を繰り返しました。これらの細胞も同様に鉄の蓄積とヘム合成の低下を示し、ミトコンドリアの品質管理と鉄バランスが病態の異なる形式でも密接に結びついているという考えを支持しました。
パーキンソン病と将来の治療への意味
簡潔に言えば、本研究は悪循環の輪郭を示しています。ATP13A2が抑制されると、リソソームは損傷した構成要素(不良ミトコンドリアを含む)を除去できなくなります。弱ったミトコンドリアはエネルギーとヘムを十分に生産できなくなり、細胞の鉄感知システムが鈍ります。すると表面の鉄取り込み経路から鉄が流入し続け、脆弱な区画に蓄積して有毒反応を促進し、さらにミトコンドリアを傷害します。時間とともに、このループがパーキンソン病や関連する鉄過負荷脳疾患で特定のニューロンが死に至る理由の一端を説明し得ます。これらの所見は、将来の治療が過剰な鉄の除去だけでなく、リソソーム機能の回復、ミトコンドリア品質管理の修復、およびヘム合成の回復を目指すべきであることを示唆しており、単に金属を後から掃除するのではなく、問題の根本に対処する方向を示しています。
引用: Murakami, T., Ohuchi, K., Kiuchi, M. et al. Disruption of intracellular iron homeostasis through mitochondrial dysfunction associated with suppression of ATP 13A2 expression. Sci Rep 16, 5007 (2026). https://doi.org/10.1038/s41598-026-35368-x
キーワード: パーキンソン病, 脳内鉄, ミトコンドリア, リソソーム, ヘム合成