Clear Sky Science · ja
酵素の機能的ホットスポット残基の解析:NMRと計算手法による酵素反応のリアルタイム監視
将来の抗ウイルス薬にとってなぜ重要か
ファビピラビルはインフルエンザ治療薬として既に用いられ、COVID-19でも試験された経口薬ですが、私たちが飲む形のままではウイルスと戦いません。体内の細胞がまずそれを活性な、ウイルスを阻害する分子に変換する必要があります。本研究は、ヒトのある酵素がその重要な活性化ステップをどのように行うか、ほぼ原子レベルで解き明かし、酵素のどの微小な部分が「ホットスポット」として薬の活性化速度や効率を制御しているかを明らかにします。これらの詳細を理解することで、より強力で患者間の反応が予測しやすい次世代の抗ウイルス薬設計に道を付ける可能性があります。
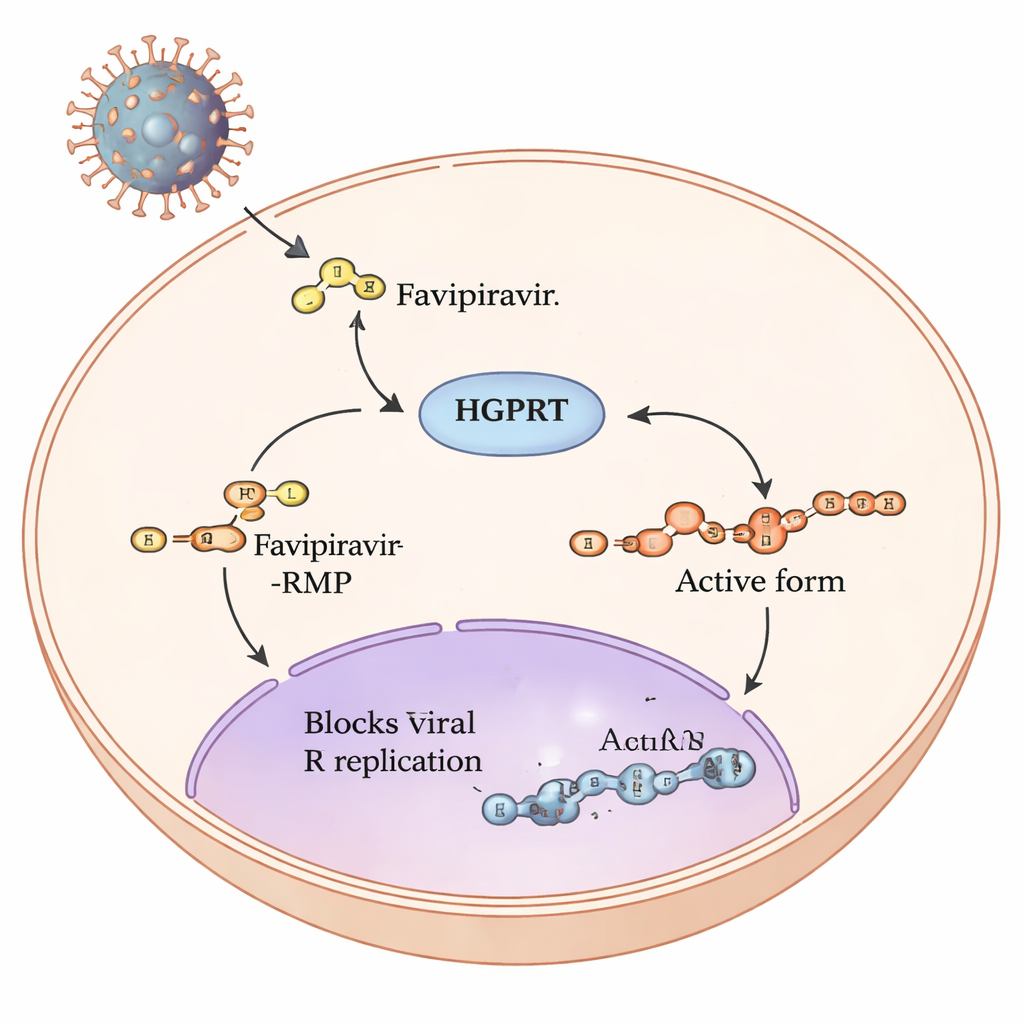
プロドラッグが細胞内をたどる道筋
ファビピラビルはいわゆるプロドラッグであり、ヒト細胞に入ると一連の化学反応によって、インフルエンザやSARS-CoV-2のようなRNAウイルスの複製機構を阻害できる形に改変されます。この経路の最初で最も遅いステップを担うのが、ヒトの酵素ヒポキサンチン-グアニンホスホリボシルトランスフェラーゼ(HGPRT)です。HGPRTはファビピラビルに糖-リン酸基を付加してファビピラビル-RMPを生成します。この段階を経てはじめて、他の酵素が完全に活性なトリホスフェート形へと変換し、ウイルスのRNAポリメラーぜを直接阻害します。最初のHGPRT駆動ステップが活性化薬の生成量に対するボトルネックとなるため、著者らはHGPRTのどの部分がファビピラビルの処理に最も重要かを突き止めようとしました。
NMRで化学反応をリアルタイム観察
特異な点として、ファビピラビルは磁場中で小さな無線送信器のように振る舞うフッ素原子を含みます。研究チームはこれを利用し、フッ素-19核磁気共鳴(NMR)分光法で反応の進行に伴い試験管内に存在するファビピラビルとファビピラビル-RMPの量をリアルタイムで観察しました。フッ素を持つのは薬だけであるため、NMR信号は雑音が少なく追跡しやすいという利点があります。12時間にわたり繰り返しスペクトルを記録することで、出発物質の減少と生成物の増加を追い、反応速度や酵素の見かけの結合の強さといった標準的な動力学指標を抽出できました。
酵素の鍵となる位置を調整する
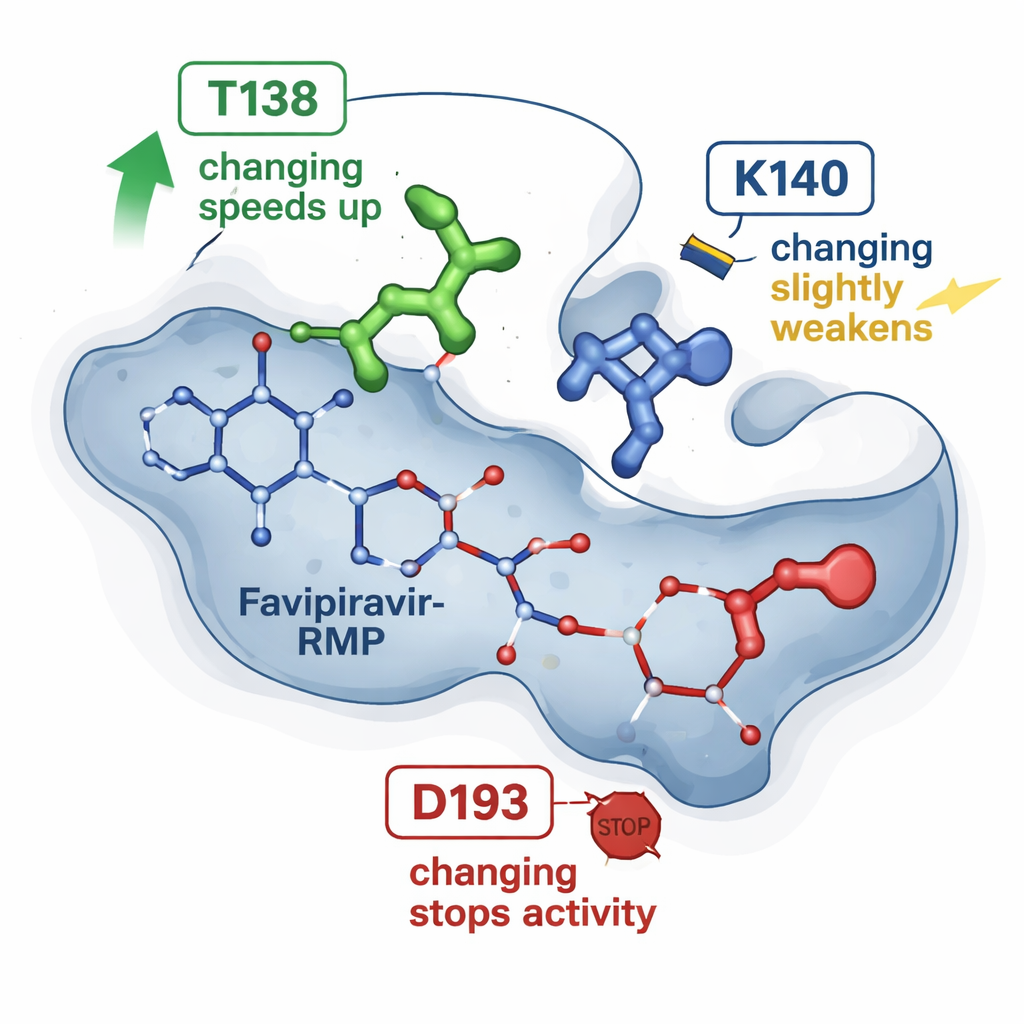
以前のX線結晶構造でHGPRTがファビピラビル-RMPを抱えているスナップショットから、薬を取り囲むいくつかのアミノ酸が示唆されていました。新しい研究ではそれらの位置のうち3つを正確な一文字置換で変更し、各変異体酵素を天然型と比較しました。1つの変化(T138Aと命名)は予想外に酵素を約4〜6倍速くファビピラビルを変換するようにし、薬を保持するのに役立つと考えられていた化学基を失っているにもかかわらず速度が上がりました。2つ目の変化(K140M)は反応をやや遅くし、見かけ上の結合をわずかに弱めました。3つ目の変化(D193N)は、変化したタンパク質が生成物を結合できるにもかかわらず、ファビピラビル-RMPを作る能力を完全に失わせました。これらの結果は、接触点がすべて同等ではないことを示しています:あるものは繊細な速度調節子として働き、別のものは不可欠なスイッチとして機能します。
計算機上で動きをシミュレートする
静的な構造を超えて見通すため、研究者らは分子シミュレーションに取り組みました。既知の三次元構造であるHGPRTとファビピラビル-RMPを出発点に、確立された計算ツールを用いて各変異体で薬がどれほど強く結合するかを推定し、多数の短い分子動力学シミュレーションを実行しました。これらのシミュレーションは、原子が数十ナノ秒の間にどのように揺れ動き相互作用するかを追跡します。計算結果はNMR由来の傾向と一致しました:T138A変異体はファビピラビル-RMPをより好ましく保持する傾向を示しつつも、薬が放出へ向かう“脱出”経路に移動するエピソードも観察されました。その経路は、リン酸基を一時的に固定してから放出する別の残基(K140)に導かれていました。一方でD193N変異体は生成物を保持しているように見えるものの、マグネシウムイオンを必要とするより早い触媒ステップで失敗している可能性が高く、安定した結合があるにもかかわらず活性を失った理由を説明します。
より賢い抗ウイルス薬設計へのロードマップ
リアルタイムNMR測定と詳細な計算モデルを組み合わせることで、本研究はファビピラビルの活性化効率を支配するHGPRTの機能的ホットスポットをマップしました。専門外の読者への要点は、私たち自身の酵素が細胞内でどれだけ活性な抗ウイルス薬が蓄積されるかに強く影響し得ること、そして薬の形状や酵素のポケットのいずれかを調整することでその結果が劇的に変わり得ることです。著者らのハイブリッド戦略は、他の薬剤が標的タンパク質とどのように相互作用するかを調べる一般的な設計図を提供し、体内の活性化機構により適合した新しい抗ウイルス化合物の開発を加速する可能性があります。
引用: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
キーワード: ファビピラビル, 抗ウイルス剤の活性化, HGPRT酵素, NMR分光法, ドラッグデザイン