Clear Sky Science · ja
多重免疫蛍光データのための空間情報を取り入れたパターン解析
腫瘍細胞の「近隣」が重要な理由
膵臓がんは最も致死率の高いがんのひとつであり、その一因は腫瘍が免疫細胞や支持細胞からなる複雑な「近隣空間」の中に存在し、これらの細胞ががんと戦うこともあれば、がんを隠す手助けをすることもある点にあります。本研究は顕微鏡画像におけるこれらの細胞の空間的配置を読み取る新たな手法を提案し、侵襲性の高い膵管腺がん(PDAC)と、その前がん病変である乳頭粘液性管内腫瘍(IPMN)で免疫系がどのように異なる振る舞いをするかを明らかにします。こうした隠れたパターンの理解は、より良い診断やより的確な治療法の指針になり得ます。
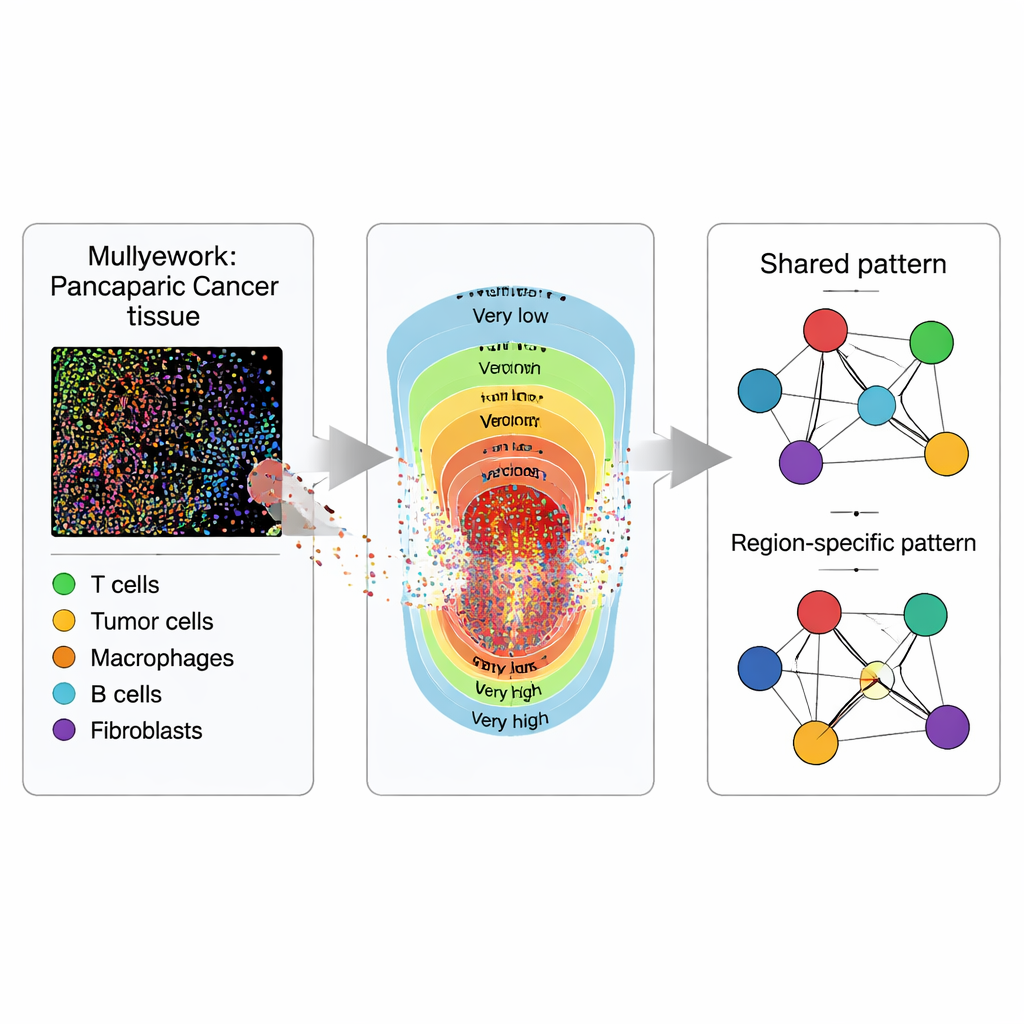
組織を単なる画像ではなく地図として見る
研究者たちは腫瘍切片を平面的な画像として扱うのではなく、点が並ぶ地図として扱います。多重免疫蛍光イメージングを用いて、119例のPDACと53例のIPMNの組織試料を染色し、異なる細胞種がそれぞれ別の色で可視化されます。専用ソフトウェアは観察される各細胞を座標とラベルを持つ点に変換します:腫瘍(上皮)細胞、攻撃的または免疫を調節するさまざまなタイプのT細胞、そして腫瘍断片をT細胞に提示する抗原提示細胞などです。重要なのは各細胞が何個存在するかだけでなく、組織内で互いにどのような位置関係にあるかです。
腫瘍をゾーンに分割する
腫瘍が中心から周辺に向かってどのように変化するかを捉えるために、各組織試料は腫瘍細胞の密度に基づいて「非常に低い」から「非常に高い」までの5つのゾーンに分けられます。これらのゾーンは、病理医が顕微鏡でしばしば観察するが定量化されることの少ない腫瘍負荷や細胞の混雑度のグラデーションを表しています。各ゾーン内でチームは各細胞種について平滑化した“強度マップ”を推定し、散在する点を連続的なヒートマップに変換して各細胞種がどこに集まりやすいかを示します。このゾーニングによって、細胞間の相互作用を全体として比較できるだけでなく、希薄な領域から高密度領域へのシフトに伴う相互作用の変化も比較できます。
細胞の近隣関係をネットワークに変換する
次に、研究者たちは空間パターンをネットワークへと翻訳します。各細胞種をノードとし、リンクは他のすべてを考慮した上で二つの細胞種が一緒に現れる強さを表します。ISPat(Informed Spatially aware Patterns)と名付けたベイズ統計フレームワークを用い、全ゾーンに共通する特徴とゾーン固有の特徴を分離します。ISPatは利用可能な生物学的事前知識を組み込むこともでき、複雑なデータに対する推定の安定化に寄与します。シミュレーション実験では、ISPatは既知のパターンを確実に再現し、従来法に比べてはるかに高速に処理できることが示されており、大規模なイメージング研究に実用的です。
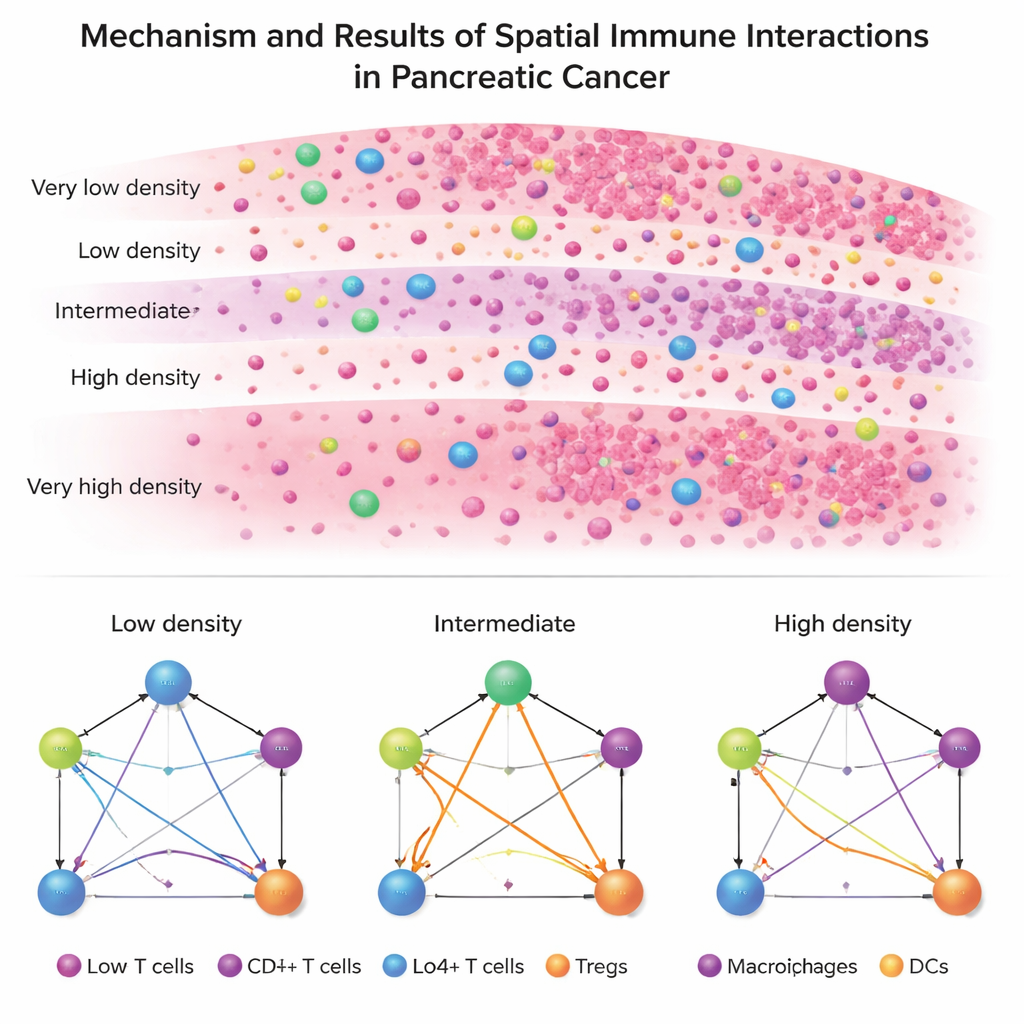
二つの疾患、二つの免疫構造
ISPatを実患者データに適用すると、PDACとIPMNの間で顕著な対照が浮かび上がります。PDACは硬直化した均質な免疫構造を示し、ほぼすべてのゾーンで腫瘍細胞、ヘルパーT細胞、キラー(細胞傷害性)T細胞、制御性T細胞、抗原提示細胞がほぼ同じ関係パターンを保っています。これは除去し難い安定した免疫抑制的環境が確立していることを示唆します。対照的に、IPMNはゾーンごとの差異がはるかに大きく、とくに制御性T細胞が他の免疫細胞とどう結びつくかにおいて変動が目立ちます。IPMNでは、腫瘍細胞で完全に埋まっているわけでもほとんど腫瘍がないわけでもない中間密度のゾーンで免疫相互作用の再形成が最も劇的に起きています。
免疫回避と治療のホットスポット
さらに掘り下げると、本研究はPDACとIPMNで一貫して異なる相互作用を示す特定の細胞対を特定します。これらの多くは免疫攻撃を抑えることのできる制御性T細胞、抗原提示を行う細胞、腫瘍を直接攻撃するキラーT細胞を含みます。特に抗原提示や直接的な腫瘍細胞殺傷を促す相互作用、そして免疫抑制を強化する相互作用が、最も極端な腫瘍領域ではなく中間のグラデーション領域で最も鋭く分岐します。このパターンは、腫瘍と免疫系がまだ積極的にせめぎ合っている過渡的なゾーンが免疫制御の重要な戦場であることを示唆しています。
患者への意味
専門外の方への要点は、腫瘍内で細胞がどこに位置するかが、どの細胞が存在するかと同じくらい重要だということです。PDACは安定して抑制的な免疫“配置”を固定化している一方で、IPMNの免疫景観はより柔軟で領域依存的です。こうした空間的な指紋は、危険な腫瘍と前がん病変を区別したり、どの患者が特定の免疫療法の恩恵を受けやすいかを予測するバイオマーカーになる可能性があります。ISPatのフレームワークは、多くの疾患でこうした空間コードを読み取るための汎用的なツールを提供し、がん治療が遺伝学や細胞型だけでなく、各患者の腫瘍内における細胞の細かな地理に基づいて導かれる未来を支えます。
引用: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
キーワード: 膵臓がん, 腫瘍微小環境, 空間イメージング, 免疫相互作用, 精密医療