Clear Sky Science · ja
近接バイオチニル化用途のためのリジン非含有RECタグシステム
タンパク質に小さなタグが重要な理由
細胞の内部では、タンパク質が単独で働くことはまれで、健康や病気を左右する流動的なパートナーシップを組んでいます。これらの連携を調べるために、研究者はしばしばタンパク質に小さな「名札」を付けて追跡したり、混合物から引き出したり、顕微鏡で可視化したりします。近接バイオチニル化という一般的な手法は、細胞内で誰が誰の近くにいるかをマップするのに有効ですが、隠れた問題があります:多くのこうした名札は化学的に修飾されてしまい、最も必要とされるときに事実上「見えなく」なってしまうのです。本研究は、こうした過酷な条件下でも視認性を保つよう設計された新しいタグ、RECタグを紹介します。
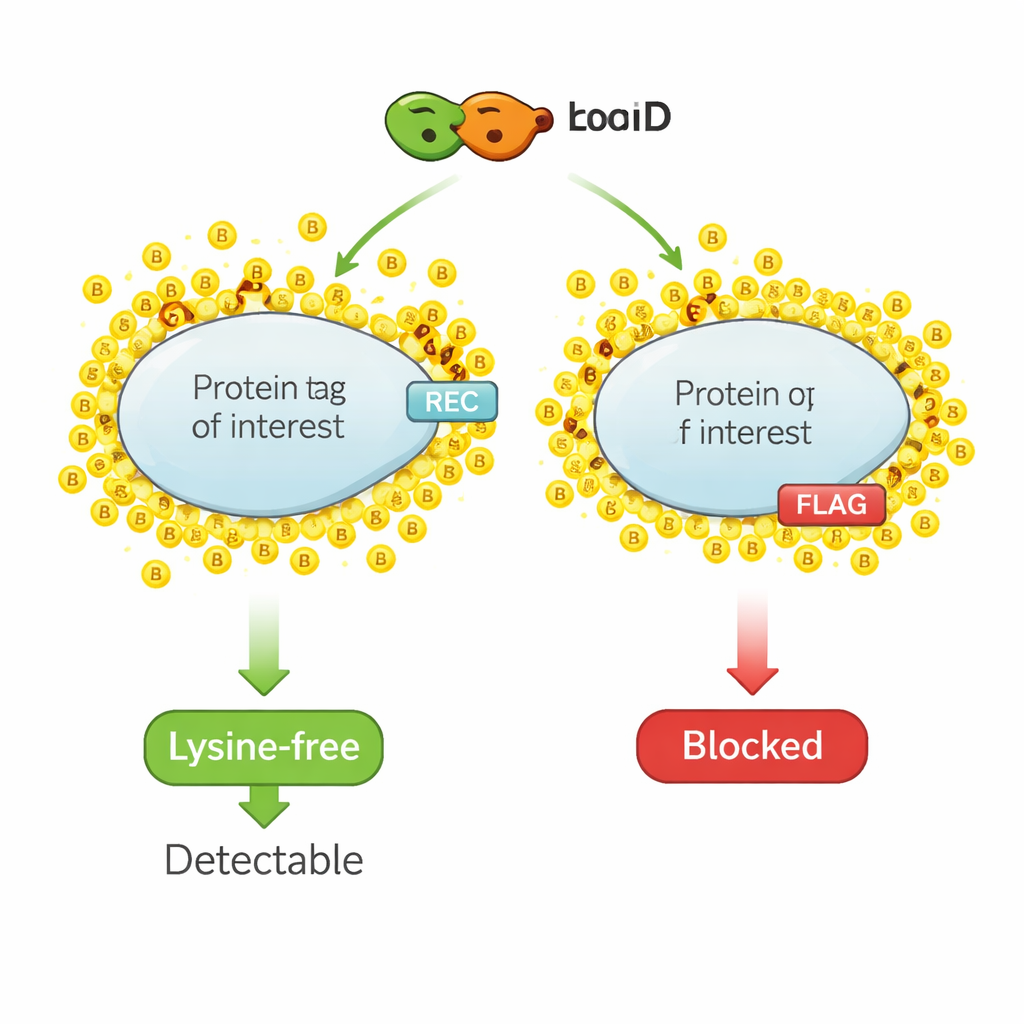
タンパク質近傍をマーキングする化学的ハイライター
近接バイオチニル化は分子レベルのハイライターペンのように働きます。TurboIDのような設計酵素を興味のあるタンパク質に融合させ、ビオチン(小さなビタミン)を加えると、TurboIDが急速に近傍のタンパク質へビオチン分子を付加します。研究者はその後、ビオチンで標識されたタンパク質を回収して同定し、タンパク質の局所的な近隣関係のスナップショットを得ます。しかし、近傍のタンパク質を標識する同じ化学反応が、検出に一般的に使われる小さなエピトープタグにも作用します。というのも、これらのタグは通常リジンというアミノ酸を含み、ビオチンが結合しやすい主要な部位だからです。タグ中のリジンがビオチンで修飾されると、抗体がタグを認識できなくなり、標準的な検出法でのシグナルが低下したり消失したりします。
修飾を拒むタグの設計
この問題を解決するため、著者らはリジンを一切含まない新しいタグを作ることに着手しました。出発点としてマラリア寄生虫のタンパク質断片であるPfRipr5を用いました。PfRipr5はヒトタンパク質と類似性が低く、望ましくない交差反応のリスクを下げます。ラビットを用いたマイクロチップベースのスクリーニング法でPfRipr5に対する22のモノクローナル抗体を作製し、そのうち特に結合が強く特異的なクローンNo.6を同定しました。PfRipr5断片を系統的に切り詰めおよび変異導入することで、抗体の標的を11アミノ酸の領域まで絞り込みました。この最小配列には1つだけリジンが含まれていたため、それを類似のアミノ酸であるアルギニンに置換しました。驚くべきことに、抗体はほぼ同等に結合し続けました。この最適化されたリジン非含有配列をRECタグと名づけ、対応する抗体をREC抗体と呼びました。
RECタグの実地試験
研究チームは次に、RECタグが一般的に使われるFLAGのようなタグの代替になり得るかを検証しました。蛍光タンパク質やシグナルタンパク質に融合して細胞外翻訳系および哺乳類細胞で発現させたところ、RECタグ付加タンパク質はウェスタンブロット、感度の高いプレートアッセイであるAlphaScreen、細胞内での免疫染色により容易に検出されました。検出の強度はFLAGタグや別のリジン非含有タグシステム(AGIA)と同等で、REC抗体はさまざまなヒトおよびサルの細胞株において背景ノイズが非常に低いことを示しました。重要なのは、タグがタンパク質のN末端またはC末端に配置されても機能し、核、ミトコンドリア、粗面小胞体、細胞膜など多様な細胞内局在を持つタンパク質でも有効だった点です。
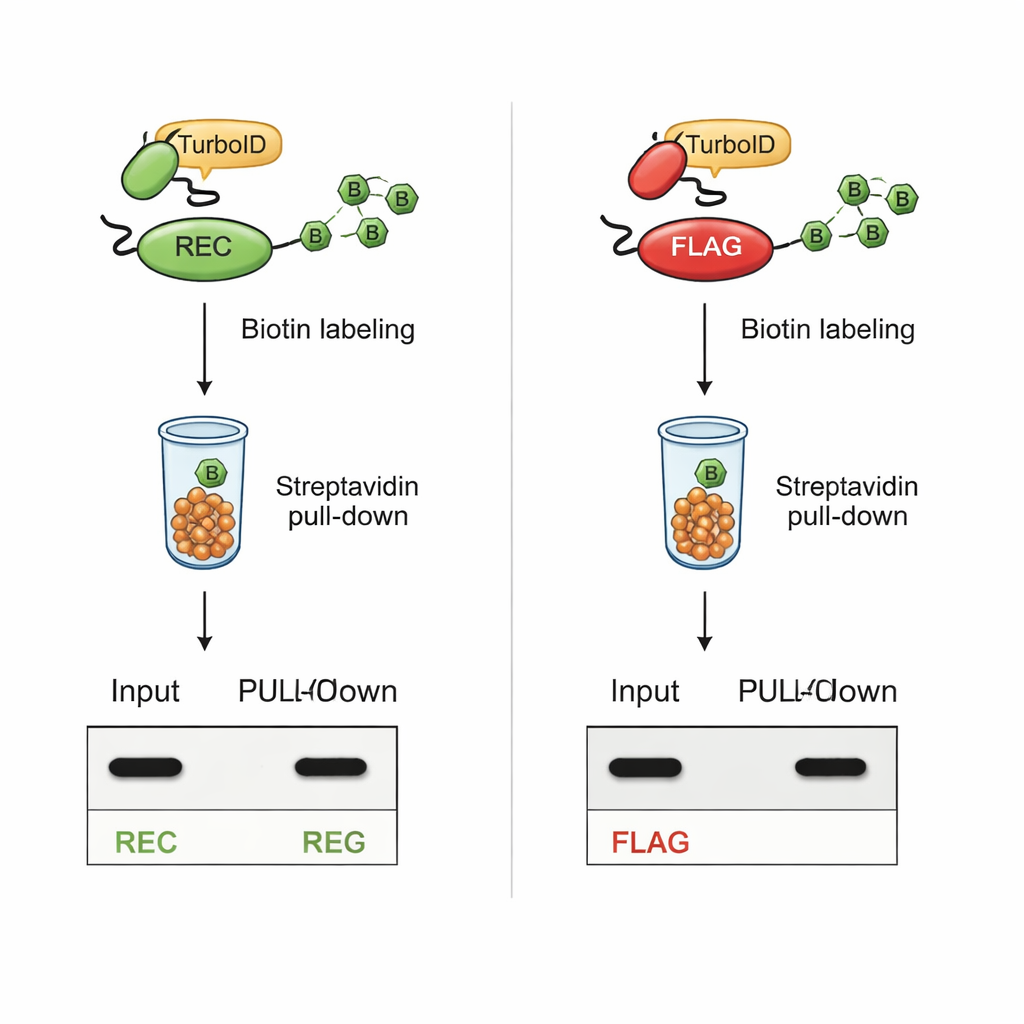
集中的な標識下でも視認性を維持
重要な試験は、TurboIDベースのビオチニル化後にRECが検出可能であり続けるかどうかでした。TurboIDが既知の相互作用パートナーに融合された細胞では、RECタグを持つタンパク質は全細胞抽出物および精製されたビオチン標識分画の両方で明瞭に検出され続けました。これに対して、従来のFLAGタグを持つタンパク質は、TurboIDが活性化されるとFLAGシグナルを失いましたが、タンパク質自体は存在していました。合成ペプチドを用いた追加実験により、TurboIDがFLAG配列中のリジンを直接ビオチニル化して抗体のアクセスを物理的に遮断することが示されました。リジンを全く含まないRECタグはTurboIDによる影響を受けず、検出が容易なままでした。
今後の実験への意義
生きた細胞内のタンパク質ネットワークを探る研究者にとって、RECタグは実用的な新ツールを提供します:日常的なアッセイでは既知のタグと同様に振る舞いながら、強力な近接標識酵素が働いている状況でも機能し続けます。これにより、タグ付けしたタンパク質が確実に存在し正しく捕捉されていることをより信頼して確認でき、タグ自体が干渉することなくユビキチン化やアセチル化など他のリジン基質の修飾を研究できます。要するに、RECは小さな設計変更でありながら大きな効果をもたらし、複雑なタンパク質マッピング実験をより明瞭で信頼できるものにします。
引用: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
キーワード: タンパク質タグ付け, 近接バイオチニル化, TurboID, タンパク質相互作用, エピトープタグ