Clear Sky Science · ja
全身性アミロイドーシスに対する抵抗性の生化学的基盤の評価
小さなタンパク質の変化が致命的な蓄積を阻むとき
関節リウマチから結核に至る多くの慢性炎症性疾患は、稀ではあるがしばしば致命的となる合併症、全身性AAアミロイドーシスを引き起こすことがある。この状態では、通常の血中タンパク質が硬い繊維として蓄積し、臓器を詰まらせる。本研究は驚くほど希望に満ちた問いを投げかける:そのタンパク質に起こる小さな自然変異が、一部の動物を病気に対してほぼ免疫にすることがあり得るのか――もしそうなら、その仕組みは何か?
タンパク質の蓄積が隠す脅威
AAアミロイドーシスは、血中の炎症性指標である血清アミロイドA(SAA)の増加から始まる。重度または長期にわたる炎症の際、SAAの濃度は通常値の何千倍にも跳ね上がることがある。人や動物の一部では、このタンパク質の一部が誤った折りたたみを起こし、アミロイド線維と呼ばれる長い繊維状に積み重なって脾臓や腎臓などの臓器に広がる。時間の経過とともにこれらの繊維は臓器機能を損なう。しかし、SAAが高値になったすべての個体がアミロイドーシスを発症するわけではなく、特定のマウス系統は実験室で病気に誘導されても驚くほど抵抗性を保つことがある。その理由を理解できれば、人間のアミロイド蓄積を防ぐ新たな戦略につながる可能性がある。
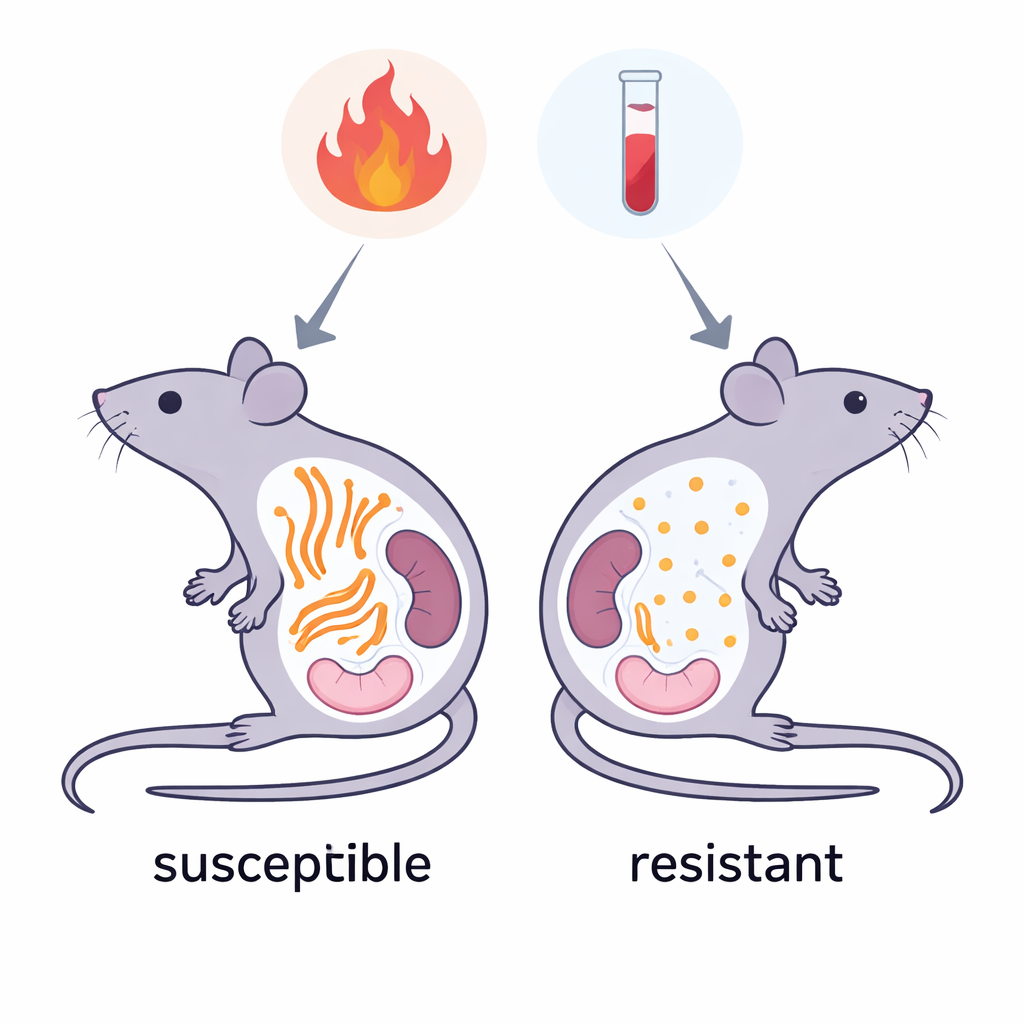
抵抗性マウスと彼らの特別なタンパク質バージョン
マウスでは、ほとんどのAAアミロイド線維はSAA1.1と呼ばれるSAAの一つのバージョンから生じ、これは疾患と強く関連している。しかし、あるマウス系統は主にわずかに変化したバージョン(SAA1.5やSAA2.2)を産生し、これらの系統は全身性AAアミロイドーシスをほとんど発症しない。これらのタンパク質はアミノ酸のわずかな違いしかないが、それらの変化は疾患を引き起こす繊維の内部コアを形成するきっちり詰まった領域に集中している。研究者らは、これらの小さな違いがタンパク質の凝集そのものを止めるのではなく、有害な特定の線維形状を採ることを阻害しているのではないかと提案した。
試験管内でタンパク質を検証する
この仮説を検証するため、研究チームは3種のマウスSAA変異体をすべて大腸菌で発現させ、試験管実験でその挙動を観察した。アミロイドが形成されると蛍光を発する色素で線維形成を追跡し、電子顕微鏡で構造を確認した。疾患に結び付くSAA1.1は長くまっすぐな線維を容易に形成した。SAA2.2も線維を形成し得たが、それらはより太くねじれがあり構造の多様性が大きく、同じ強い蛍光シグナルを引き起こさなかった。対照的にSAA1.5は、試験した条件下で線維を形成できなかった。研究者が病気のマウス脾臓から採取した実際の病的線維の微量サンプルを「シード」として加えると、SAA1.1は元の構造を忠実に模した新しい線維を急速に成長させ、まるでプリオンのように振る舞った。注目すべきことに、SAA1.5とSAA2.2はこれらのシードにまったく増殖せず、ex vivo(外部由来)の線維はそれらを病原性の形に取り込むことができなかった。
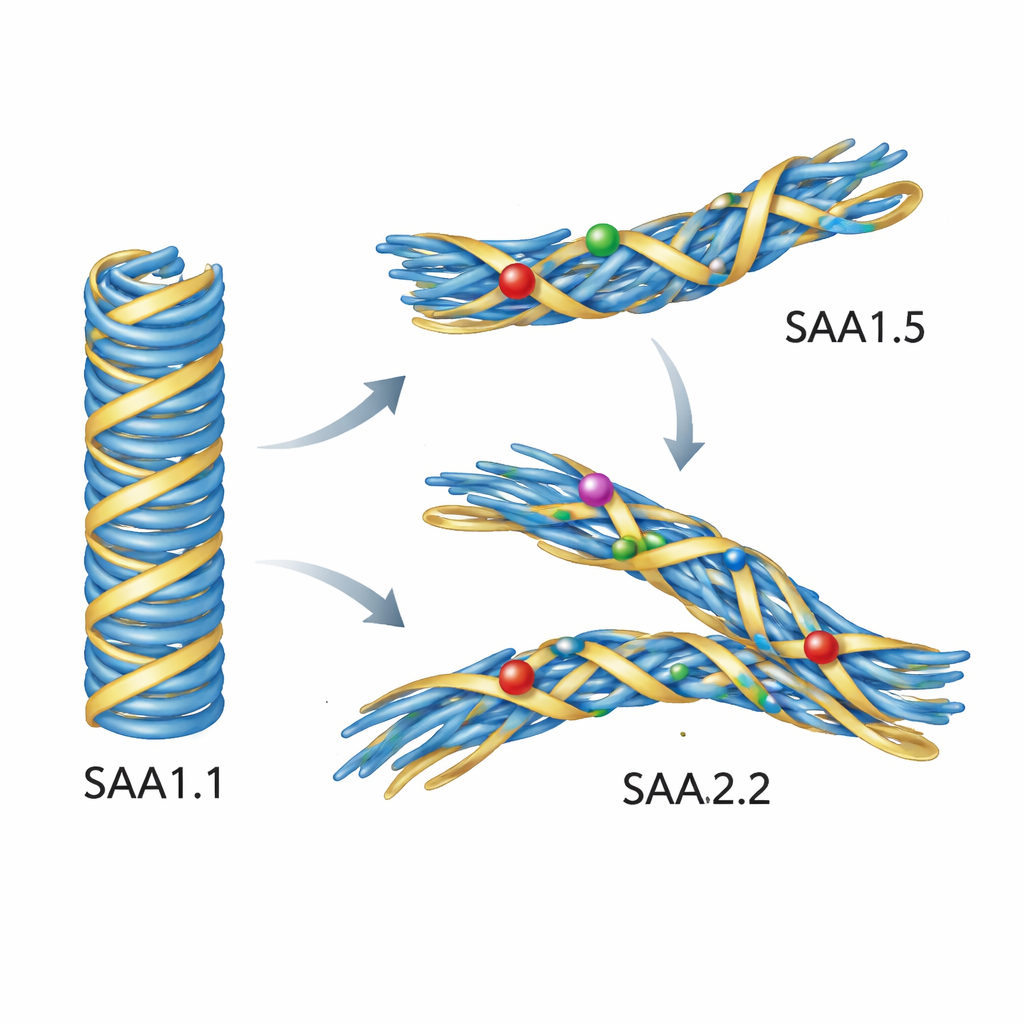
シミュレーションが示す、変異タンパク質が有害な形を拒む理由
実験だけでは原子レベルで正確に何が起きているか示せないため、著者らは詳細なコンピュータシミュレーションに取り組んだ。まずSAA1.1由来の病的なマウスAA線維の高解像度構造を出発点とし、そこにSAA1.5やSAA2.2の配列を計算的に置き換えた。これらの線維を体温の水中でシミュレートすると、SAA1.1基盤のモデルは驚くほど安定に保たれた。一方、SAA1.5やSAA2.2から構築した線維はずれや歪みを起こした。コアの鍵となるループ領域が外側に動き、タンパク質の始端領域との接触が緩み、いくつかの側鎖が新しい配向に反転した。これらの微妙な再配置が、病原性フォールドを定義する密な詰まりを乱した。言い換えれば、変異配列は一般的に線維を形成することを嫌わないが、病的なAA線維の設計図に心地よくはまることができなかったのだ。
自然のデザインが示す将来の治療の示唆
総じて、この研究は「アミロイドに抵抗性のある」マウス系統が保護されているのはSAAがまったく凝集できないからではないことを示している。むしろ、彼らのSAAは全身性AAアミロイドーシスを引き起こす特定の線維形状と構造的に相容れないのだ。タンパク質は依然として凝集し得るが、代わりに見かけ上無害な別の形態で凝集する。類似の保護的変異は、いくつかのプリオン病やアルツハイマー病の症例でも知られている。これはより広い原理を示唆する:疾患を起こしやすいタンパク質がその有害な構造を採らないようにわずかに改変することで――その機能を保ちつつ――病気を防げる可能性がある。長期的には、これら自然由来の「抵抗性」変異やそこから派生した短い断片に着想を得た治療法が、タンパク質を有害な折りたたみから遠ざけ、無害な折りたたみへと導く助けになるかもしれない。
引用: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
キーワード: AAアミロイドーシス, 血清アミロイドA, タンパク質の誤った折りたたみ, アミロイド抵抗性, マウスモデル