Clear Sky Science · ja
血液遺伝子発現データからの深層学習とXAIに基づく解釈可能な特徴選択によるアルツハイマー病予測
この研究が重要な理由
アルツハイマー病は記憶や自立を徐々に奪いますが、現在最も精度の高い検査は高価で侵襲的、反復が難しい脳画像や腰椎穿刺を必要とすることが多いです。本研究は、より負担の少ない代替手段を検討します。すなわち、単純な採血と高度な計算解析を組み合わせて、アルツハイマーを示す遺伝子活動のパターンを見つけ出すことで、より早期かつアクセスしやすい診断につながる可能性を探っています。
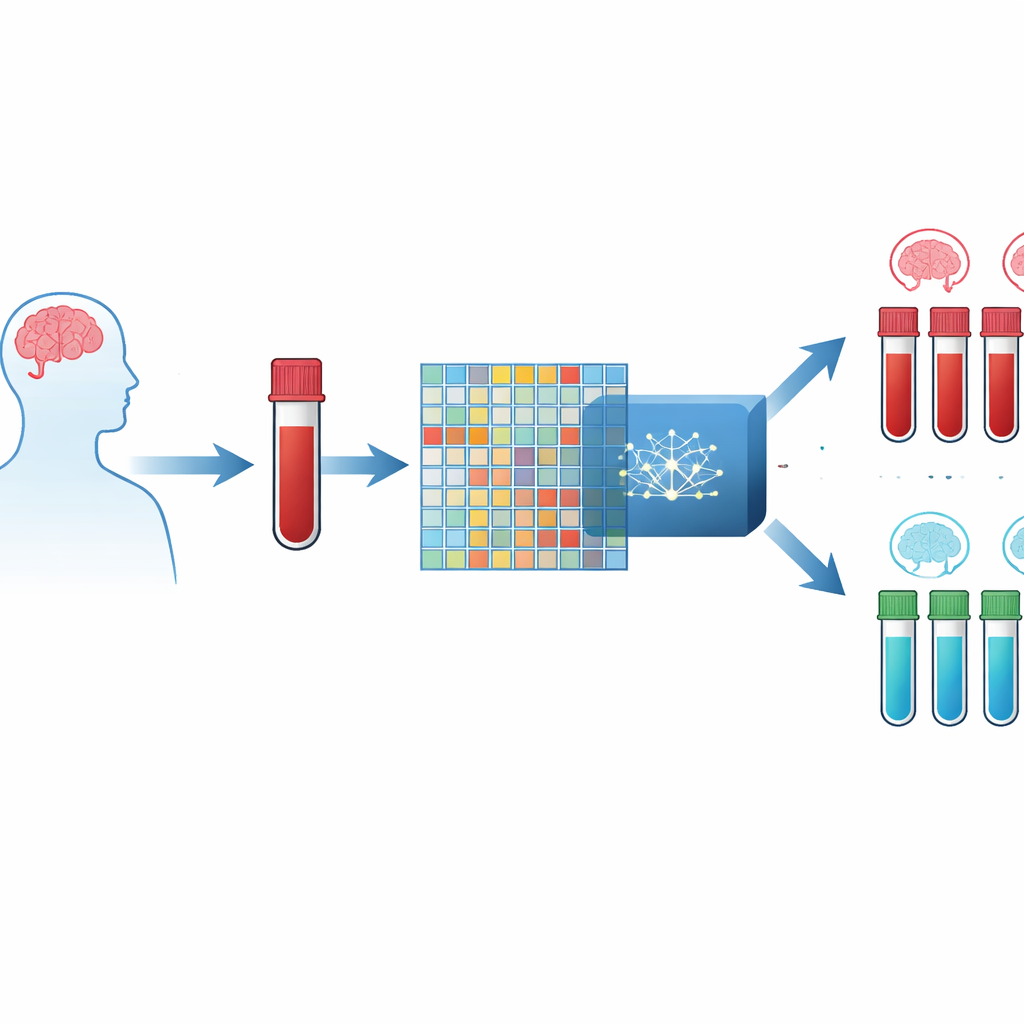
脳スキャンの代わりに血液検査
著者らは血中細胞での遺伝子のオン・オフのわずかな変化に着目しています。現代のマイクロアレイやシーケンサーチップは何千もの遺伝子の活動を同時に測定でき、各個人について膨大な数値の表を生成します。問題は、患者数より遺伝子測定数の方が圧倒的に多く、コンピュータモデルが誤った学習をしやすい点です。これに対処するため、研究者たちはアルツハイマー患者と健康なボランティアの血液サンプルを含む三つの大規模公開データセットを統合し、数百人規模で共通に測定された1万二千以上の遺伝子を備えた資源を作成しました。
重要な警告サインを選ばせる学習
アルゴリズムに1万二千の遺伝子すべてを処理させるのではなく、まず極めて情報量の多いごく小さな遺伝子群を選ぶよう教えました。単純な統計検定、段階的に重要度の低い遺伝子を除去する手法、選択をモデル内に組み込むアプローチなど、複数の方法を比較しました。こうした「特徴選択」ツールにより、患者と健常者を最もよく区別する数百からせいぜい千少々の遺伝子に絞り込めました。遺伝子セットを絞ることでモデルがノイズを丸暗記するのを防ぎ、未見データでの性能を向上させました。
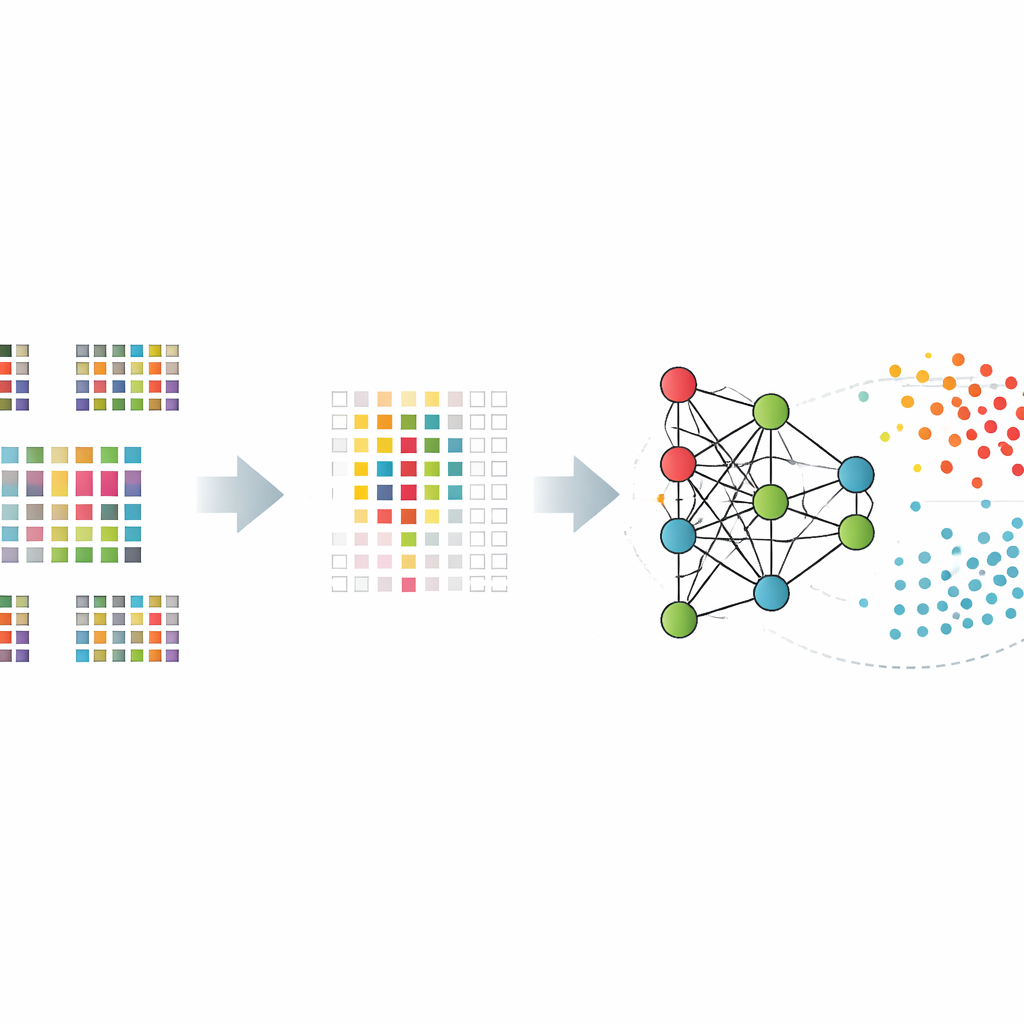
ブラックボックスを理解する
ブラックボックス予測を盲信しないために、研究者たちは説明可能な人工知能(XAI)技術を用いて、どの遺伝子がどれほど重要で、各判定にどのように影響したかを解析しました。ゲーム理論から借用したSHAPと呼ばれる手法は、各遺伝子が個々の最終結果にどれだけ寄与したかをスコア化します。最も性能の良かったモデルにこれを適用することで、アルツハイマーと健常のいずれかへ一貫して傾けるコアな遺伝子群が浮かび上がりました。これらの多くは既に脳の健康や免疫機能と関連付けられており、モデル内部の挙動に生物学的な信頼性を与えています。
合成患者で検出力を強化
データセットを統合しても実際の血液サンプル数は限定的でした。モデルを強化するため、著者らは敵対的生成ネットワーク(GAN)と呼ばれる特殊なニューラルネットワークを訓練し、実際の患者に似た現実的な合成遺伝子プロファイルを生成しました。これらの人工サンプルは訓練データにのみ追加され、テストデータには一切使われなかったため、性能評価の公正性は保たれています。この拡張訓練セットと注意深く選ばれた遺伝子群により、深層ニューラルネットワークは全体で約91%の正解率と95%の精度を達成し、健康な人が誤って病気と判定される割合を非常に低く抑えられました。
患者にとっての意味
この研究は、重要な遺伝子信号を選択・説明する賢いアルゴリズムによって支えられた将来の血液ベースのアルツハイマー検査が、高価なスキャンや侵襲的手技を補完または軽減する可能性を示唆します。独立した患者群でのさらなる検証や測定手法間の差異のより厳密な管理が必要ですが、複数データセットの統合、無益な情報の削減、AIのブラックボックスの可視化を組み合わせることで、より実用的で解釈可能な血液検査に近づけることを示しています。
引用: Hariharan, J., Jothi, R. Alzheimer’s disease prediction using deep learning and XAI based interpretable feature selection from blood gene expression data. Sci Rep 16, 8022 (2026). https://doi.org/10.1038/s41598-026-35260-8
キーワード: アルツハイマー診断, 血液バイオマーカー, 遺伝子発現, 深層学習, 説明可能なAI