Clear Sky Science · ja
Snhg5の喪失は嚢胞形成を変えずに細胞周期制御を乱す――多発性嚢胞性腎疾患のマウスモデルにおける検討
変わった名前の腎遺伝子が重要な理由
多発性嚢胞性腎疾患(PKD)は遺伝性の一般的な疾患で、無数の液体を満たした嚢胞がゆっくりと腎臓を覆い、しばしば腎不全に至ります。PKD1およびPKD2という二つの遺伝子の異常が病気を駆動することは知られていますが、進行速度に影響する他の多くの遺伝的因子が存在する可能性があります。本研究はSnhg5と呼ばれる長鎖ノンコーディングRNAというやや特殊な種類の遺伝子に焦点を当て、問いは単純かつ重要です:この分子はPKDの進行に実質的な影響を与えるのか、それとも単なる傍観者にすぎないのか?
あまり知られたくない遺伝子メッセンジャーの詳細
通常の遺伝子がタンパク質の設計図を提供するのに対し、長鎖ノンコーディングRNAは細胞内で分子の整理役やスイッチのように振る舞います。以前の研究は、Snhg5がマウスのPKDモデルで強く増加し、いくつかのがんや腎障害と関連していることを示しており、有害な増殖を促す可能性を示唆していました。研究者たちはまず、正常マウスでSnhg5がどこでいつ活性化されるかを詳しく調べました。その結果、Snhg5は多くの臓器で発現しており、特に腸で高レベルであること、腎臓では出生後に活性が急速に低下することが分かりました。これは、臓器が急速な成長期からより安定した成熟状態へと移行するためです。腎細胞内では、ほとんどのSnhg5分子がDNAを収める司令部である核に存在しており、Snhg5が直接タンパク質を作るよりも遺伝子発現の制御に関与していることを示唆します。
病的腎臓でのパターンは全てを語らない
研究チームは次に、さまざまなPKDマウスモデルでのSnhg5レベルを比較しました。嚢胞が速やかに形成される進行の速いモデルでは、病変のある腎臓でSnhg5が2〜3倍に増加し、単一細胞レベルのイメージングでは嚢胞上皮細胞やその周辺組織の核内に強いシグナルが示されました。驚くべきことに、ヒトのPKDの長期間にわたる経過をよりよく模倣する、進行が遅く軽度のマウスモデルではSnhg5は増加しませんでした。さらに注目すべきは、進行した常染色体優性PKDの患者腎組織では、この遺伝子のヒト相同体であるSNHG5が90%以上減少していたことです。これらを総合すると、このRNAの変動は嚢胞形成に伴うものではあるが、その増減の方向性やタイミングは種や病期によって異なり、Snhg5単独が嚢胞成長の単純な駆動因子であるとは言い難いことが示唆されます。
遺伝子を除去すると何が起きるか
相関関係を超えて原因を探るため、研究者たちはCRISPR遺伝子編集を用いてマウスからSnhg5遺伝子を完全に欠失させ、全身ノックアウト系統を作成しました。強く変動していた分子を除去することが有害ではないかという懸念に反して、Snhg5欠損マウスは出生比率に異常なく生まれ、寿命も正常で、腎臓の外観と機能は健康な同胎児と同等でした。顕微鏡検査でも瘢痕化や炎症のない正常な腎構造が示され、血液検査でも濾過障害の徴候は見られませんでした。しかし分子レベルではより微妙な変化が現れました:Snhg5を欠くマウスの腎臓組織および培養した腎尿細管細胞では、細胞分裂やDNA複製に結びつく遺伝子の活性に一貫した変動がありました。細胞培養では、より多くの細胞が細胞周期の後期や損傷を受けたsub-G1状態で停止していました。特にARPC5という、細胞内部の骨格を再編して細胞分裂を助ける複合体の一部であるタンパク質がSnhg5欠損で減少しており、因果連鎖の手がかりを示唆します。
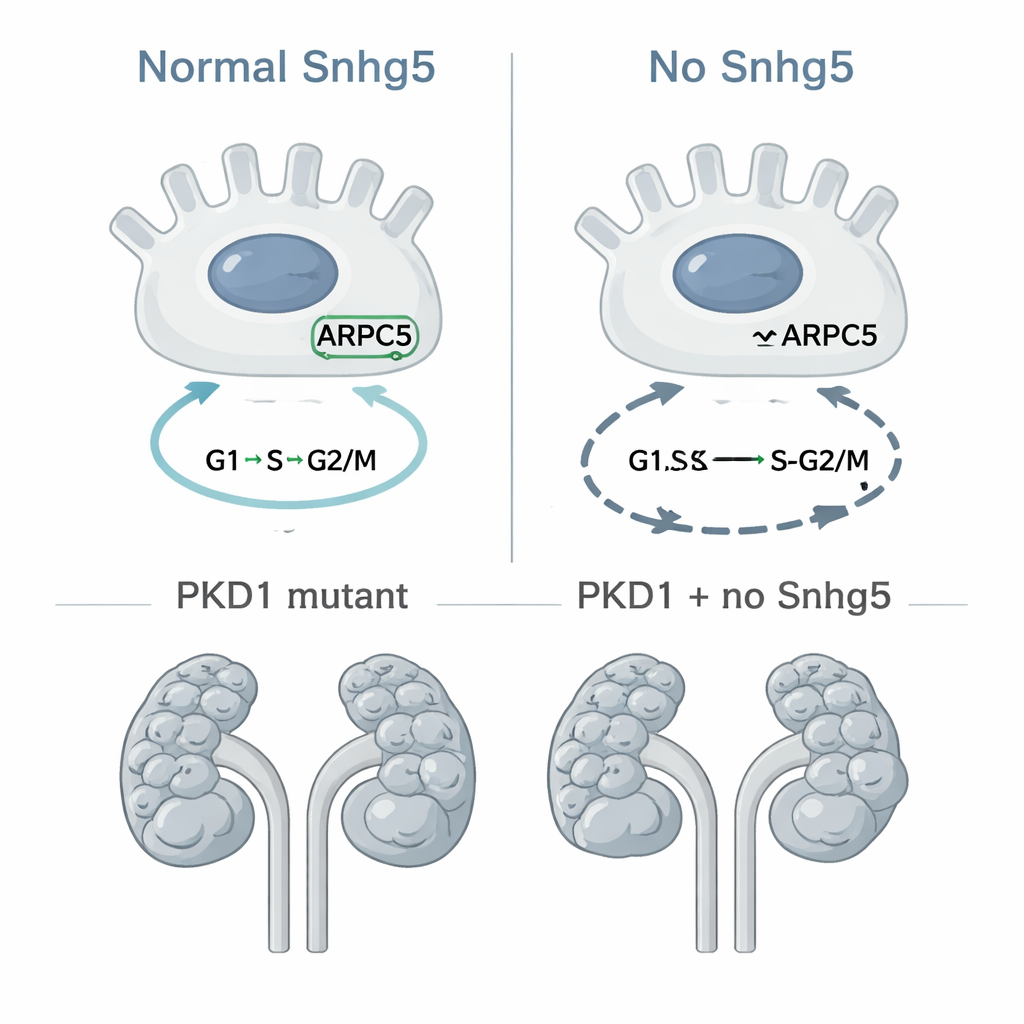
嚢胞成長における直接的な役割の検証
制御されない細胞分裂はPKDの中心的特徴のひとつであるため、研究者たちは次にSnhg5を除去すると、集合管細胞で特異的にPKD1が失われる確立されたマウスモデルにおける嚢胞形成が遅くなるかを調べました。彼らは、ある個体群がPKD1変異のみを持ち、他の個体群はPKD1とSnhg5の両方を欠くように交配しました。生後10日で動物を調べると、両群とも重度の嚢胞性腎を呈し、腎臓サイズ、嚢胞面積、嚢胞数の綿密な計測ではSnhg5除去による有意な保護効果は見られませんでした。むしろ二重変異マウスは僅かに嚢胞負荷が多い傾向がありましたが、その差は小さく統計的に説得力のあるものではありませんでした。言い換えれば、Snhg5は腎細胞の細胞周期関連遺伝子に影響を与えるものの、この特定のPKDモデルにおける嚢胞の出現や拡大の速度を明確に変えるほどの効果は示しませんでした。
今後の治療への示唆
患者と創薬者にとっての主要な結論は、Snhg5はマウスPKDで最も大きく変動する分子シグナルの一つであるにもかかわらず、少なくとも集合管由来の疾患の早期かつ急速に成長する段階においては、嚢胞形成の主要因ではないということです。この遺伝子はARPC5のような因子を介して腎細胞の細胞分裂の進行を微調整しているようですが、その影響は比較的微細であり、完全に失われても腎の発生やPKDの早期進行はほとんど変わりません。これらの発見は広い教訓を強調します:病変組織で目立つ分子変化のすべてが有望な治療標的であるとは限らないということです。原因と結果を切り分けるには、Snhg5のような長鎖ノンコーディングRNAを複数の疾患モデルや異なる時点で検証する必要があり、そのうえで初めて薬剤候補として自信を持って追求できるようになります。
引用: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
キーワード: 多発性嚢胞性腎疾患, 長鎖ノンコーディングRNA, Snhg5, 細胞周期, 腎嚢胞