Clear Sky Science · ja
REAC RGN-AR治療は脂肪組織由来幹細胞の脂肪分化を変調させる
脂肪細胞の再形成が重要な理由
多くの人は体脂肪を単なる余分な重さと考えますが、脂肪組織は活発に全身と情報をやり取りする臓器であり、健康を守ることも害することもあります。肥満や2型糖尿病のような関連疾患では、脂肪細胞が肥大化し炎症を起こし、代謝的に有害になることがよくあります。本研究は、ラジオ波を穏やかに用いて脂肪由来の幹細胞を不健康な“貯蔵”脂肪細胞へと向かわせるのを避け、より活動的でカロリーを消費するタイプの細胞へ誘導する新しい非侵襲的技術を探ります。このスイッチを理解し利用できれば、代謝性疾患の治療や組織修復の新たな道を開く可能性があります。
細胞と“会話”する新しい方法
体内の脂肪組織には自己更新し脂肪、骨、軟骨など複数の細胞型に分化できる幹細胞が存在します。これらの脂肪組織由来幹細胞(ADSC)は日常的な手術から容易に採取でき、すでに再生療法で検討されています。課題は、とくに代謝に問題のある人では、これらの細胞が大量の脂肪を蓄える通常の白色脂肪細胞になりやすく、低度の炎症を助長する点です。研究者らはRadio Electric Asymmetric Conveyer(REAC)という技術を、彼らがTO RGN-ARと呼ぶ特定プロトコールで適用し、細胞自身の電気的活動を微妙に調整することを試みました。目的は、この生体電気的“調律”が幹細胞の若々しい可塑性を保ちながら、不健康な脂肪細胞への分化を抑えられるかを確認することでした。
細胞の若さと可塑性を保つ
試験管内の実験では、ADSCは肥満や糖尿病のない成人からの少量の脂肪試料から分離されました。これらの細胞は通常脂肪細胞へ分化させる条件下で培養されました。いくつかの培養皿は培地中に置かれた小さなプローブを介して72時間のREAC処理を受け、他は未処理の対照として扱われました。後に遺伝子発現を調べると、REAC暴露はOct-4、Sox2、Nanogといった幹性を保つ重要な遺伝子の発現を増加させ、細胞が多能性と自己更新能力を維持するのに寄与していることが示されました。注目すべきは、この保護効果が強力な脂肪誘導カクテルにさらされた場合でも持続し、ラジオ電気治療が細胞を通常の脂肪への一方通行的な決定から抵抗させるのを助けたことです。
貯蔵脂肪からの回避を誘導する
研究チームはまた、脂肪の貯蔵や脂質処理に関与するPPAR-γ、LPL、ACOT2などの白色脂肪形成を駆動する遺伝子も測定しました。分化培地のみで処理された細胞では、これらの遺伝子は強くオンになり、大量の中性脂肪を蓄える大きな脂肪細胞へのシフトを示していました。対照的に、REAC処理を受けた細胞ではこれらの脂肪形成マーカーが著しく低下し、細胞の生存や増殖に変化は見られませんでした。同時に、熱産生や代謝的に活発な脂肪に関連する遺伝子UCP1の発現が増加しました。このパターンは、REACが単に細胞増殖を阻害するのではなく、発生プログラムを貯蔵脂肪の形成からエネルギー消費型の性質へと再配向させていることを示唆します。
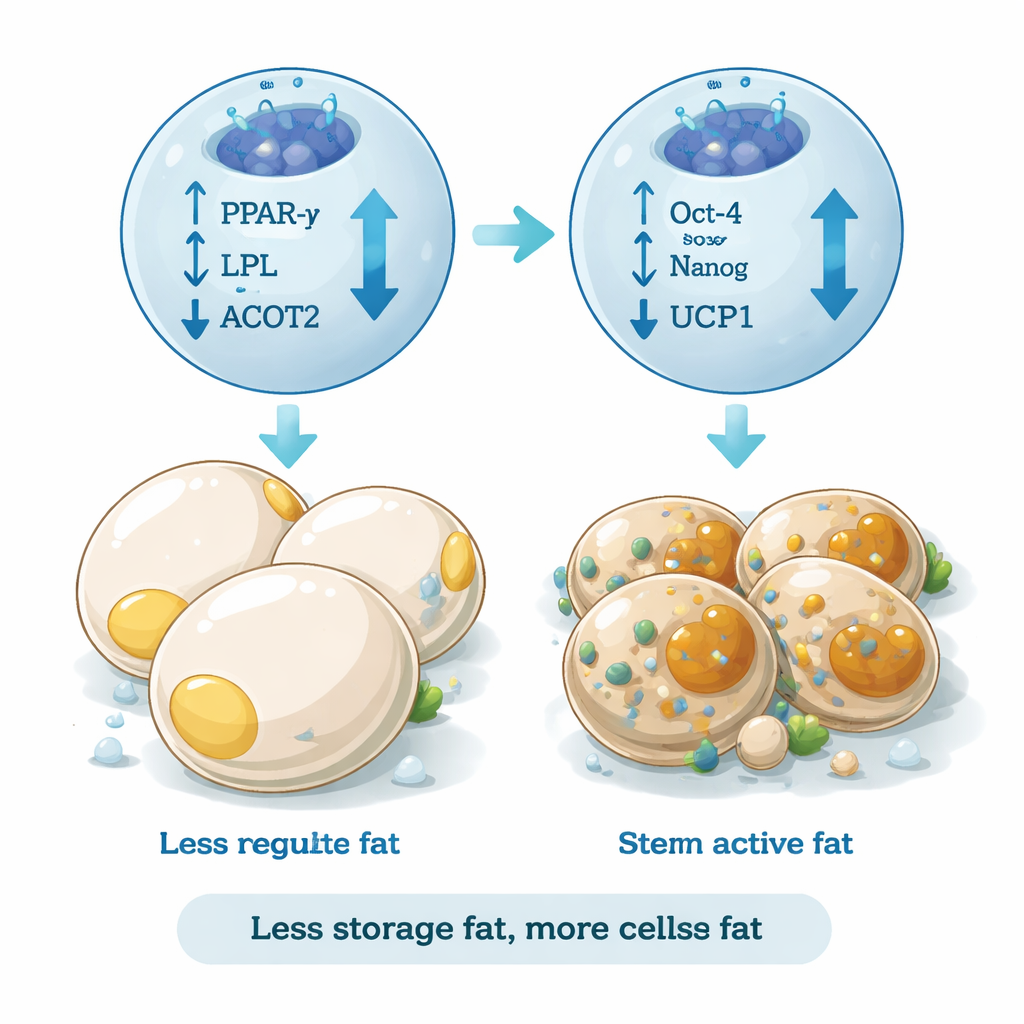
“良い”脂肪特性を促進する
遺伝子発現に加え、研究者らは細胞の外見や表面マーカーも調べました。蛍光標識を用いて異なる脂肪細胞タイプを識別するタンパク質を追跡しました。自己分化させた細胞は古典的な白色脂肪のマーカーであるASC-1を高発現していました。REAC処理ではASC-1が低下し、TMEM26やPAT2などベージュ脂肪や褐色脂肪に関連するマーカーがより顕著になりました。ベージュ脂肪細胞は熱を生産してカロリーを燃焼し、抗炎症性のシグナルを放出する傾向があるため特に注目されます。顕微鏡下では、REAC処理を受けた培養では成熟した脂質で満たされた脂肪細胞が少なく、幹細胞様の形態を保った細胞が多く見られ、より健康で柔軟な脂肪プロファイルへのシフトをさらに示していました。
将来の治療に対する意義
総じて、これらの所見はREAC TO RGN-ARが脂肪由来幹細胞を穏やかに“指導”し、若々しさを保ち、有害な貯蔵脂肪細胞への分化を避け、代わりにベージュで代謝的に活発な脂肪の特徴を採用させる可能性を示唆します。これらの実験は培養皿内で行われたものであり患者での検証はまだですが、微調整された電気的シグナルを用いて脂肪組織のバランスを回復し、慢性炎症を軽減し、代謝健康を改善する有望な戦略を示しています。今後、動物や人での研究がこれらの効果を確認すれば、こうした非侵襲的治療は食事、運動、薬物療法を補完して肥満関連疾患に対処したり、再生医療における幹細胞治療の性能を向上させたりする可能性があります。
引用: Cruciani, S., Rinaldi, S., Fontani, V. et al. REAC RGN-AR treatment modulates adipogenic differentiation in adipose tissue-derived stem cells. Sci Rep 16, 4860 (2026). https://doi.org/10.1038/s41598-026-35204-2
キーワード: 脂肪由来幹細胞, 生体電気的変調, ベージュ脂肪, 代謝性疾患, 再生医療