Clear Sky Science · ja
食品由来および腸内微生物がメチルグリオキサールを生成し、この代謝物が生理活性を持つ1-アセチル-β-カルボリンアルカロイドの生成をもたらす
腸内の化学工房が重要な理由
私たちの腸内や多くの発酵食品の中では、何兆もの細菌が摂取した糖を絶えず変換し、多様な化学的副産物を生み出しています。本研究はそのような経路の一つを詳しく調べています:一部の一般的な細菌が糖を高度に反応性の高い化合物メチルグリオキサール(MGO)に変え、さらに1-アセチル-β-カルボリンと呼ばれる生理活性分子群へと転換する仕組みです。これらの物質は疾病プロセスと新しい医薬品候補の双方に関連しているため、細菌がいつどのようにそれらを作るかを理解することは、食品、マイクロバイオーム、そして健康に対する考え方を変え得ます。
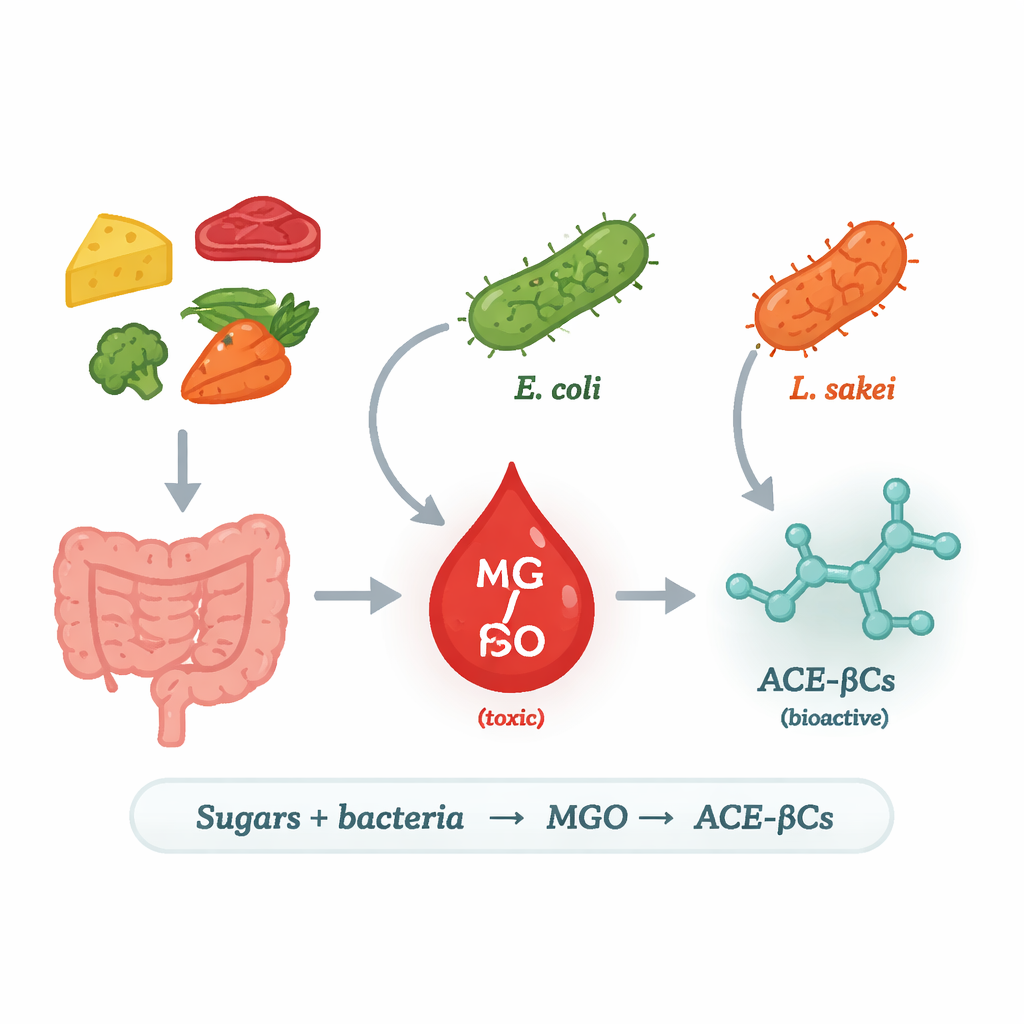
日常の糖から危険な分子へ
研究者たちはメチルグリオキサール(MGO)に着目しました。MGOは糖の分解で生じる非常に反応性が高く有害な副産物です。ヒトでは過剰なMGOがタンパク質やDNAを損傷しうるため、糖尿病、心血管疾患、神経変性と関連しています。私たちの細胞は通常、解毒システムでMGOを制御していますが、発生源はそれだけではありません:細菌もMGOを産生します。一部の微生物では、メチルグリオキサール合成酵素(MgsA)と呼ばれる酵素が糖代謝中間体を直接MGOに変換し、エネルギー代謝の“近道”を作ります。研究チームはどの食品や腸内細菌がこの経路を使うのか、どんな条件で使うのか、そして放出されたMGOに何が起こるのかを問いかけました。
どの細菌が産生するのか?
この問いに答えるため、科学者たちは食品にしばしば見られる複数の乳酸菌株と、実験室用株のEscherichia coliを、グルコースまたはガラクトースを含む制御培地で培養しました。そして、高精度のクロマトグラフィーと質量分析で培養液中のMGOと二つの関連アルカロイドを時間経過で追跡しました。顕著な量のMGOとアルカロイドを生成したのはE. coliと肉製品に関連する種Lactilactobacillus sakeiのみで、他に試した乳酸菌は産生しませんでした。ゲノム検索は重要な違いを示しました:E. coliとL. sakeiはMgsAの遺伝子を持ち、多くの乳酸菌近縁種は持っていません。研究者がL. sakei由来のmgsA遺伝子を産生しない株に導入すると、その改変菌はMGOとアルカロイドの両方を作り始め、MgsAがこの経路に確実に関与していることが示されました。
毒性のあるMGOが生理活性アルカロイドになる仕組み
次の質問は、MGOが生成された後に何が起こるかでした。チームは1-アセチル-β-カルボリン(ACE-βC)アルカロイドに注目しました。これらは抗菌性、抗炎症性、抗がん活性が報告されている小分子です。MGOを産生する細菌がアミノ酸L-トリプトファンの存在下で培養されると、1-アセチル-β-カルボリンとその3-カルボキシル酸型の二つのACE-βCのレベルが急増することを示しました。培地に追加のMGOを加えることでも形成は促進されました。これは、MGOが細胞外へ漏れ出し、追加の酵素を必要とせず周囲の液中でL-トリプトファンと自発的に反応してこれらの生理活性化合物を生成することを示しています。言い換えれば、MGOを危険にする同じ化学反応が、それをより複雑で潜在的に有用な効果を持つ分子に変えているのです。
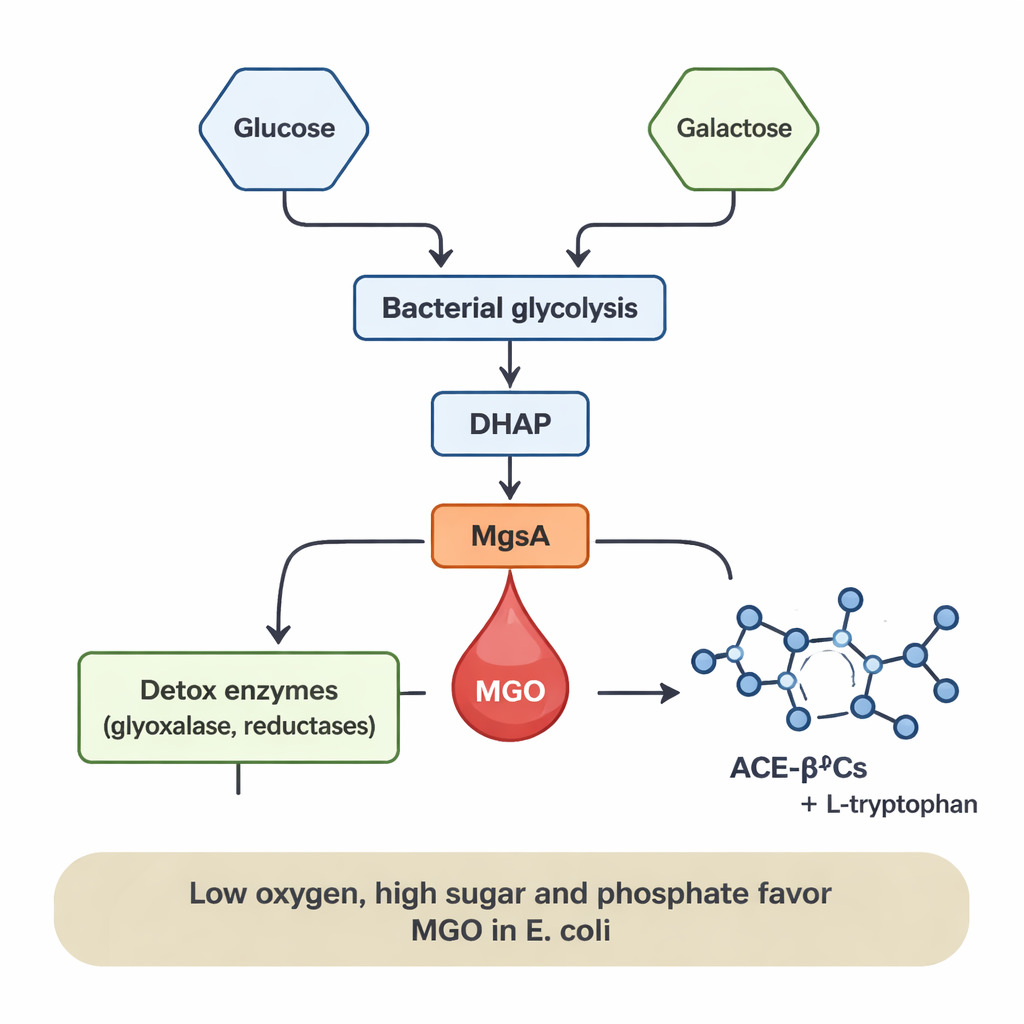
産生量を上下させる要因
MGOの産生は固定的ではなく、細菌の栄養と環境に強く依存していました。E. coliでは、MGOはグルコースが存在する場合にのみ出現し、グルコース濃度が上がるにつれてその量は増加しました。一般的な無機栄養素であるリン酸を加えると、リン酸化糖中間体の蓄積を促してMgsA近道に供給されやすくなるため、MGO生成は数倍に増強されました。ヒトの腸に似た低酸素(嫌気)条件もMGO放出を促し、高酸素、十分に曝気された条件では細菌がよく増殖していてもMGOは大幅に減少しました。対照的に、L. sakeiは主にガラクトースで育てたときにMGOを生成し、ガラクトース濃度が高いほど産生が増えました。これらのパターンは、細菌代謝を通る糖の流れが高く酸素が限られるとき、MGOが蓄積する糖中間体の負荷を軽減する“減圧弁”として働く可能性を示唆しています。
食品と健康にとっての意義
この研究結果は、腸や食品中のすべての細菌がMGOやACE-βCを作る能力が同じではないことを示唆しています。MgsA酵素を持つ種、例えば特定のL. sakei株やE. coliは、特に腸内や一部の発酵環境のような糖に富み酸素が乏しい状況で重要な寄与者になり得ます。彼らが排出するMGOは宿主組織への化学的負荷に加わる可能性がありますが、ACE-βCへの変換はこの反応性化合物を一部“掃除”すると同時に、それ自体の生物学的効果を持つ分子を生み出すことでもあります。本研究は培養条件下で行われたものですが、食事、微生物組成、細菌代謝が共同して体内の有害と潜在的に有益な化学物質のバランスを形作るもっともらしい経路を浮かび上がらせ、ACE-βCが食品や腸内での細菌性MGO生成の指標となり得ることを示しています。
引用: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
キーワード: 腸内細菌叢, メチルグリオキサール, 細菌代謝, 食品発酵, β-カルボリンアルカロイド