Clear Sky Science · ja
性能と一般化の課題に着目した結腸組織病理学向けのコンパクト深層学習モデル
患者と医師にとってこの研究が重要な理由
結腸がんは世界で最も致命的ながんの一つですが、その診断は依然として専門家が顕微鏡画像を注意深く観察することに依存しており、この作業は時間がかかり意見の不一致が生じやすいです。本研究は、非常に小型で効率的な人工知能(AI)モデルが、計算資源の限られた施設を含む日常の臨床現場で役立つほど正確に結腸のがん組織を検出できるかを検証します。また、開発段階ではほとんど完璧に見えるモデルでも、実世界の新しいデータでは大きく失敗するという潜在的な弱点を明らかにします。
顕微鏡画像をコンピュータに学習させる
結腸生検が行われると、病理医は薄く切った染色組織切片を顕微鏡で観察します。がん組織は歪んだ腺構造、不規則な細胞形状、周囲組織への浸潤を示す一方で、正常組織は整然とした規則的なパターンを示します。著者らは、がん(結腸腺がん)と良性組織がほぼ同数ずつ含まれる約24,000枚の公開デジタル画像コレクションを使用しました。すべての画像を標準の小さなフォーマットにリサイズし、スライドの切り方、染色、スキャン方法の自然なばらつきを模倣するために、小さな回転、反転、ズーム、穏やかな色調変化といった現実的な補正を適用しました。この慎重な前処理により、AIモデルは向きや明るさなどの表面的な差異ではなく、意味のある組織パターンに着目できるようになります。
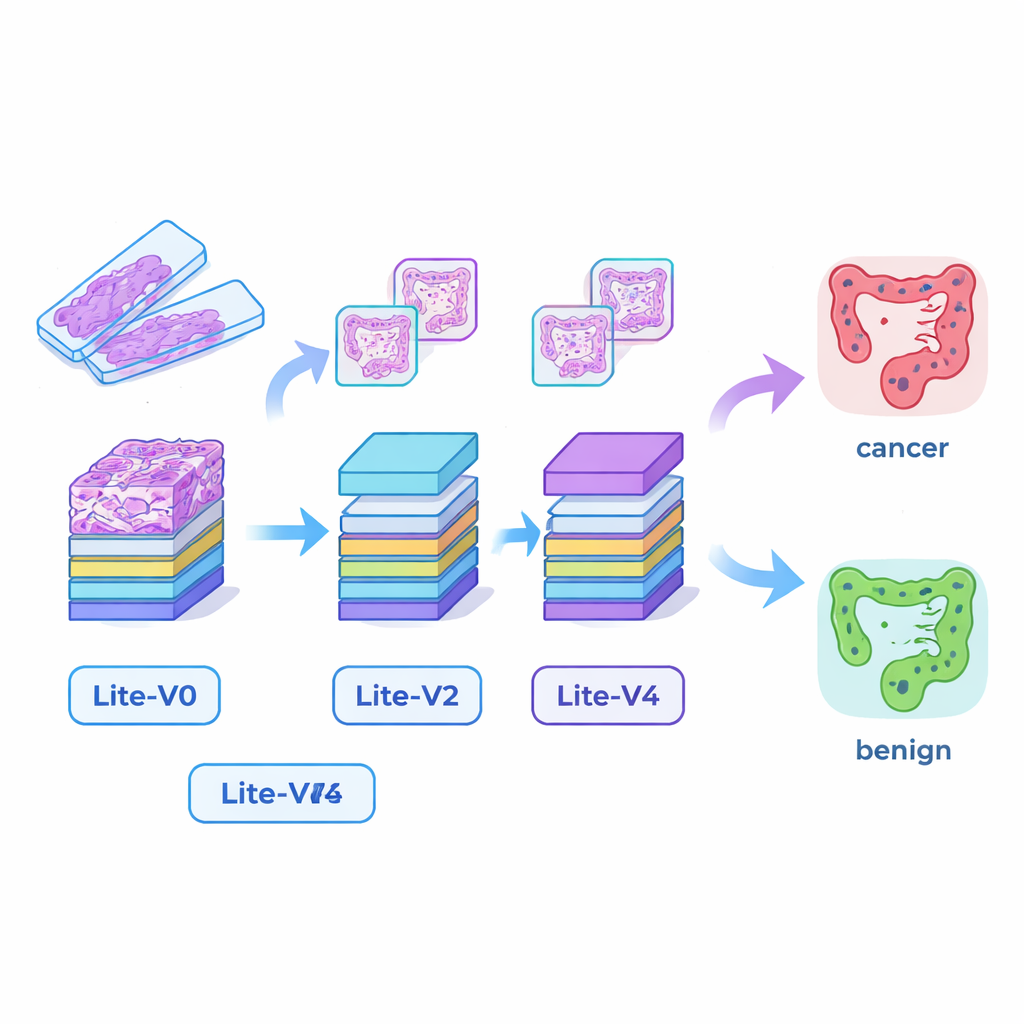
小型だが有能なAI「目」の構築
多くの成功した医療用AIシステムは、強力なGPUと大量のメモリを必要とする非常に大きな深層学習モデルに依存しており、小規模な病院や臨床現場での導入が難しいことがあります。このギャップを埋めるために、研究者たちは4つのコンパクトな畳み込みニューラルネットワーク(Lite‑V0、Lite‑V1、Lite‑V2、Lite‑V4)を設計しました。各モデルは同じ入力画像パッチを扱いますが、エッジ、テクスチャ、腺の形状などの視覚的特徴を検出する層の数やフィルタ数が異なります。いずれも、標準的な畳み込み、正規化、プーリングを繰り返す単純で透明性の高い設計を共有し、最後に小さな「決定ヘッド」でがんか良性かの確率を出力します。目的は、基本的な臨床ハードウェアに容易に収まるほど小さいモデルからどれだけの精度を引き出せるかを検証することでした。
ラボ内での印象的な成績
チームはデータセットを固定分割して4モデルを訓練・比較し、精度、両クラスの誤りを均等に評価するマクロF1スコア、混同行列、ROC曲線や適合率-再現率曲線といった診断プロットなど、広く受け入れられた指標を用いました。中規模のモデルであるLite‑V2が最も優れた成績を示しました。サイズは約1.5メガバイトで学習可能パラメータは約128,000にすぎないにもかかわらず、内部検証セットではほぼ完璧な性能を示し、マクロF1スコアは約0.999、感度と特異度もほぼ完璧でした。つまり、この注意深く準備された環境内では、Lite‑V2は結腸のがん組織と良性組織をほとんど常に区別でき、かつ控えめな計算環境でも高速に動作することが示されました。
実世界のばらつきが魔法を壊すとき
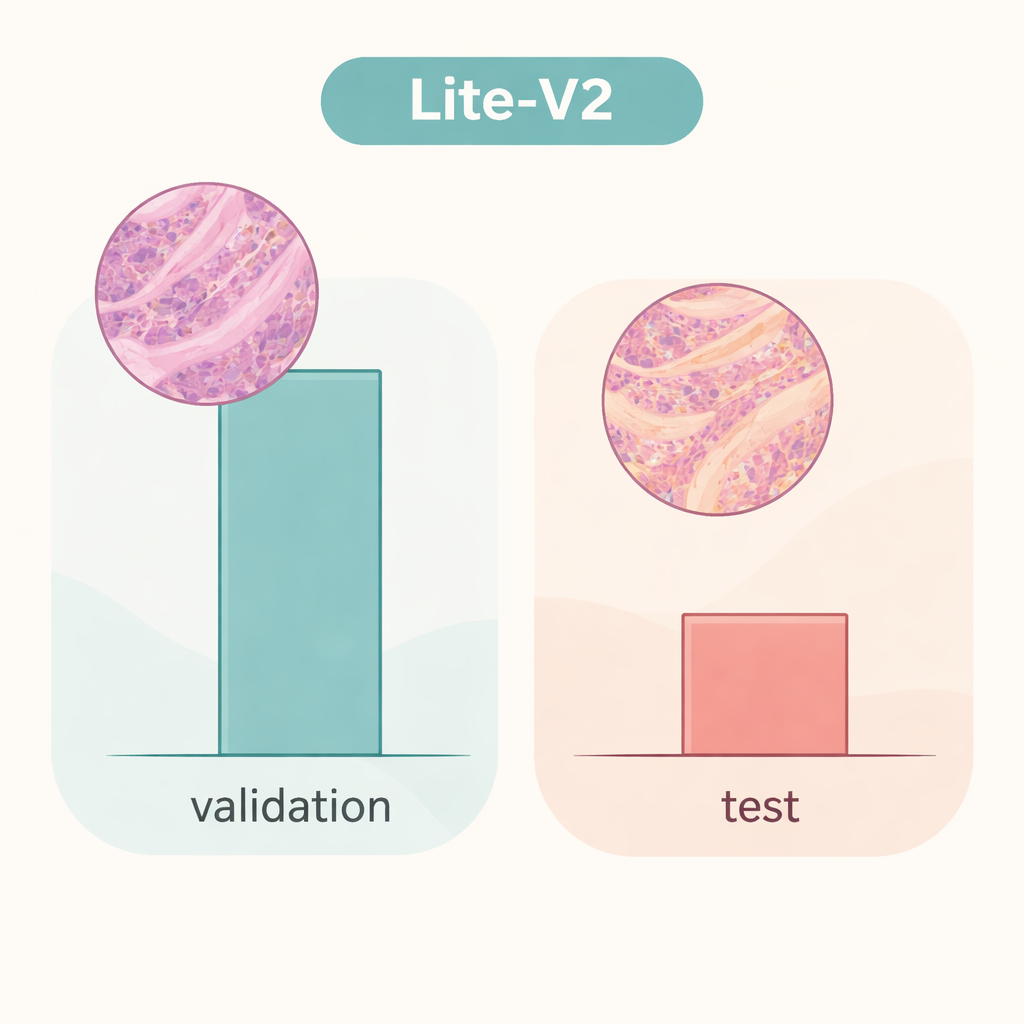
しかし、同じLite‑V2モデルを別の研究室から来たスライドを模した微妙に異なる独立画像セットで評価すると、状況は劇的に変わります(研究者が言うところの「ドメインシフト」)。この未見のテストセットでは全体の精度が約50%に落ち、マクロF1スコアは約0.33に低下しました。モデルは多くのがんサンプルを認識し続けましたが、良性組織に対して大きく誤分類し、多数を悪性と判断してしまいました。これはネットワークが、染色スタイルやスキャナ特性など元のデータソースに強く結びついた詳細を学習しており、病変の堅牢で移植可能な特徴ではなくそれらに依存していたことを示しています。この結果は、内部検証で優れた結果が得られても、真に異なるデータで挑戦されなければ誤った安心感を与える可能性があることを強調します。
将来のAI診断ツールにとっての意味
一般読者への結論は二つあります。第一に、コンパクトなAIシステムは結腸組織画像で専門家レベルの性能に達し得る一方で、小型で効率的なため広く展開でき、過負荷のかかった病理医を支援してより迅速なスクリーニングを可能にします。第二に同じく重要なのは、ホームデータセットで「完璧」に見えるモデルでも新しい病院からの画像と出会うと大きく失敗する可能性があることです。著者らは、軽量モデルを染色やスキャナ、患者集団の変化に対して堅牢にすることに今後の研究の重点を置くべきだと論じており、染色ロバストな訓練、ドメイン適応、より広範な多施設データセットといった戦略が必要だと述べています。それまでは、AIはがん診断における独立した決定者というよりも、有望な補助者として位置づけるべきです。
引用: Hanif, F., Raza, A. & Mohammed, H.A. Compact deep learning models for colon histopathology focusing performance and generalization challenges. Sci Rep 16, 5489 (2026). https://doi.org/10.1038/s41598-026-35119-y
キーワード: 結腸がん, 組織病理学, 深層学習, 軽量CNN, ドメインシフト