Clear Sky Science · ja
二重特異性ホスファターゼ6はFOXO1のCYP4A11に対する抑制活性を阻害し、肝臓での脂質蓄積を仲介する
なぜ肝臓の脂肪が重要なのか
肝臓に過剰な脂肪がたまる「脂肪肝」は、砂糖や脂肪の多い現代の食生活とともに増え続けています。コレステロールや血糖はよく知られていますが、肝細胞内の小さな分子スイッチが脂肪を燃焼するか貯蔵するかを決めていることを知る人は少ないでしょう。本研究はDUSP6、FOXO1、CYP4A11という3つのタンパク質に着目し、これらの綱引きがどのように肝細胞を過剰な脂肪の貯蔵へと傾けるかを明らかにします。この隠れた制御系を理解することは、脂肪肝や関連する代謝異常の新たな治療法の手がかりになる可能性があります。
肝細胞内の隠れた交通整理役
研究者たちは主にERK経路という細胞シグナル伝達をオフにすることで知られるタンパク質DUSP6に注目しました。過去の研究ではDUSP6を欠くマウスは食事誘発性の脂肪肝に意外にも抵抗性であり、脂質代謝に関与するCYP4A酵素のレベルが低下していることが示されていました。本研究では、ヒト由来の肝酵素の一つであるCYP4A11に対してDUSP6がヒト肝細胞でどのように働くかを問いました。研究には標準的な肝がん細胞株であるHepG2とHuH‑7をヒト肝細胞の代替として用い、パルミチン酸とオレイン酸の混合脂肪酸で細胞を処理して不健康な高脂肪環境を模倣しました。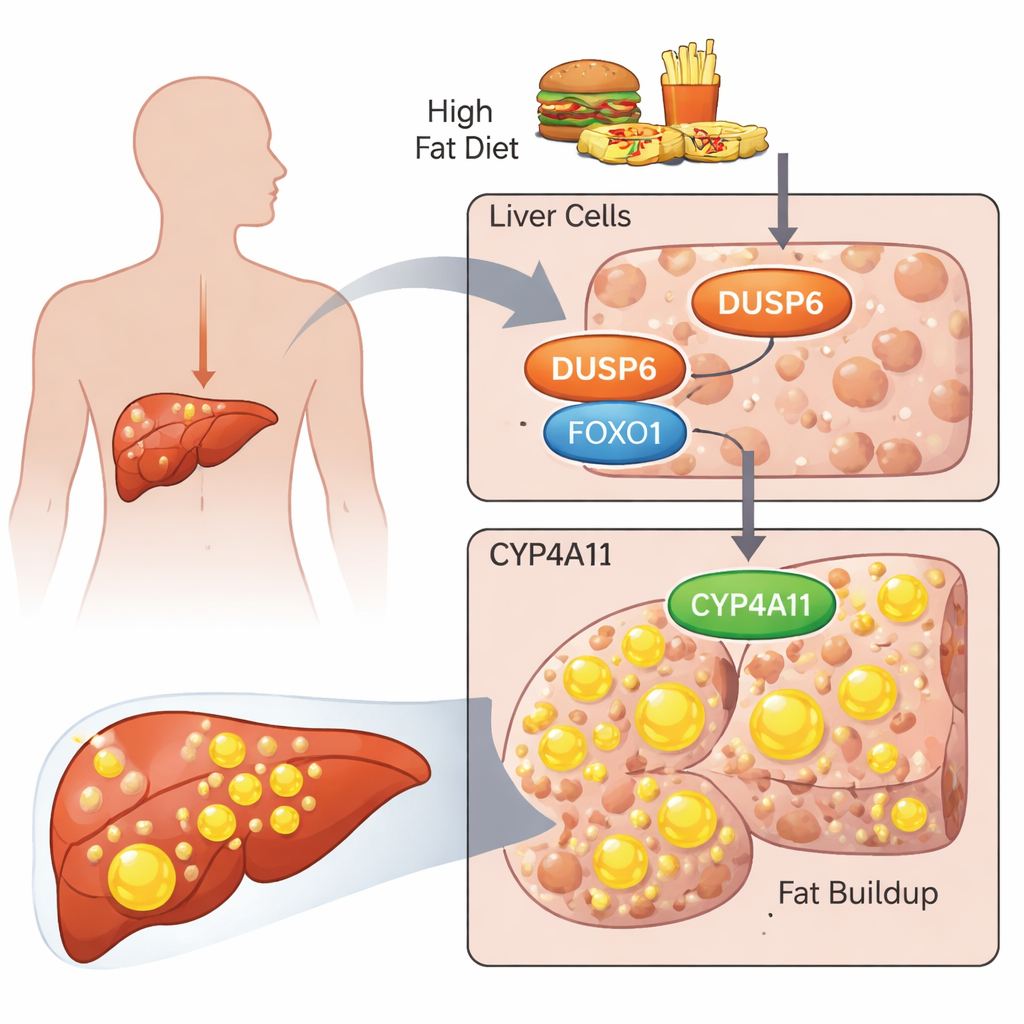
脂肪酸から脂肪で満たされた細胞へ
これらの脂肪酸で処理すると、細胞は明らかに脂滴を蓄積し、研究者はそれを染色して定量しました。同時にDUSP6とCYP4A11のレベルが上昇し、主要なシグナル伝達タンパク質であるAKTとFOXO1の活性化型も増加しました。標的RNAを用いてDUSP6をノックダウンするとこのパターンは逆転し、細胞の脂肪蓄積は減少し、CYP4A11のレベルは下がりましたが、活性化したERK、AKT、FOXO1はすべて増加しました。ERK経路を単独で阻害すると脂肪蓄積がむしろ悪化する一方、AKTを単独で阻害するとそれは減少しました。ERKとAKTの両方を同時に阻害すると脂肪蓄積が低下し、CYP4A11のレベルも減少しました。これらの実験はCYP4A11が脂肪蓄積の程度と強く結びついており、特にAKT活性が脂肪貯蔵を駆動する上で重要であることを示唆しています。
脂肪促進遺伝子にかかるブレーキ
もう一つの重要な因子であるFOXO1は転写因子であり、核に入り遺伝子のオン・オフを制御できます。FOXO1はCYP4A11と同じ酵素ファミリーのいくつかのメンバーに対するブレーキとして働くことが知られています。研究チームはFOXO1を減らすと細胞がより多くの脂肪を蓄え、CYP4A11が増加することを見出し、逆にCYP4A11を直接増やすと細胞はさらに脂っぽくなりました。対照的にFOXO1を過剰発現させるとCYP4A11と脂肪蓄積の両方が減少しました。CYP4A11の活性を阻害する薬剤(HET0016)はFOXO1低下による脂肪過剰を抑え、CYP4A11が単なる傍観者ではなく脂質蓄積の駆動因子であることを支持しました。化学分析ではHET0016がCYP4A11により生成される20‑HETEの量を低下させ、20‑HETEは酸化ストレスや炎症と関連するため、この経路が肝障害に結びつくことがさらに示されました。
DUSP6はどうやってブレーキを外すのか
FOXO1がCYP4A11をどのように制御しているかを理解するために、研究者たちはCYP4A11遺伝子の前方領域(プロモーター領域)を調べ、FOXO1が結合できる配列を見つけました。クロマチン免疫沈降(ChIP)アッセイを用いて、FOXO1、特にその非リン酸化型がCYP4A11プロモーターに直接結合することを示し、同遺伝子に対する抑制的な役割と一致しました。共免疫沈降実験ではDUSP6がFOXO1と物理的に相互作用するが、FOXO1のリン酸化型とは相互作用しないことが明らかになりました。分画化と顕微鏡観察により、DUSP6は細胞質に存在し、DUSP6があるとFOXO1が核に入るのを抑えていることが示されました。DUSP6をノックダウンするとより多くのFOXO1が核へ移行し、そこでDNAに結合してCYP4A11を抑制できるようになります。実質的に、DUSP6は錨(いかり)のようにFOXO1を細胞質に隔離し、FOXO1がCYP4A11に対するブレーキとして働くのを阻害しているのです。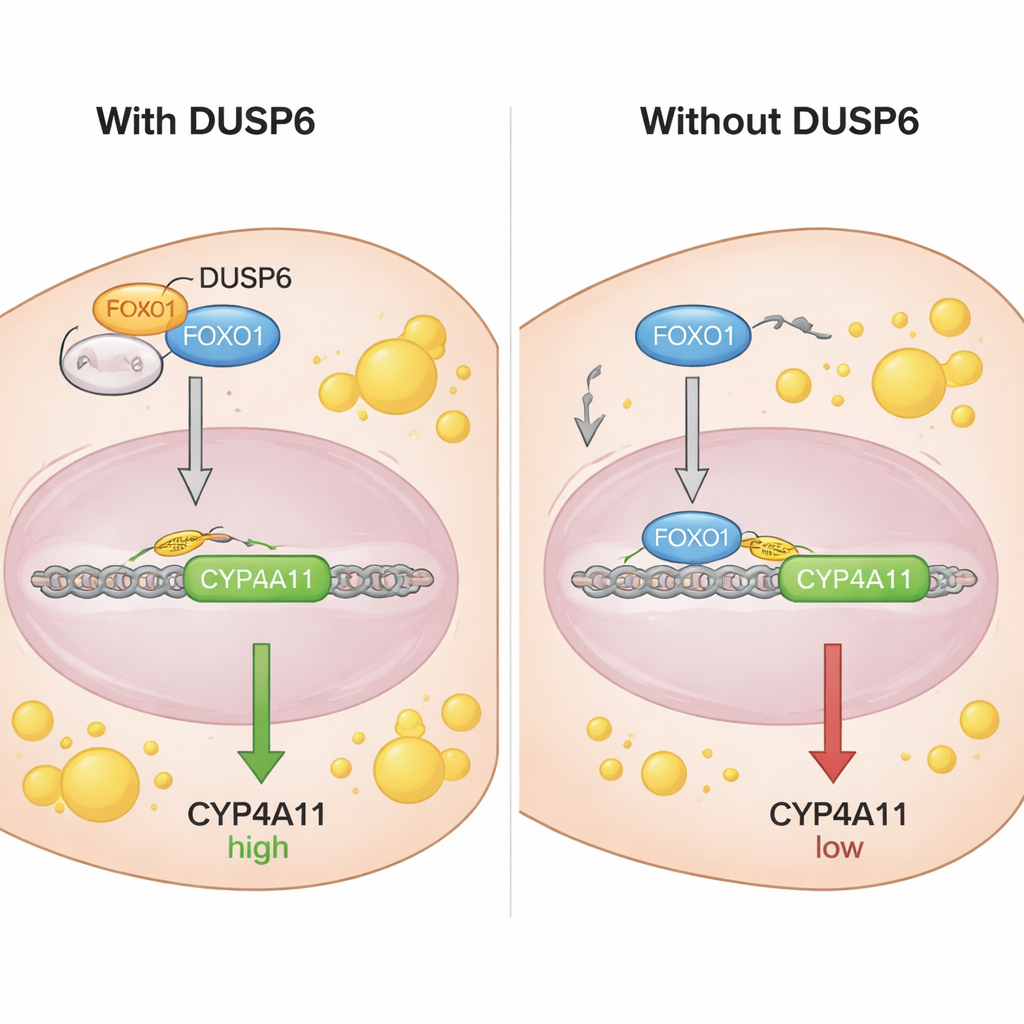
脂肪肝とその先にある意義
要約すると、本研究は肝細胞内の一連の出来事を描きます。DUSP6がFOXO1を細胞質に留めることで、FOXO1によるCYP4A11遺伝子の抑制力が弱まり、FOXO1が脇に追いやられるとCYP4A11の活性が高まり、細胞はより多くの脂肪を蓄え、20‑HETEのような酸化ストレスや炎症を促す分子を生成します。これらの発見は培養された肝由来細胞に基づくものであり、健常なヒト肝臓組織からのデータではない点には注意が必要ですが、DUSP6とCYP4A11が代謝機能障害に関連する脂肪肝疾患の新たな治療標的になり得ることを示しています。DUSP6活性を減らすかCYP4A11の作用を抑える治療は、理論的にはFOXO1の抑制機能を回復させ、肝臓の脂肪蓄積を抑える助けになるかもしれません。
引用: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
キーワード: 脂肪肝疾患, DUSP6, FOXO1, CYP4A11, 肝代謝