Clear Sky Science · ja
機械学習を用いたDrugBank解析が明らかにしたBCL-2阻害の新たな候補
より賢いがん薬を見つける意義
がん細胞は、通常なら死ぬべきときに死を回避することが多くあります。多くの腫瘍は、細胞の自己破壊プログラムを遮断する「護衛役」タンパク質群であるBCL-2を過剰に利用して生き延びます。BCL-2を標的とする薬剤はすでに存在しますが、副作用を引き起こしたり、すべての患者に効くわけではありません。本研究は、最新の機械学習を用いて既存の何千もの薬剤をふるいにかけ、BCL-2を無力化してがん細胞の自己破壊を促す可能性のある、新しくより安全な候補を見つけられるかを探ります。
細胞が生か死かを決める仕組み
健康な組織では、損傷したり不要になった細胞がアポトーシス(プログラム細胞死)と呼ばれる制御された自己破壊プロセスを通じて常に除去されています。BCL-2ファミリーと呼ばれるタンパク質群は、この決定の中心的スイッチとして働きます。メンバーの中には細胞の生存を促すものもいれば、死を促すものもあります。多くのがんでは、BCL-2や近縁のBCL-XLといった生存促進側のタンパク質が過剰に産生されています。この過剰な保護によってがん細胞は死のシグナルを無視し、化学療法に耐性を示します。こうした理由からBCL-2を阻害することは有望な治療戦略となっていますが、現行薬は関連するタンパク質にも作用してしまい、血小板数の危険な低下などの副作用を招くことがあります。
有望な分子を見分けるためにコンピュータを訓練する
研究者たちは新規化合物を一から探す代わりに、すでに研究されていたり医薬品として使われている分子のデータベースに目を向けました。出発点として用いたのはChEMBLという大規模な公開リソースで、ここにはさまざまな化学物質がBCL-2にどれほど強く結合するかという実験データが収められています。この情報を慎重に精製し(重複、測定の不確かさ、過度に大きいまたは異常な分子を除去)、最終的に601の良く記述された化合物を得ました。各分子はその構造的特徴をとらえた一種のデジタル指紋に変換されました。これらの指紋を用いて、新しい分子が強力なBCL-2阻害剤である可能性が高いか、あるいは実質的に不活性であるかを判定するタスクに対し、7つの異なる機械学習モデルを訓練・比較しました。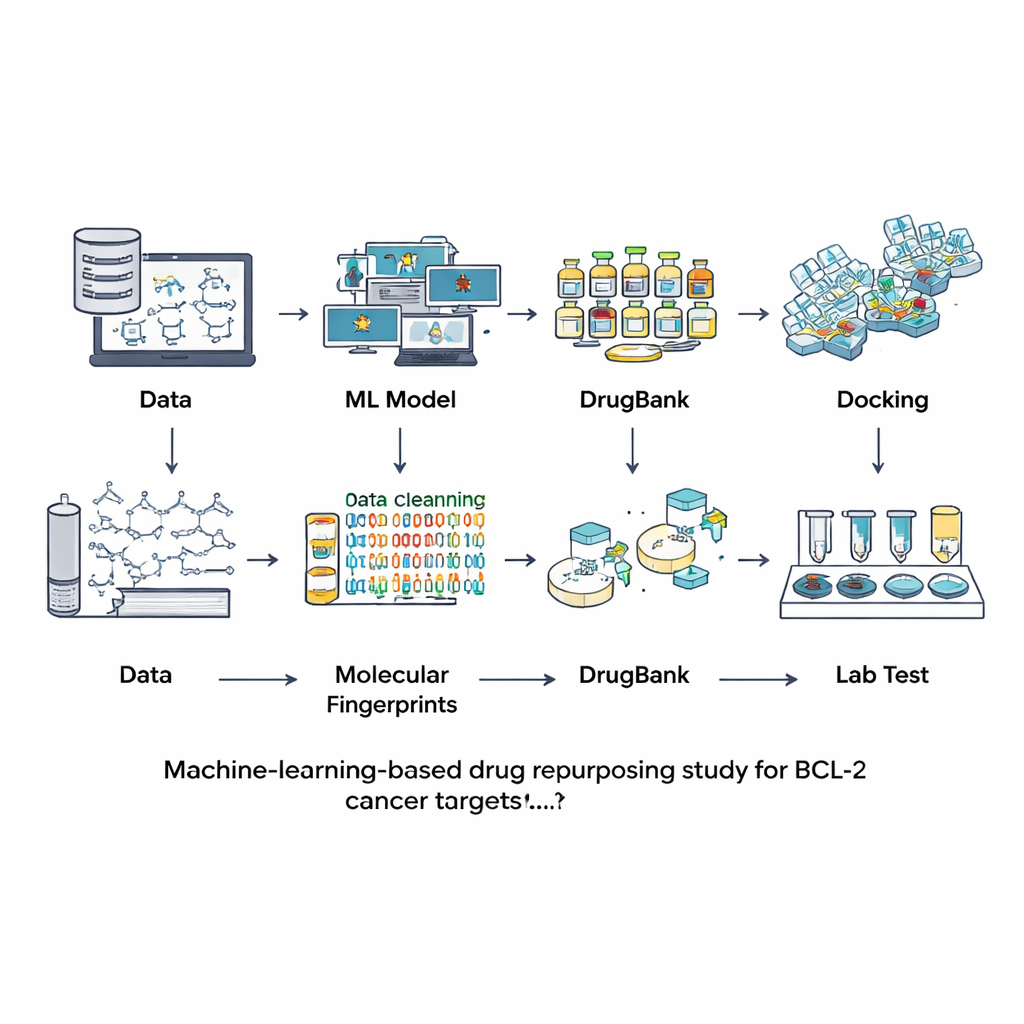
最良モデルの選定と薬剤ライブラリのスキャン
研究チームは、訓練時に用いられていない別のテストセットを使ってモデルを評価し、正答率だけでなく、活性化合物と不活性化合物をどれだけうまく区別できるかや予測のバランスの良さも確認しました。LightGBMと呼ばれる、木構造に基づくブースティング法の一種が、全体的な精度や信頼できる確率を割り当てる能力を含む多くの指標で最良の成績を示しました。この調整済みモデルを用いて、研究者たちはDrugBankへと向かいました。DrugBankは承認薬、実験薬、撤回された薬を含む1万2千以上の薬剤を集めた精選データベースです。同じタイプの指紋を計算した後、LightGBMに対してどの分子がBCL-2阻害剤に見えるかを尋ねました。高スコアを得た化合物はわずか9件で、ライブラリ全体の上位約0.1%に相当し、仮想スクリーニングが非常に選択的であったことを示しています。その9件のうち4件は既にBCL-2阻害剤として知られており、手法の妥当性が裏付けられました。
コンピュータのヒットから分子間相互作用へ
残りの高スコア分子のうち、研究者たちはこれまでBCL-2と関連づけられていなかった3種、Dersalazine、Opelconazole、Zongertinibに注目しました。これらの候補がBCL-2の結合ポケットに物理的に適合し得るかを調べるため、コンピュータドッキングを用いました。これは小分子がタンパク質表面にどのように収まるかを予測する手法です。シミュレーションの結果、特にOpelconazoleとZongertinibは、よく研究された参照薬ABT-737が捉えるのと同じ重要なアミノ酸と好ましい接触ネットワークを形成することが示唆されました。予測される結合強度は確立された阻害剤のそれに近く、機械学習モデルが実際にBCL-2を無力化し得る分子を発見していた可能性を示しています。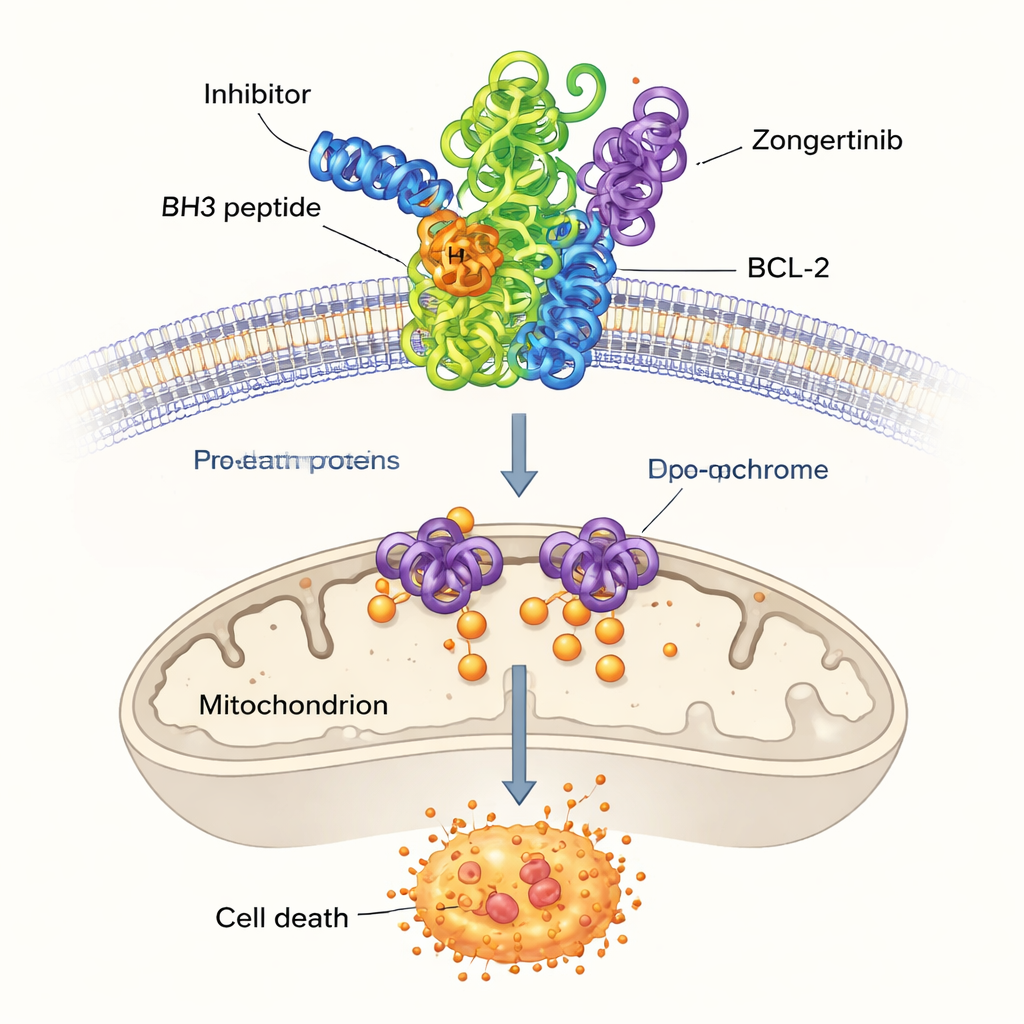
実験室で予測を検証する
計算上の示唆は、実際の条件で通用してこそ意味があります。そこでチームは3候補を、化合物がBCL-2とその天然の結合パートナーの結合をどれだけ阻害できるかを測る生化学的アッセイで試験しました。濃度の範囲で見ると、Dersalazineはほとんど効果を示しませんでした。一方でOpelconazoleとZongertinibは高用量でBCL-2活性を低下させ、特にOpelconazoleはほぼ信号を遮断しました。これらの濃度は臨床的に理想的な水準よりも高いものの、候補が実際にBCL-2と相互作用することを示し、発見のパイプライン全体を検証する結果となりました。
今後のがん治療への示唆
専門外の読者にとっての要点は、研究者たちがコンピュータにBCL-2を阻害する分子が「どのような見た目か」を学習させ、それを用いて既存の薬剤や薬様化合物の大規模ライブラリを精査したことです。このアプローチは既知のBCL-2薬を再発見し、新たな候補を浮かび上がらせ、そのうち2つは実験室試験で実際に阻害活性を示しました。効力の向上、安全性の理解、細胞や動物での試験など多くの課題が残っていますが、本研究は機械学習と丁寧なデータ精製が、既知の化合物を再利用・再評価することでより良いがん薬探索を加速できることを示しています。
引用: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
キーワード: BCL-2阻害薬, 機械学習, 薬剤リポジショニング, アポトーシス, がん治療