Clear Sky Science · ja
アルツハイマー病の薬再利用におけるDYRK2用ドッキングベース結合親和性を近似する物理情報を取り入れたグラフニューラルネットワーク
なぜアルツハイマー病にとって重要なのか
アルツハイマー病は世界的に増加している一方で、現在の多くの薬は症状を和らげるに留まり、病気を止めることはできません。実験室で新薬を評価するには時間と費用がかかり、記憶や神経の健康に関わる可能性があるが十分に研究されていない脳タンパク質の検査は特に難しい。本研究は賢い近道を検討します:物理的知見を取り入れた人工知能モデルを用いて、既存のアルツハイマー薬が未開拓のタンパク質DYRK2にどの程度結合するかを予測し、治療の新たな道を開く可能性を探るのです。
既存薬を新たな視点で見る
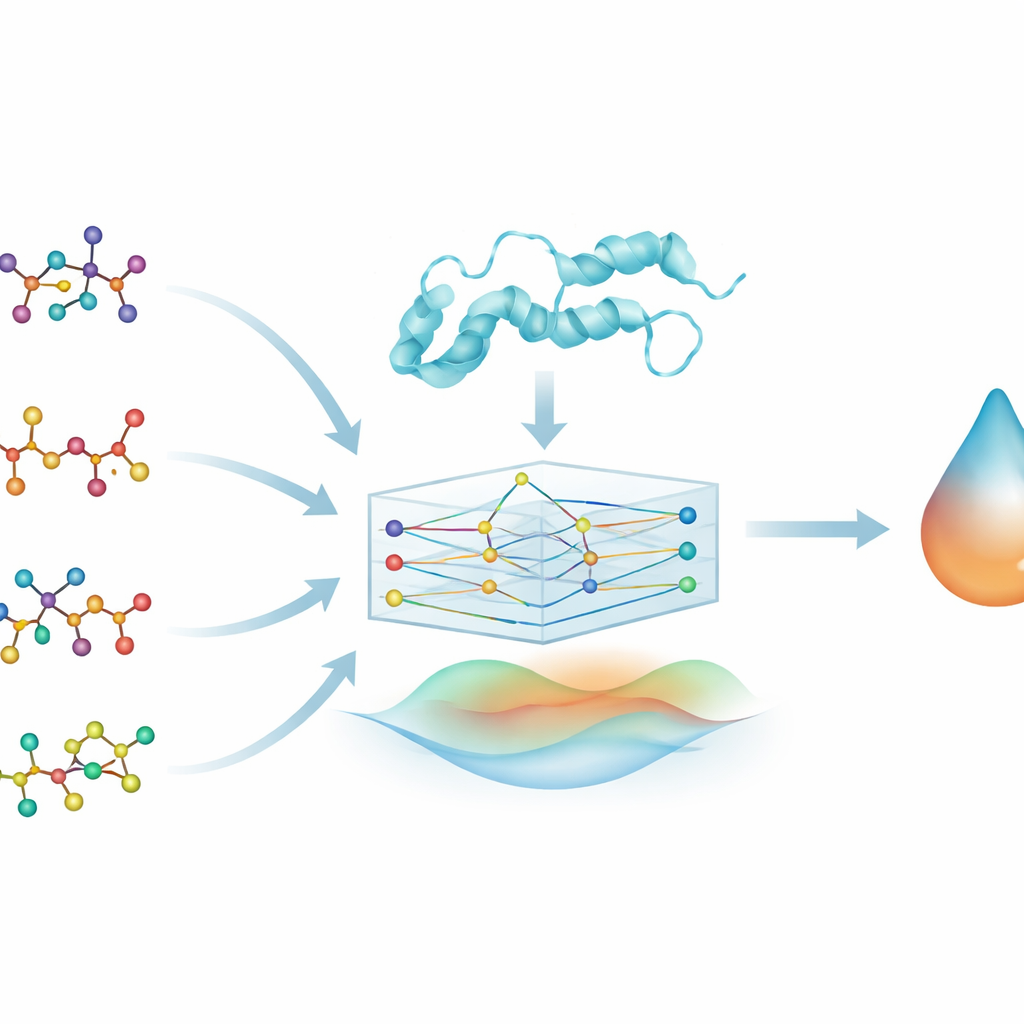
まったく新しい化合物を一から設計する代わりに、研究者らは薬の再利用に焦点を当てます――すでに承認され安全性の比較的確立した薬に新しい用途を見いだすことです。彼らは4種のよく知られたアルツハイマー薬(ブレキシプラゾール、ドネペジル、ガランタミン、リバスチグミン)を調べ、それぞれが神経細胞の成長と機能に関与するタンパク質キナーゼDYRK2にどの程度強く結合するかを評価します。DYRK2はアルツハイマー病ではほとんど研究されていませんが、シナプス、軸索、記憶との関連を示す初期の証拠があり、今日の治療を補完しうる興味深い標的です。
分子をネットワークに変換する
薬とタンパク質の関係を探るため、チームは各薬分子をグラフに変換します:原子を点に、化学結合をそれらをつなぐ線にします。DYRK2についても類似の表現を用い、アミノ酸配列を連結された単位の鎖として表現します。グラフニューラルネットワーク(GNN)と呼ばれる機械学習モデルはこれらのグラフ型入力を自然に扱い、接続に沿って情報を伝播させることで形状や化学パターンを学習します。これにより、PhysDual-GCNと名付けられたモデルは、薬とDYRK2の双方を単なる文字列や特徴の一覧ではなく、相互作用するネットワークとして“読み取る”ことができます。
物理学と人工知能の融合
創薬分野の多くの深層学習ツールはデータからのみ学ぶため、その内部動作が解釈しにくくなることがあります。本研究では、著者らは原子同士の相互作用に関する基本的な物理的考え方を意図的に組み込みます。学習されたグラフ特徴に加え、PhysDual-GCNは2つの古典的なエネルギー項を計算します:部分電荷間の静電的な引力と斥力を捉える項と、ファンデルワールス力の押し引きを記述する項です。これらの物理ベースのエネルギーはGNNの内部表現と結合され、最終的に予測される結合強度を出力します。実質的に、このモデルは標準的なドッキングプログラム(特にAutoDock Vinaなど)と同様の挙動を模倣するよう訓練されますが、より高速に、かつ馴染みのある物理原理に基づいています。
モデルが実際に予測するもの
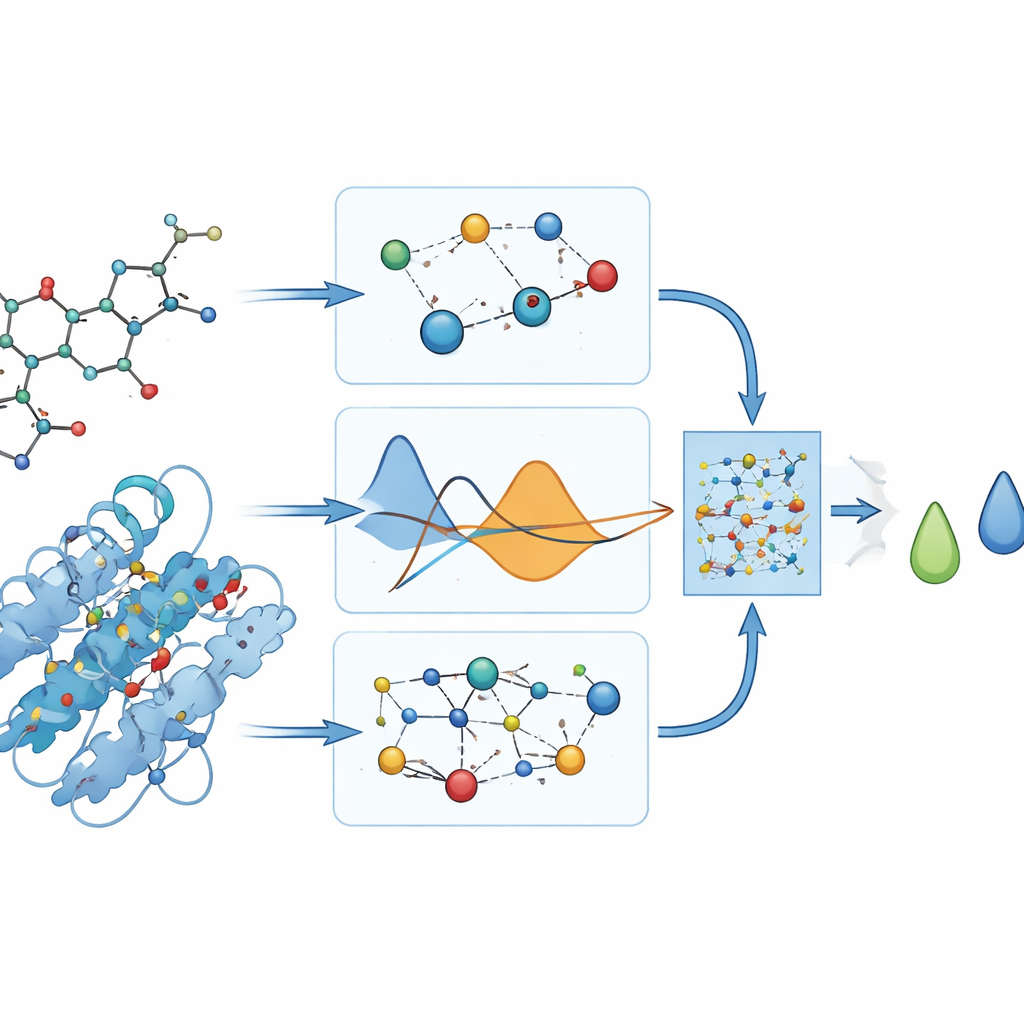
これらの薬がDYRK2にどれほど強く結合するかについての実験データが存在しないため、著者らはドッキングプログラムが出す「参照」結合スコア(エネルギー単位)に頼ります。彼らはそのスコアを訓練過程に直接与えることを避け、代わりにPhysDual-GCNがどれだけ学習したかを評価するために後からのみ使用します。4つのアルツハイマー薬について、モデルはドッキング値を小さな平均誤差(約0.3 kcal/mol程度)で再現し、化合物の順位付けも正しく行います:ドネペジルとブレキシプラゾールが最も強く結合し、ガランタミンとリバスチグミンはやや弱めながらも安定性はあると示されました。これらの結果は、物理情報を取り入れたGNNがより遅いドッキング実行の計算代替として機能しうることを示しています。
手法の約束と限界
これらの有望な数値にもかかわらず、著者らは研究の範囲が厳しく制限されていることを強調します。対象は4つの薬のみで、評価は実験的な生化学データではなく他の計算プログラムに依存しています。DYRK2タンパク質は主に一次元の配列グラフとしてモデル化されており、三次元構造全体を表現していないため、結合ポケットの詳細な立体形状はまだ考慮できません。物理的エネルギーも簡略化されており、標準的な力場パラメータとカットオフを用いています。したがって、この仕事は概念実証として見るべきであり、物理ガイド付きグラフニューラルネットワークが低データ環境で古典的ドッキングスコアをよく追跡できることを示す一方で、試験管や臨床で予測が現実に一致することをまだ証明してはいません。
今後のアルツハイマー研究への意味
非専門家に向けた主要なメッセージは、物理的知見を取り入れた賢いアルゴリズムが、従来の方法だけでは時間のかかる新しいアルツハイマー標的(例えばDYRK2)の探索をはるかに迅速に助ける可能性があるという点です。ドネペジルとブレキシプラゾールを有望なDYRK2結合薬として示し、ドッキング結果を近似する透明性のある手法を提供することで、PhysDual-GCNはより詳細な実験研究の出発点を提供します。より大規模な薬物ライブラリ、豊富な3Dタンパク質情報、実験による検証が加われば、この種のモデルは候補治療のスクリーニングや薬の再利用の方針決定に役立つ実用的なツールとなり、アルツハイマー病の進行を遅らせる・変えることを目指す取り組みに貢献しうるでしょう。
引用: Gider, V., Budak, C. A physics-informed graph neural network to approximate docking-based binding affinity for DYRK2 in Alzheimer’s drug repurposing. Sci Rep 16, 8357 (2026). https://doi.org/10.1038/s41598-026-35102-7
キーワード: アルツハイマー病, 薬の再利用, グラフニューラルネットワーク, タンパク質–リガンド結合, DYRK2キナーゼ