Clear Sky Science · ja
多包条虫(Echinococcus multilocularis)シスタチンBの結晶構造が示す古典的ステフィンの新たな特徴
肝臓寄生虫の“切り札”が重要な理由
多包虫症は、肝臓でゆっくりと発育するがんのように振る舞う小さな条虫感染症で、この長い名前が示す以上に深刻な病気です。致命的になることが多く、現在の薬は効果が乏しく副作用が問題になることもあります。本研究は寄生虫が作る特定の分子、EmCystatin-Bと呼ばれるタンパク質に着目し、それがどのようにして寄生虫の免疫回避に寄与するか、そして将来的に新しい治療標的になり得るかを明らかにしようとしています。
腫瘍のように増殖する危険な条虫
この病気は条虫Echinococcus multilocularisの幼虫期が原因です。人は汚染された食物や水などから誤って卵を摂取することで感染します。体内に入ると幼虫は主に肝臓に定着し、多数の小さな液胞を形成して周囲の組織に浸潤し、脾臓など近接する臓器へ広がり、場合によっては肺や脳など遠隔部位に達します。有効な治療がなければ、10〜15年で患者の9割以上が死亡するとされています。外科手術と長期の抗寄生虫薬の併用が現状では最良の選択ですが、早期診断が難しく薬剤が確実に感染を治癒するわけではありません。したがって、寄生虫が分子レベルでヒトとどう相互作用するかを理解することが重要です。
切断酵素の働きを無効化する寄生虫タンパク質
多くの動物、ヒトを含めて、シスタチンと呼ばれるタンパク質群は強力な分解酵素(システインプロテアーゼ)に対する安全装置の役割を果たします。これらの酵素は他のタンパク質を切断し、老朽化した細胞部品の分解や免疫応答の活性化などに重要です。寄生虫は宿主の酵素や免疫系を妨げるためにシスタチン様のタンパク質を作ることを学んで来ました。本研究ではE. multilocularis由来のシスタチン様タンパク質を同定し、EmCystatin-Bと命名しました。EmCystatin-Bの遺伝子は寄生虫の成熟した幼虫頭部(原頭節)で周囲の嚢胞組織より格段に活性が高く、タンパク質は細胞質や核に存在し、特に分裂中の“幹様”増殖細胞で目立ちました。in vitro試験では、EmCystatin-Bは免疫や組織リモデリングに関与する重要なシステインプロテアーゼであるヒトカテプシンBの活性を強力に阻害することが示されました。
馴染みのある折りたたみ、しかし予想外のひねり
EmCystatin-Bがどのように構築されているかを詳しく見るため、研究チームは精製タンパク質を結晶化し、X線結晶構造解析でほぼ原子分解能の三次元構造を解きました。他のシスタチン科タンパク質と同様に、各EmCystatin-B分子は特徴的な形状を持ち、中央のらせん状領域とそれを支える平坦なβストランドが楔形を作り、通常プロテアーゼの活性部位に嵌まる構造です。配列や分泌シグナルペプチドの欠如から、EmCystatin-Bは一般に小さく細胞内に存在し、安定化する二硫化結合を持たないことが多い「ステフィン」サブグループに属します。驚くべきことに、各ユニットは予想される折りたたみをしているものの、それらが互いに結合する様式はヒトの対応タンパク質(シスタチンB)と比べて異常で種特異的でした。
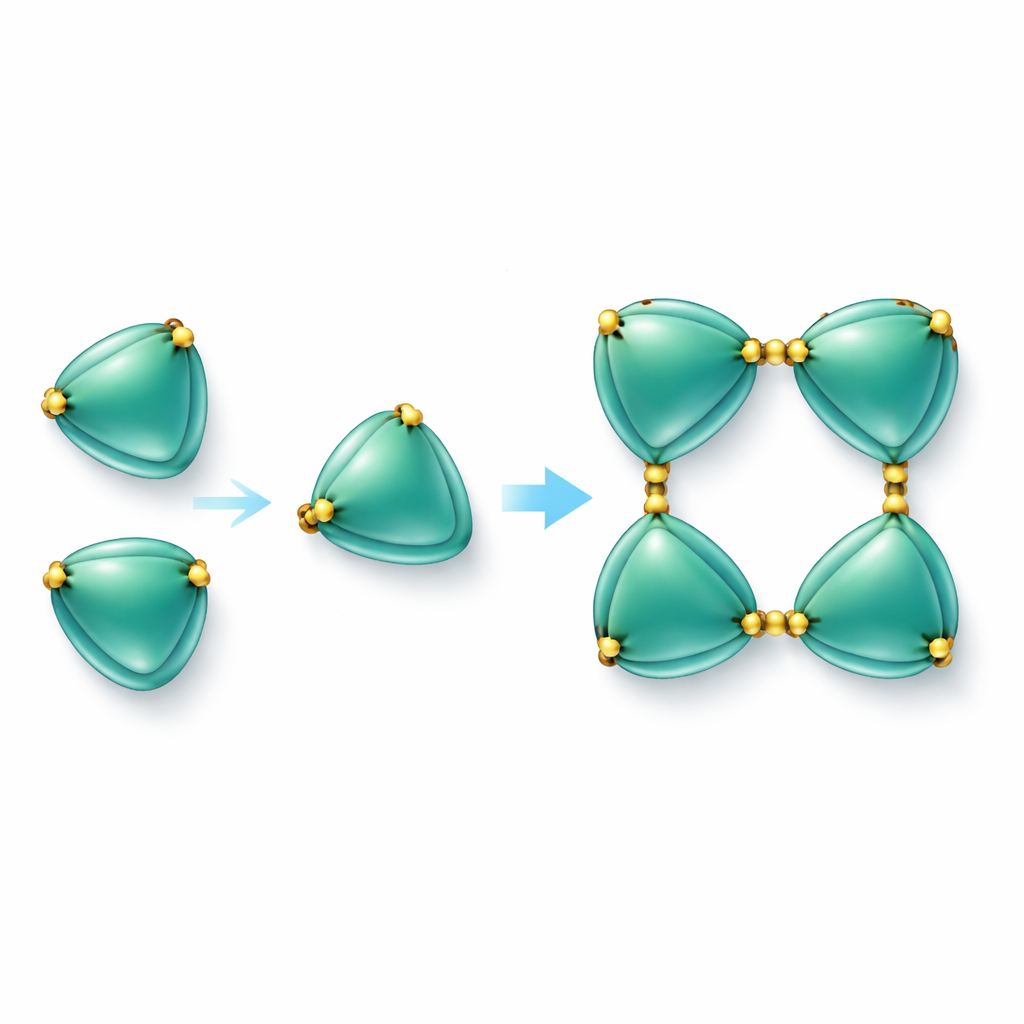
硫黄の橋でつながるタンパク質鎖の構築
最も注目すべき発見は、EmCystatin-B分子が単独で浮遊するだけでなく、段階的に結合して二量体(ペア)、さらに四量体(四つ組)を形成することでした。初期の二量体を作る機構は2種類あります。1つはある分子の一部が飛び出して隣の分子の構造を補完する「ドメインスワッピング」と呼ばれる現象、もう1つは二つの分子が二硫化結合によって結び付けられる方法です。EmCystatin-Bでは、1つの分子の位置4のシステインがパートナー分子の位置76のシステインと結合します。こうした交差結合が4ヶ所できることで四量体が安定化します。古典的なステフィンは通常このような二硫化架橋を欠くため、複数の分子間二硫化結合を用いることは全く新しい発見です。研究者がこれらの重要なシステインを別のアミノ酸に置換すると、タンパク質は高次集合体を効率よく形成できなくなり、カテプシンBを阻害する能力が著しく低下しました。
感染と戦う上での意味
専門外の方に向けた結論としては、寄生虫が一般的なタンパク質ファミリーを特別に配線し直し、追加の化学的“リベット”を使って複数の阻害ユニットを固定するよう進化したということです。このオリゴマー型は本来なら感染制御に寄与する宿主酵素を効果的に止めるために重要であるように見えます。EmCystatin-Bの正確な構造とそのユニークな二硫化架橋による集合様式を明らかにしたことで、シスタチンタンパク質が種ごとにどのように調整され得るかの理解が深まりました。長期的には、これらの知見がEmCystatin-Bの保護的効果を阻害する薬剤の設計や、逆にその免疫抑制特性を模倣して炎症性疾患を治療する手法の開発に役立つ可能性があります。
引用: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
キーワード: 多包虫症(alveolar echinococcosis), Echinococcus multilocularis, シスタチンB, タンパク質構造, 免疫調節