Clear Sky Science · ja
配列ドメイン間相互作用のリガンド誘導リモデリングによるNLRP3インフラマソーム組み立ての破壊
暴走する炎症を抑える意味
関節炎や痛風から心血管疾患や神経変性まで、多くの慢性疾患は細胞内の過剰に活性化した免疫アラームシステムにより悪化します。このアラームの重要な構成要素であるNLRP3インフラマソームは感染と戦うのに役立ちますが、誤作動すると有害な炎症を引き起こします。本研究はE9と名付けられた新しい低分子を記述しており、NLRP3活性化の初期段階を標的にすることで、免疫系全体をシャットダウンせずに有害な炎症を抑える薬剤設計の新たな視点を提供します。
裏の顔を持つ細胞の火災報知器
危険を感知すると、免疫細胞は分子レベルの火災報知器のように機能する大きなタンパク質複合体、NLRP3インフラマソームを組み立てます。形成されると、この構造はカスパーゼ-1と呼ばれる酵素を活性化し、さらにサイトカインIL-1βやIL-18など強力な炎症性シグナルを活性化します。これらのシグナルは感染と戦い、損傷組織を除去するために重要です。しかし、インフラマソームが長時間オンのままになったり、誤ったタイミングで活性化されたりすると、関節、血管、脳などの慢性炎症性疾患に寄与します。したがって研究者たちは、免疫を広範に抑制することなくNLRP3を精密に制御する方法を世界中で探しています。
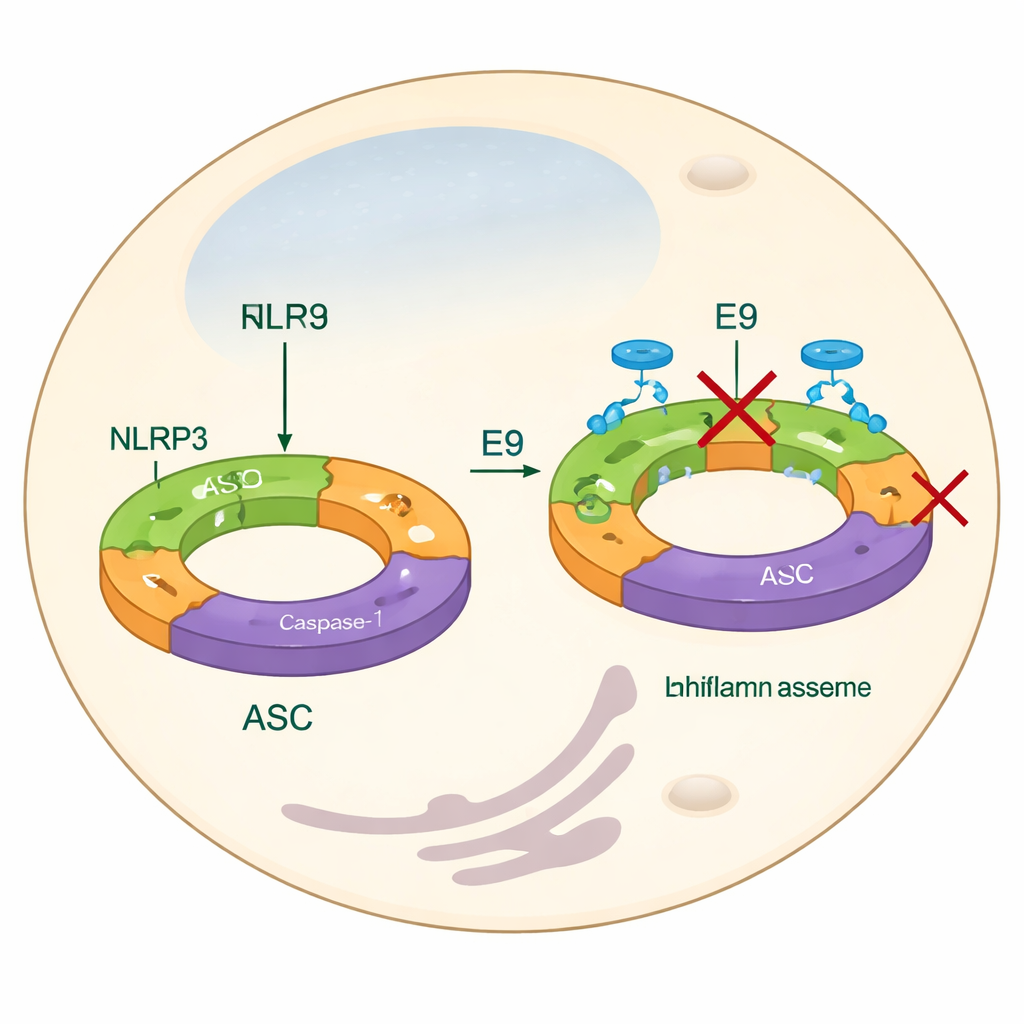
従来の薬剤標的を超えて見る
現在の多くのNLRP3抑制戦略は、IL-1βのような終末産物を阻害するか、ATPなどのエネルギー分子を用いる中心的なエンジン様ドメインの働きを妨げることに焦点を当てています。これらのアプローチは有効な場合もありますが、組み立ての最初期段階を見逃したり、NLRP3タンパク質が機能的な装置を形成する際の結合様式に十分に対処しないことがあります。本研究では、代わりにピリンドメインに注目します。これは個々の単位が長いフィラメントにスナップ結合するのを助けるNLRP3の一部です。これらのフィラメントはさらにアダプタータンパク質ASCを呼び寄せ、細胞内に明るい“スぺック”を形成します—インフラマソーム活性化の視覚的指標です。ピリンドメイン同士の適合を妨げる化学物質を見つけることで、研究チームはインフラマソームがそもそも形成されるのを止めることを目指しています。
鎖を断つ分子の発見
研究者らは巧妙な光学的アッセイを用いて、合成した1500種の低分子ライブラリをスクリーニングしました。ルシフェラーゼ酵素の分割片をNLRP3のピリンドメインに融合し、二つのピリンドメインが結合すると酵素フラグメントが再集合して光を発しました。ピリン–ピリン接触を阻害する化合物は光シグナルを低下させました。このスクリーニングから4つの有望な候補が見つかり、そのうちE9は強力かつ一貫した阻害を示して際立ちました。マイクロスケール熱流動法(MST)と呼ばれる手法による追試測定では、E9がサブミクロモーラー濃度でピリンドメインに強く結合することが示され、その効果がランダムなアーティファクトではなく特異的相互作用によるものであることが確認されました。
生細胞内での効果の確認
E9が生体内でも機能するかを評価するため、チームは蛍光標識されたASCを作るように設計されたヒトの免疫様細胞を用いました。これらの細胞に細菌由来成分と二次トリガーを与えると、NLRP3が活性化されASCタンパク質が明るいスぺックに凝集し、顕微鏡下で数えられます。E9存在下では、これらのスぺックの数は著しく減少し、既知のいくつかのNLRP3阻害剤と同等かそれ以上の効果を示しました。これは、ピリンドメイン接触の妨害だけでインフラマソームの組み立てと炎症性細胞死の初期段階を実験室条件下で低減できることを示しています。
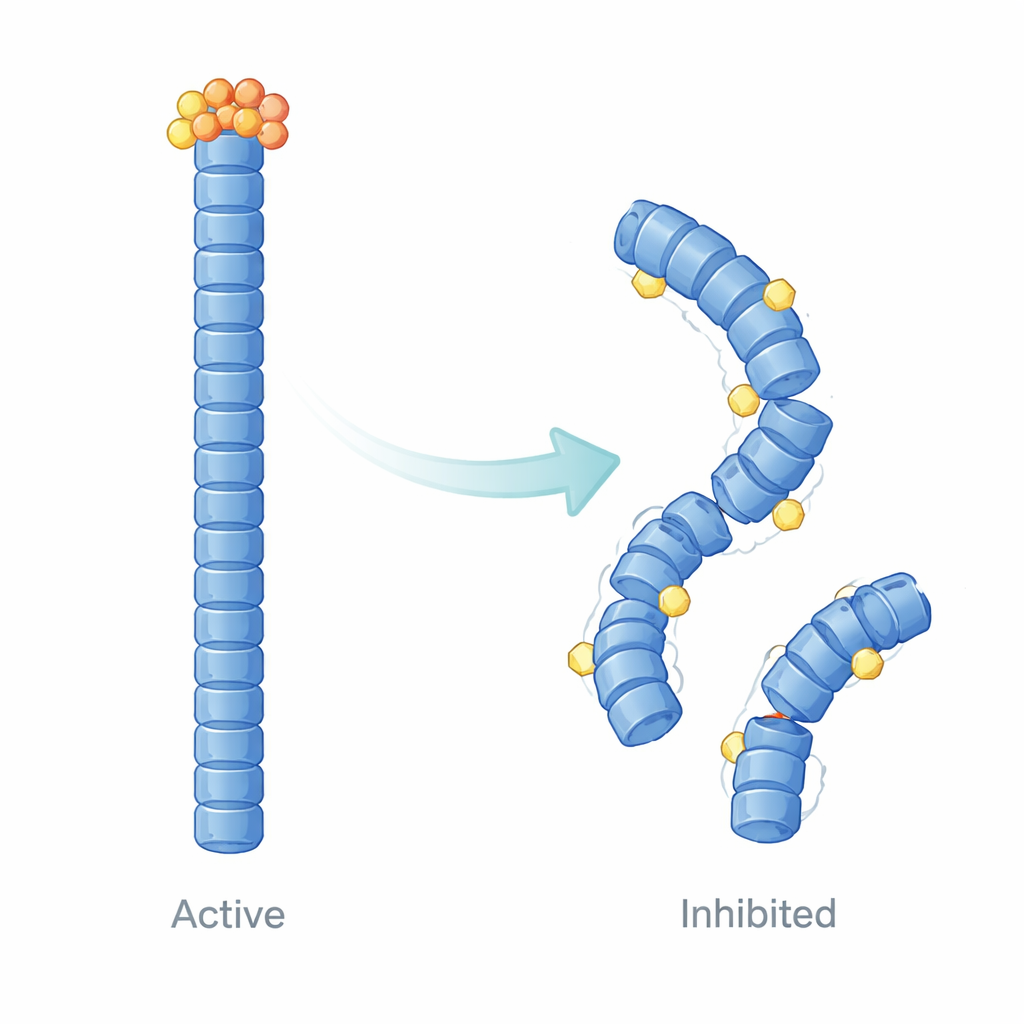
E9がインフラマソーム足場をどのように再形成するか
結合を単に測定するだけでなく、著者らは計算構造モデリングと分子動力学シミュレーションを用いて、E9が時間とともにNLRP3フィラメントの挙動をどのように変えるかを可視化しました。彼らの計算は、E9がピリンドメイン同士が接触する特定の表面に入り込み、フィラメントを微妙に緩めて形を変えることを示唆します。一様に安定で協調的な構造の代わりに、フィラメントは不均一になります:E9が結合した近傍領域はより柔軟になり精密な整列を失い、他の部分は動的に孤立します。これらの変化は、効率的なASCの呼び込みに必要な大規模な運動と密接な通信を弱め、細胞内で観察されるスぺック形成の低下に対する物理的説明を提供します。
将来の治療への示唆
総じて、これらの知見はE9を、NLRP3のエネルギー利用や終末産物の阻害ではなく、NLRP3構成要素間の界面を破壊することで作用する新しいクラスのインフラマソーム標的薬のプロトタイプとして位置づけます。現時点の研究は試験管アッセイ、計算シミュレーション、および培養細胞に限られており、動物や人でのさらなる研究が必要ですが、慎重に設計された低分子がインフラマソーム足場自体をリモデリングできることを示しています。暴走する炎症が病因となる患者にとって、こうした界面に焦点を当てた薬剤は、必須の防御は大部分維持しつつ有害な免疫活性化をより精密に抑える手段を将来提供し得るでしょう。
引用: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
キーワード: NLRP3インフラマソーム, ピリン(pyrin)ドメイン, 低分子阻害剤, 自然免疫, パイロトーシス