Clear Sky Science · ja
サルコペニア患者の骨格筋における異常な選択的スプライシングのトランスクリプトーム特性解析
加齢した筋肉が力を失う理由
サルコペニア――加齢に伴う筋肉量と筋力の漸進的な低下――は、高齢者が階段を上ったり買い物袋を運んだりする日常的な動作に苦労する主因の一つです。本研究は、細胞がどのタンパク質を作るかを指示するメッセージであるRNAのレベルで、老化筋肉の内部を詳しく調べます。著者らは、サルコペニアでは多くのRNAメッセージが異常な形で切り貼りされており、その結果筋肉のエネルギー産生が乱れ得ること、そして新たな治療標的を示唆することを示しています。
筋肉喪失と体内の遺伝子“編集”システム
遺伝子はDNAに書かれていますが、細胞はまずそれをRNAのコピーとして扱います。RNAのメッセージが機能する前に、細胞は通常それをトリミングしスプライス(つなぎ替え)します――まるで映画を編集するように――一つの遺伝子から複数のタンパク質バージョンを生み出せるようにするのです。このプロセスは「選択的スプライシング」と呼ばれ、収縮や修復、運動への適応のために精密に調整されたタンパク質を必要とする筋肉で特に活発です。スプライシングが誤ると、誤ったタンパク質バージョンが生じたり重要なものが失われたりして、筋ジストロフィーや一部の脳疾患の要因となります。著者らは、同様の隠れたRNAの誤編集がサルコペニアを促しているのではないかと考えました。
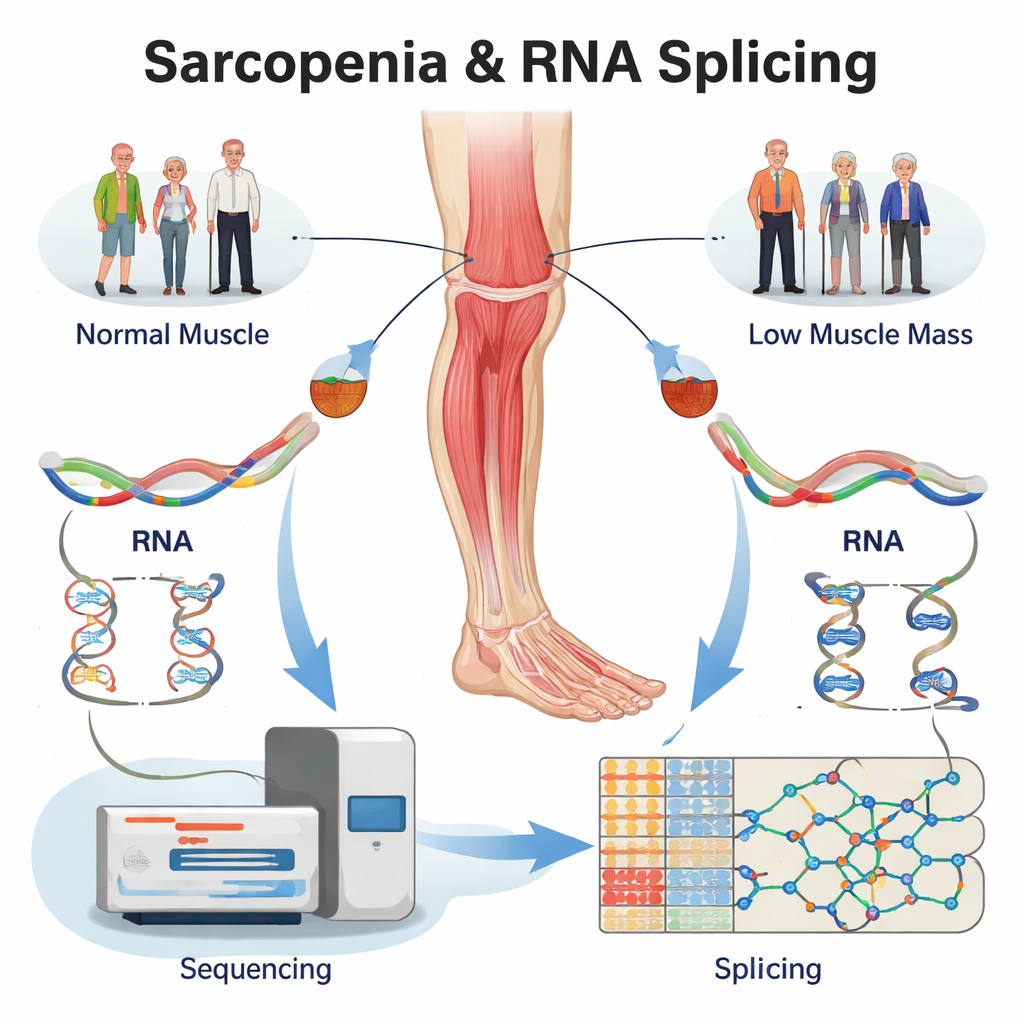
既存データの再解析で見つける隠れたRNAエラー
研究チームは新規被験者を募集する代わりに、ヒト大腿筋生検から得られた既存の大規模RNAシーケンスデータを再解析しました。サンプルは以下の4群から採取されました:明確なサルコペニアを有する高齢者、筋肉量のみが低下している人、筋力のみが低下している人、そして年齢対応の健康対照群。特殊なソフトウェアを用いて、まず疾患筋で数百の遺伝子が発現上昇または低下していることを確認しました。さらに重要なことに、各遺伝子のRNAがどのようにスプライスされているかを詳しく調べ、健康な筋肉と比べて3つの問題群で5,000件を超えるスプライシング変化を記録しました。これらの変化はエクソンのスキップや代替切断部位の選択などいくつかの基本的なタイプに集中しており、タンパク質構造を大きく変えることが知られているパターンでした。
エネルギー工場と細胞の“燃料計”経路が乱れる
検出されたスプライシング変化は筋肉生物学の中心に位置する遺伝子群に現れていました。多くはミトコンドリアの構成要素を作る遺伝子で、ミトコンドリアは筋収縮にエネルギーを供給する小さな発電所です。サルコペニア筋では、栄養を可利用なエネルギーに変換する酸化的リン酸化に関与する16の遺伝子のスプライシングが変化しており、特に電子伝達やプロトンポンピングを担うミトコンドリア複合体の構成要素に影響が集中していました。ほかにも、細胞のエネルギーと修復に重要な分子であるNAD⁺を作る・使う遺伝子に変化が見られました。単に発現量が増減しているのではなく、CD38、PARP2、いくつかのシルトゥインなどの重要な酵素が異なるRNAバリアントを産生しており、NAD⁺の産生と消費のバランスがスプライシングレベルで歪められていることを示唆します。影響を受けた遺伝子はまた、細胞の燃料計やストレス応答として機能するAMPKやFoxO経路などのよく知られた筋肉シグナル伝達経路にも集積していました。
異なる段階間、そして種を越えた共通パターン
注目すべきことに、同じ遺伝子の多くが、明確なサルコペニアの人々だけでなく、筋肉量のみが低下している人や筋力のみが低下している人にもスプライシング変化を示しました。これは、異常なスプライシングが早期に始まり、病態の異なる臨床表現型に共通していることを示唆します。これらの変化が動物モデルでも再現されるかを検証するため、研究者らはステロイドであるデキサメタゾンを用いてマウスに筋萎縮を誘導しました。これはサルコペニアの一部の特徴を模倣する一般的な方法です。マウスは握力低下や走行・バランス試験での成績低下を示しました。マウス筋のRNAをシーケンスしたところ、再び数百の遺伝子でスプライシング変化が見つかりました。これらのうち約5分の1はヒトのサルコペニア遺伝子と重複し、多くは転写制御、クロマチン構造、スプライシング自体を制御する遺伝子――細胞の全タンパク出力を再構築し得る上位のスイッチ――に関係していました。
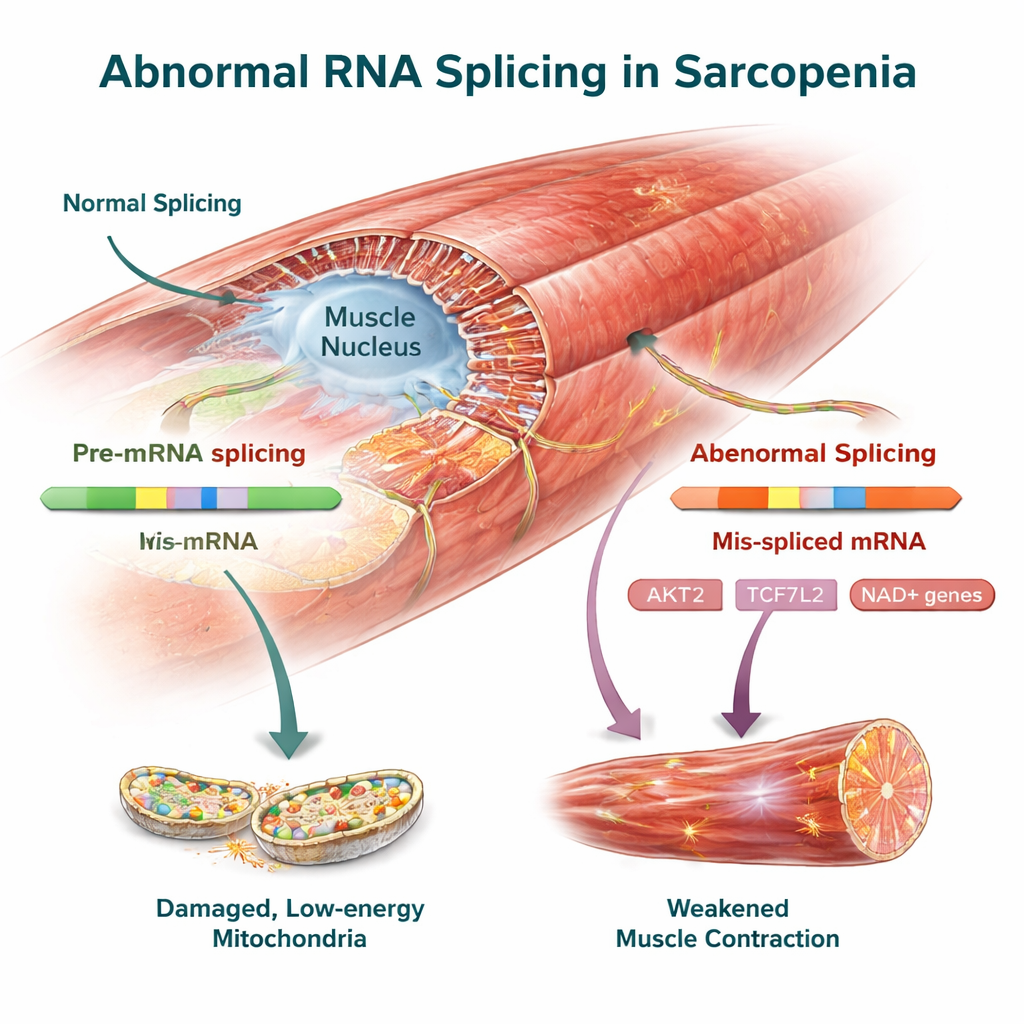
治療標的になり得る主要な筋制御遺伝子
種を越えた変化の中には、すでに筋の健康に関連づけられているいくつかの遺伝子が含まれていました。筋の成長とタンパク質合成の中心的調節因子であるAKT2は、ヒトとマウスの両方で特徴的なスプライシング変化を示し、筋量を維持する能力を弱める可能性があります。Wntシグナル経路の一部であるTCF7L2や、筋の内部骨格の組織化やタンパク質品質管理に関わるFMNL2およびUSP40も異なるRNAバリアントを示しました。研究チームはこれらのスプライシング変化をマウス筋で実験的に確認しており、これらがデータ解析のアーティファクトではなく疾患の実在する特徴であるという主張を強めています。
虚弱予防にとっての意義
専門外の読者にとっての要点は、サルコペニアが単に筋肉の“摩耗”や遺伝子のオン・オフだけでは説明できないということです。筋細胞が自身の装置を作り維持する方法を導くRNAメッセージの広範な誤編集、特にエネルギーを生み出しストレスを感知するシステムに関係する誤編集が関与しています。スプライシングは理論的には精密に設計されたRNAベースの薬で是正可能であるため、ここで発見された保存されたスプライシングエラー――特にAKT2やTCF7L2のような遺伝子におけるもの――は、高齢の筋肉がより長く強さを保つのを助ける治療法を探るための新たな手がかりを提供します。
引用: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
キーワード: サルコペニア, 筋肉老化, RNAスプライシング, ミトコンドリア, AKT2