Clear Sky Science · ja
トランスサイレチン安定化の現象論的モデル
患者と家族にとってなぜ重要か
トランスサイレチン(TTR)は本来血中に存在する正常なタンパク質ですが、崩壊して断片が心臓や神経に有害な沈着物を作ることがある重篤な疾患、トランスサイレチンアミロイドーシスを引き起こします。タファミディスやアコラミディスといった新しい薬剤は、このタンパク質を安全な四量体の形に保つよう設計され、多くの患者で予後を改善してきました。それでも臨床現場では不可解な現象が観察されます:治療を受けた患者の血中TTR濃度が30%以上上昇することがあり、その理由は一見して明らかではありません。本稿は、簡略化した数学的モデルを用いて体内で何が起きているか、そしてそれがこれらの薬の作用機序について何を意味するかを探ります。 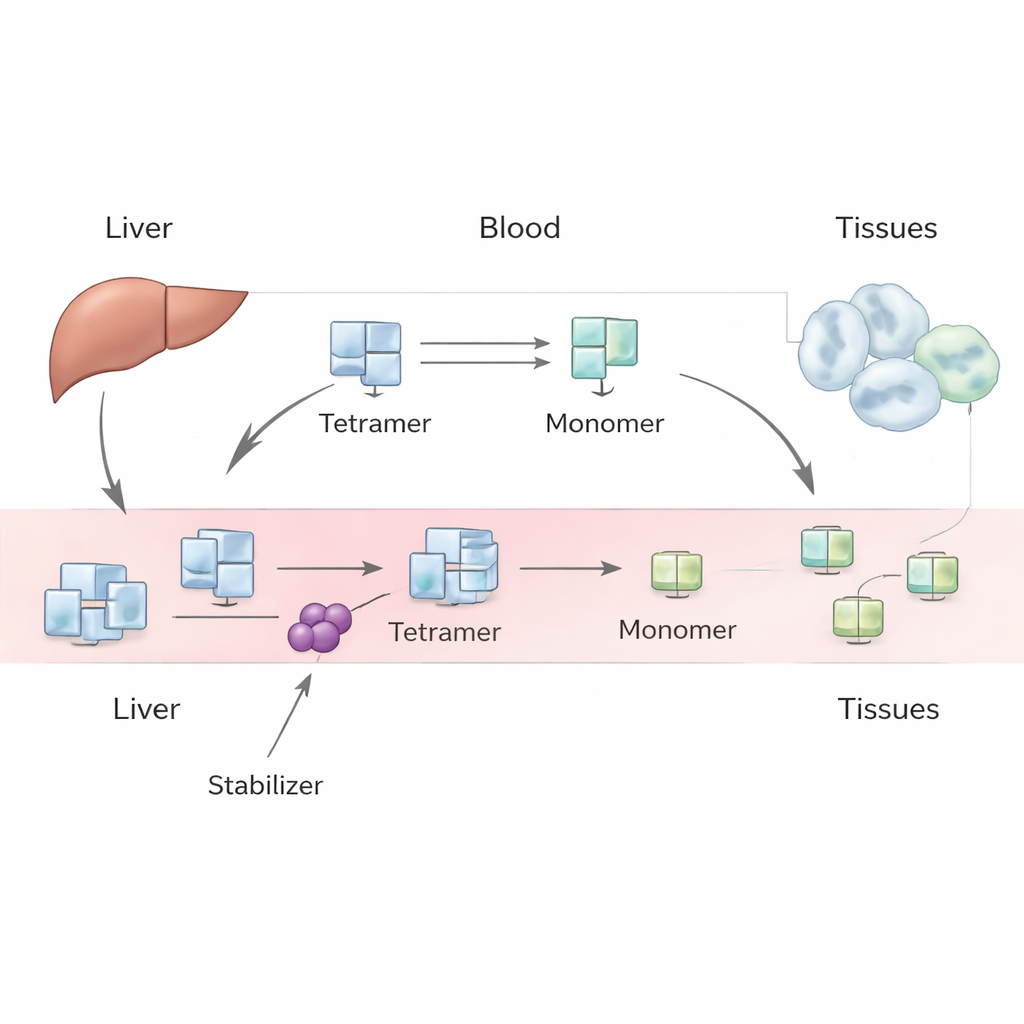
助けにも害にもなりうるタンパク質
TTRは主に肝臓で作られ、通常は四つの同一サブユニットが束になった安定した四量体として血中を循環します。甲状腺ホルモンやビタミンAを運搬します。加齢や遺伝的変異などの条件下でこの四量体は解離して単量体(モノマー)になり得ます。これらの単量体は誤って折りたたまれ、アミロイド線維として凝集し組織を損傷し、心筋症や神経障害を伴うトランスサイレチンアミロイドーシスを引き起こします。タファミディスやアコラミディスのような薬剤は四量体に結合して解離しにくくし、疾患の進行を遅らせるよう設計されています。しかし、患者がこれらの薬を開始すると、血中で測定されるTTR量が確実に上昇し、その増加は単純な実験で予想されるより大きいのです。
複雑な系を単純に描く
著者らはこの謎に対し、現象論的モデル—微視的な詳細より観察される全体的挙動に注目するモデル—で取り組みます。枠組みでは、肝臓が一定速度でTTR四量体を産生し、それが血流に入ると考えます。循環中の四量体は解離して単量体になり再結合することができ、四量体と単量体の両方が組織への取り込みや分解によって血中から除去され得ます。四量体と単量体について質量保存の二つの方程式を記述することで、著者らは異なるシナリオを検討します:単量体が主に再び四量体に戻る場合、素早く除去される場合、そして両者が重要な中間の場合です。歴史的なヒトトレーサー研究と現代の実験データを用いて、四量体のクリアランス速度、解離速度、薬剤がこの解離をどれほど抑えるかといった主要な量を推定します。
四量体の安定化だけでは十分ではない理由
これらの推定値を用いて研究者らは鋭い問いを投げかけます:もし薬が四量体の解離を完全に防げるとしたら、血中TTRはどれだけ上昇するか?あり得るすべての領域で、その答えは控えめで—典型的なパラメータ値では最大でもおよそ15%程度、多くは単量体の扱われ方によってそれより小さい—という結果になります。これは治療患者で観察される>30%の増加からは大きく乖離しています。既知のパラメータに寛大な不確実性を許してもこの不一致は残ります。したがってモデルは、単に四量体の解離を遅らせるだけでは臨床効果全体を説明できない可能性を示唆します。TTRの産生速度、細胞への取り込み、あるいは分解を制御する他の過程も、安定化薬投与時に変化している必要があると示されます。 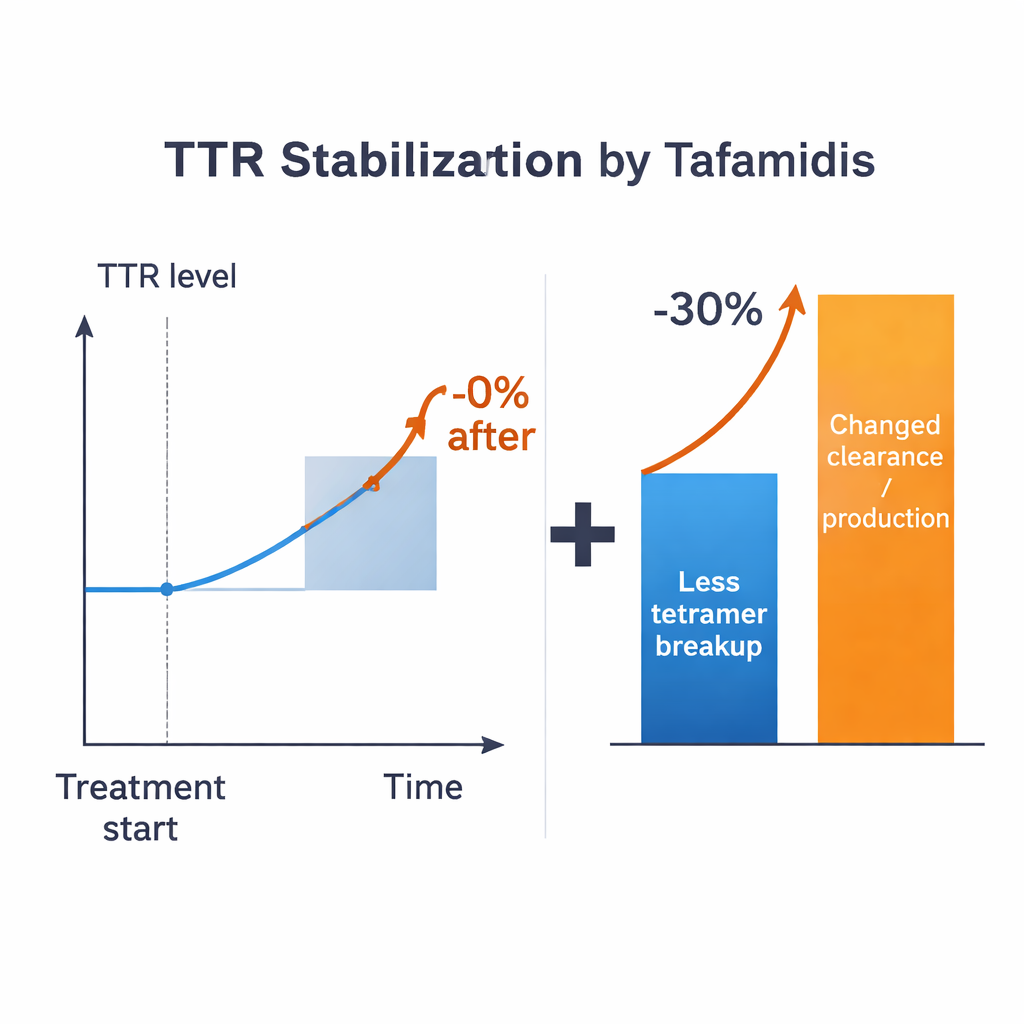
薬剤レベルと巧妙な実験からの手がかり
薬物曝露とTTR挙動を結びつけるために、著者らはタファミディスの基本的な薬物動態モデル(薬が体内を時間的にどう移動するか)と、特殊な「サブユニット交換」アッセイを組み合わせます。これらの実験では、標識された四量体と非標識の四量体をヒト血漿中で混合し、サブユニットの徐々の入れ替わりを観察することで四量体がどれくらいの頻度で解離するかが明らかになります。異なる薬物濃度でこの過程を測ることで、アルブミンや甲状腺ホルモンにどれだけ薬が結合しているかを知らなくても、タファミディス濃度と実効的な四量体安定性の間に直接的でデータに基づく関係が得られます。この現象論的な結びつきはモデルに取り込まれ、多くの生化学的未知を巧みに回避します。それでもこの利点があっても、計算は臨床で観察される増加の概ね半分程度で上限を打つにとどまり、クリアランス、細胞内取り込み、分解、あるいは合成の変化が物語の一部である必要性をさらに支持します。
今後に向けて意味すること
専門外の読者にとっての要点は、これらの安定化薬は単にTTR四量体を「接着」しているだけではなさそうだということです。薬はおそらく、体がこのタンパク質を生産、除去、再利用する仕組みにも影響を与えています。著者らは、自分たちのような単純で透明なモデルが強力であると論じており、我々の理解のギャップを露呈させ、具体的な実験の方向性を示します—例えば、単量体がどれほど速く除去されるか、異なるTTR形態が細胞にどれほど速く取り込まれるか、薬剤結合TTRが非結合のタンパク質と比べて異なる扱いを受けるかを直接測ることなどです。これらの問いへのより良い答えは、トランスサイレチンアミロイドーシスの治療を洗練するだけでなく、正常なタンパク質が有害な凝集体に変わる他の疾患に関する一般的な規則を明らかにするかもしれません。
引用: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
キーワード: トランスサイレチンアミロイドーシス, タンパク質安定化, タファミディス, 薬物動態モデリング, アミロイド疾患